Questões de Concurso
Foram encontradas 9.182 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere as duas soluções aquosas ácidas apresentadas a seguir:
I. Ácido sulfúrico (H2SO4), um ácido forte (α = 100%), 0,1 mol/L.
II. Ácido acético (CH3COOH), um ácido fraco (α = 10%), 0,1 mol/L.
O pOH do ácido sulfúrico e o pH do ácido acético são respectivamente
É comum as estruturas dos compostos orgânicos apresentarem 2, 3 ou até 4 funções orgânicas. Observe a seguinte estrutura:
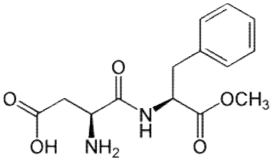
As funções orgânicas representadas na estrutura
acima são:
A acidez do leite na amostra, expressa em porcentagem (massa/volume) é, aproximadamente:
A equação química a seguir representa a ozonólise do ciclopenteno formando a substância X:
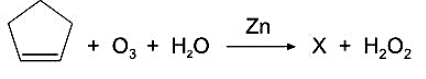
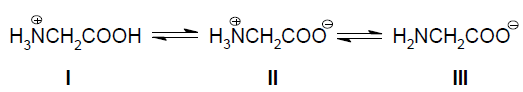
A partir da análise da figura é correto afirmar que a glicina assumirá estrutura predominantemente
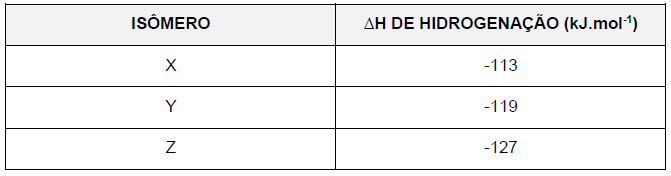
Sobre esses isômeros, é correto afirmar que
Observe a rota sintética a seguir:
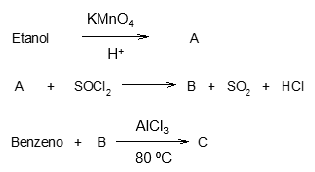
A nomenclatura do produto representado por C é
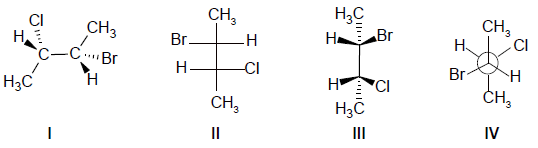
Sobre essas representações é correto afirmar que
O valor da variação de entropia da vizinhança desse sistema a 25°C, em J.K-1 , é:
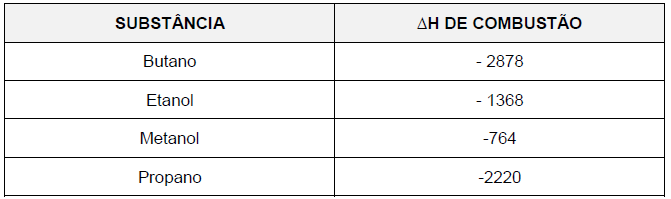
O combustível que lança na atmosfera a maior quantidade de gás poluente, para uma mesma quantidade de energia produzida, é
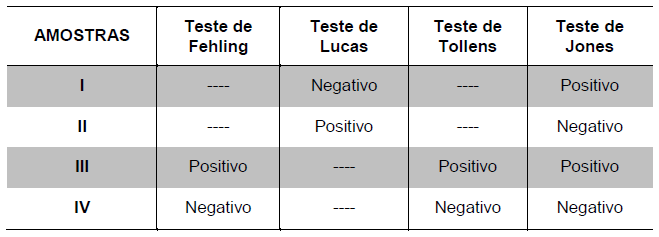
O aluno concluiu que as amostras contidas nos frascos I, II, III e IV eram, respectivamente,
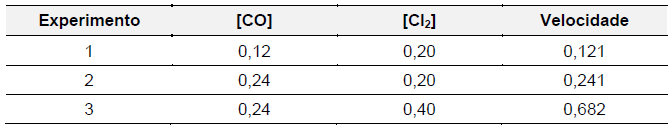
Dado que log 2,8 = 0,45 e log 2 = 0,3, o valor da constante da velocidade desta reação é
4 NH3(g) + 5 O2(g) → 4 NO(g) + 6 H2O(g) 2 NO(g) + O2(g) → 2 NO2(g) 3 NO2(g) + H2O(l) → 2HNO3(aq) + NO(g)
Supondo-se que o rendimento esperado nesse processo seja de 90% e que a amônia utilizada apresente 20% de impurezas, a massa de amônia, em toneladas, necessária para obtenção de 6,3 t de ácido nítrico será de, aproximadamente:
Os nomes dos compostos I e II são, respectivamente,
A concentração aproximada de pireno nessa solução, expressa em mol.L-1 , é