Questões de Concurso
Foram encontradas 3.161 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!


Com relação à reação apresentada e às espécies nela envolvidas, e considerando a primeira constante de ionização ácida do H2O2 igual a 2,4 × 10-12, julgue o item a seguir.
Átomos de ferro e de manganês com números de massa iguais
a 55 e 54, respectivamente, possuem o mesmo número de
nêutrons.


A partir das posições relativas dos elementos na tabela periódica, é possível inferir que um átomo neutro de ferro apresenta maior raio atômico do que um átomo neutro de manganês.


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
Se, na queima de um artefato pirotécnico ocorrera decomposição do carbonato de bário, de acordo coma reação química BaCO3(s) → BaO(s) + CO2(g), entãoa entalpia padrão dessa reação de decomposição (ΔHx),calculada a partir dos dados listados na tabela seguinte,será ΔHx = ΔH1 - ΔH2 + ΔH3.
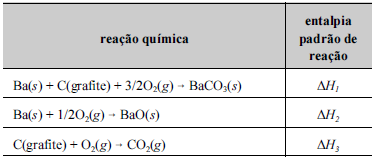


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
Na queima do magnésio metálico em presença de oxigênio,
ocorre a redução do magnésio com o consequente consumo
de 1 mol de elétrons por mol de átomos de magnésio.


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
Considere que a reação entre antimônio e sulfeto produza
o sal Sb2S3, pouco solúvel e de cor ocre que, em meio
aquoso, dissocia-se parcialmente, de acordo com o
equilíbrio Sb2S3(s)2Sb3+(aq) + 3S2-
(aq). Nesse caso,
a concentração de sulfeto necessária para iniciar a formação
do sólido Sb2S3 em uma solução aquosa de Sb3+
de concentração x mol/L deverá ser maior que
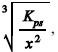 em que Kps é a constante de equilíbrio da reação precedente.
em que Kps é a constante de equilíbrio da reação precedente.


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
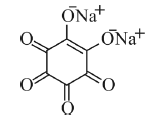
Considere que na reação do bário com o rodizonato de sódio, mostrado na figura a seguir, haja apenas troca de cátions para gerar a coloração laranja. Nessa situação, para formar o composto rodizonato de bário, serão necessários mais de 1.000 μg de rodizonato de sódio para reagir totalmente com 1.306,5 μg de nitrato de bário.


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
O composto p-aminofenol é mais solúvel em água do que
o composto 1-amino-4-metilbenzeno.


Tendo como referência a figura e os dados da tabela precedentes, julgue o item a seguir.
O sulfeto de sódio é um sólido molecular.
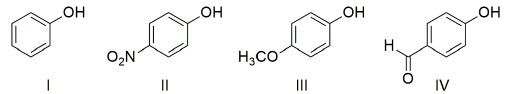
Considere os seguintes fenóis:
A + 3B → 2C + D
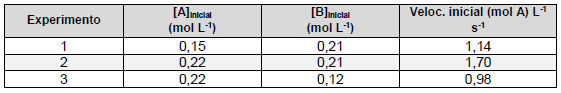
A partir dessas informações, considere as seguintes afirmativas:
1. A reação é de primeira ordem em relação ao reagente A, e também de primeira ordem em relação ao reagente B. 2. A lei de velocidade da reação, baseada na estequiometria da reação, é velocidade = k [A][B]3 , e a ordem global da reação é 4. 3. A lei de velocidade da reação, baseada nos dados experimentais, é velocidade = k [A][B], e a ordem global da reação é 2. 4. O valor de k para o experimento 2 é 36,79 L mol-1 s -1 .
Assinale a alternativa correta.

Considerando a dissociação de um ácido genérico (HA) em água, conforme a equação mostrada acima, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) Se HA = HCl, ele estará completamente dissociado e a [H3O+ ] = [HCl]inicial. ( ) HA é o ácido conjugado da H2O enquanto H3O+ é o ácido conjugado de A- . ( ) HA é um ácido de Bronsted-Lowry e H2O é uma base de Bronsted-Lowry. ( ) Se HA = ácido acético, ele estará completamente dissociado e a [H3O+ ] = [ácido acético]inicial.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
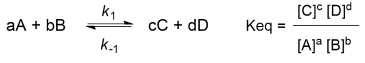
Assumindo que as equações acima são modelos que podem ser aplicados a qualquer reação química, é correto afirmar que, no equilíbrio:
1. as concentrações de A, B, C e D são iguais. 2. as concentrações de A, B, C e D não se alteram com o tempo. 3. a reação para de acontecer, logo, a formação de produtos é interrompida. 4. a constante de velocidade da reação direta (k1) é igual à da reação inversa (k-1).
Assinale a alternativa correta.
Com relação a decaimento, considere as seguintes equações:
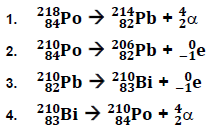
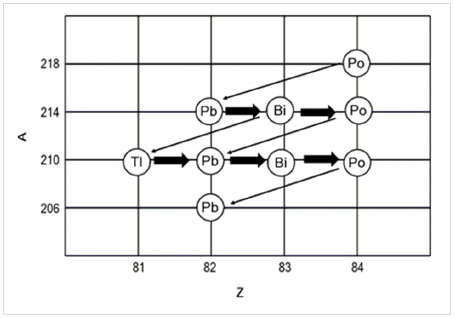
São equações de decaimento:
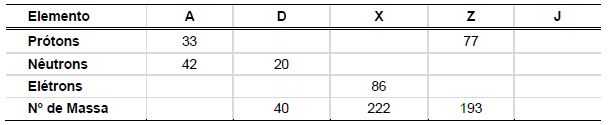
Supondo que os elementos A, D, X, Z e J possam ocorrer na forma de isótopos, e com base nas informações contidas na tabela, é correto afirmar que:
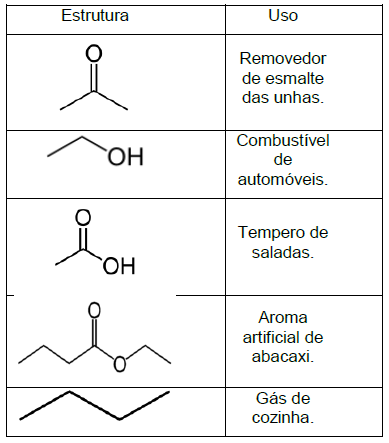
A sequência CORRETA que apresenta o nome dos compostos orgânicos, de cima para baixo, é:
A seguir são apresentadas as fórmulas estruturais do Aspartame e do Neotame:
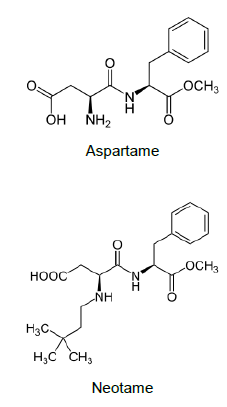
A alternativa que contém a função orgânica que NÃO está presente na estrutura do Aspartame e do Neotame é
A proteção catódica é um método utilizado para a proteção de estruturas. Com isso, tubulações e tanques de estocagem, entre outros, são protegidos por esse método. Em uma aula de química, deseja-se estudar a proteção da corrosão de um equipamento constituído basicamente por ferro, empregando-se o método da proteção catódica com o uso de um metal de sacrifício. Nesse contexto, a tabela a seguir mostra os potenciais-padrão de redução (E°) de algumas espécies.

Texto para a questão.
Entre os elementos conhecidos, alguns são familiares a todos e outros são bastante raros. Algumas das substâncias elementares são metais e outras, não. À temperatura ambiente, alguns são gases, alguns, líquidos e outros, sólidos. Variam eles extremamente nas propriedades químicas e na natureza dos compostos que formam. Como consequência, estudar química não é simples nem fácil. Para se adquirir conhecimento razoável de química geral, é necessário aprender um grande número de fatos. Não existe uma teoria que unifique todos esses fatos completamente. Contudo, várias teorias foram desenvolvidas suficientemente para servir de ajuda ao estudante na tarefa de aprender algo sobre as propriedades e reações das substâncias, correlacionando informações empíricas com teorias, como, por exemplo, a lei periódica.
L. Pauling. Química Geral. Rio de Janeiro: Ao Livro
Técnico e Edusp, 1966 (com adaptações).
Texto para a questão.
Entre os elementos conhecidos, alguns são familiares a todos e outros são bastante raros. Algumas das substâncias elementares são metais e outras, não. À temperatura ambiente, alguns são gases, alguns, líquidos e outros, sólidos. Variam eles extremamente nas propriedades químicas e na natureza dos compostos que formam. Como consequência, estudar química não é simples nem fácil. Para se adquirir conhecimento razoável de química geral, é necessário aprender um grande número de fatos. Não existe uma teoria que unifique todos esses fatos completamente. Contudo, várias teorias foram desenvolvidas suficientemente para servir de ajuda ao estudante na tarefa de aprender algo sobre as propriedades e reações das substâncias, correlacionando informações empíricas com teorias, como, por exemplo, a lei periódica.
L. Pauling. Química Geral. Rio de Janeiro: Ao Livro
Técnico e Edusp, 1966 (com adaptações).
A bioquímica, por si só, representa uma área interdisciplinar, uma vez que possui como base as ciências químicas e biológicas. Atualmente, está em voga uma variedade de temas concernentes a essa área científica, como células-tronco, transgênicos, clonagem, biopirataria, entre outros, que exigem não apenas conhecimentos científicos, mas que envolvem aspectos sociais, políticos, econômicos e até religiosos. Em pesquisa realizada com professores de química, pesquisadores reportaram que a bioquímica aparece como um dos dez temas com os quais a química pode ser abordada socialmente. Logo, a bioquímica constitui-se em um nicho temático muito rico e promissor para abordagens interdisciplinares, contextualizadas social e experimentalmente. Tratando-se de uma interface da química, é fundamental que os professores dessa disciplina tenham uma formação acadêmica que garanta os conhecimentos necessários à condução de atividades didáticas abarcadas por temas bioquímicos.
W. Francisco e W. E. Francisco Junior. A bioquímica a partir de livros didáticos: um estudo dos livros de química aprovados pelo PNLEM 2007. XV Encontro Nacional de Ensino de Química (ENEQ), Brasília, 2010 (com adaptações).
Tendo o texto como referência inicial, assinale a alternativa
correta acerca das principais características das proteínas.