Questões de Concurso Para técnico de laboratório - química
Foram encontradas 3.210 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Foi requisitado a um técnico de laboratório que preparasse uma solução de hidróxido de amônio, a partir de uma solução comercial concentrada, cujo rótulo contém as informações ao lado:
Dados: MM(NH3) = 17g/mol
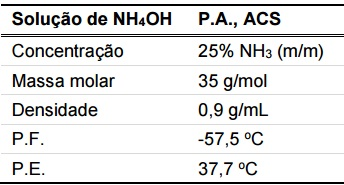
Assinale a alternativa que indica o volume aproximado da solução
comercial (em mL) que o técnico deve utilizar para obter 5 litros de
uma solução de NH4OH 1 mol/L.
O jeans com aspecto “desbotado” pode ser obtido pela oxidação parcial do índigo impregnado no tecido (denim), utilizando-se uma solução de KMnO4, como ilustrado pelo esquema reacional a seguir. Devido à formação de MnO2, sólido castanho insolúvel em água, um outro reagente deve ser usado para que ele não impregne o tecido.
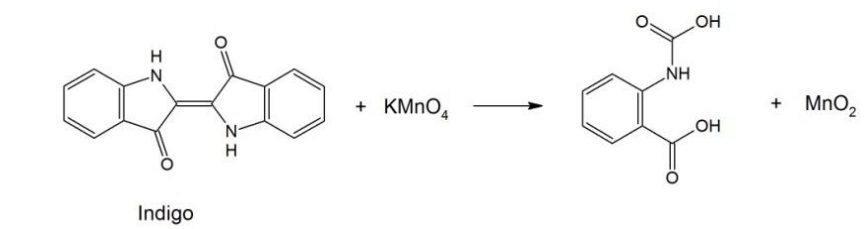
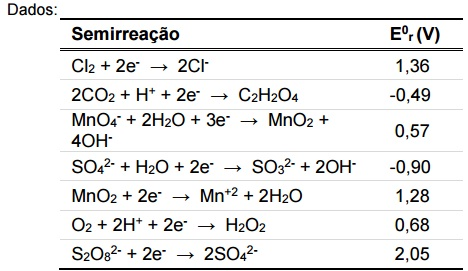
De acordo com os potenciais de redução fornecidos na tabela
ao lado, assinale a alternativa que apresenta substâncias que
podem ser usadas para transformar o MnO2 na espécie
solúvel Mn+2
.
Compostos fenólicos são utilizados como antioxidantes em alimentos, cosméticos e combustíveis, porém seu uso pode ser limitado pela solubilidade dessas substâncias nos produtos de aplicação. As estruturas de alguns antioxidantes fenólicos mais usados são mostradas ao lado:
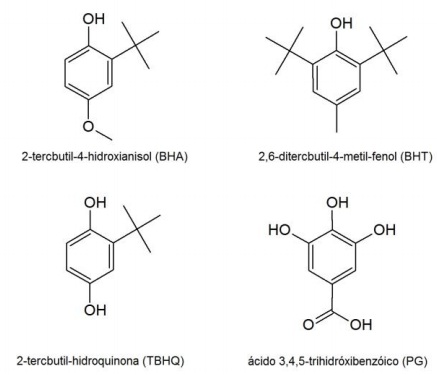
Em relação à polaridade das substâncias apresentadas,
assinale a alternativa que apresenta a ordem crescente de
solubilidade desses compostos em óleos vegetais
(triglicerídeos).
A queima de enxofre elementar gera compostos gasosos responsáveis pela formação da chuva ácida, com consequente deterioração de edificações e de monumentos construídos em mármore, acompanhada de liberação de gás carbônico na atmosfera. Esse processo pode ser ilustrado pelas seguintes reações não balanceadas:
S + O2 → SO2
SO2 + O2 → SO3
SO3 + H2O → H2SO4
H2SO4 + CaCO3 → CaSO4 + H2CO3
H2CO3 → CO2 + H2O
Considerando essa sequência de eventos, assinale a alternativa que apresenta a equação global balanceada dos eventos
supracitados.
O ácido etilenodiamino tetra-acético (EDTA) é usado como “sequestrante” em detergentes, impedindo a precipitação do surfactante (princípio ativo) pelos íons Ca+2, Mg+2 e Fe+3 presentes na água. Em análise química, o EDTA é utilizado como titulante para a determinação de dureza (Ca+2 , Mg+2) de águas, cujo sal dissódico é obtido pela seguinte reação:
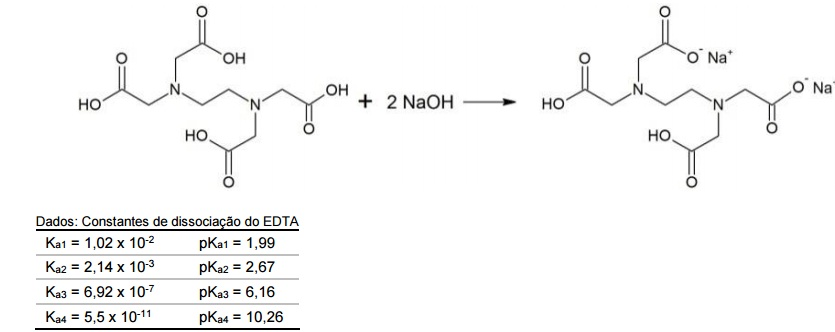
De acordo com a reação de neutralização parcial do EDTA acima apresentada, assinale a alternativa que apresenta o
intervalo de pH no qual é obtido apenas o sal dissódico.