Questões de Vestibular
Sobre calorimetria em física
Foram encontradas 375 questões
Considere duas garrafas idênticas, uma
contendo 1 kg de leite e outra contendo 1 kg de
água, ambas inicialmente a 15 °C e expostas à
temperatura ambiente de 21 °C. A capacidade
térmica do leite integral é, aproximadamente, 3,93
kJ·K-1
·kg-1 e da água é 4,19 kJ·K-1
·kg-1
. Considere
que a condutividade e a emissividade térmica sejam
as mesmas para os dois líquidos. Com base nessas
informações, é correto afirmar que, ao atingir o
equilíbrio térmico com o ambiente,
TEXTO 3
O acendedor de lampiões
Lá vem o acendedor de lampiões da rua!
Este mesmo que vem infatigavelmente,
Parodiar o sol e associar-se à lua
Quando a sombra da noite enegrece o poente!
Um, dois, três lampiões, acende e continua
Outros mais a acender imperturbavelmente,
À medida que a noite aos poucos se acentua
E a palidez da lua apenas se pressente.
Triste ironia atroz que o senso humano irrita: —
Ele que doura a noite e ilumina a cidade,
Talvez não tenha luz na choupana em que habita.
Tanta gente também nos outros insinua
Crenças, religiões, amor, felicidade,
Como este acendedor de lampiões da rua!
(LIMA, Jorge de. Melhores poemas. 3. ed. São Paulo: Global, 2006. p. 25)
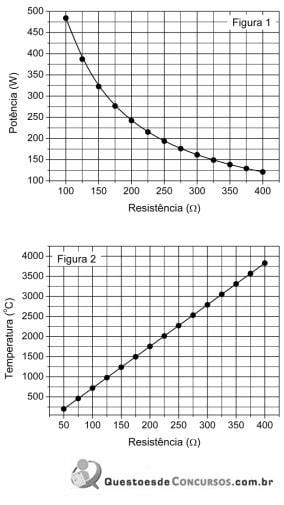
O Texto 3 cita o uso de lampiões na iluminação pública, técnica que foi substituída pela corrente elétrica, que também gera energia térmica. Considere um calorímetro (recipiente termicamente isolado) equipado com um aquecedor elétrico cuja resistência é percorrida por uma corrente de 5,1 A quando ligado a uma rede de 220 V. São colocados 1800 gramas de gelo a -10°C no calorímetro, que é ligado à tensão de 220 V. Considerando-se:
• que existe troca de energia apenas entre gelo, água e a resistência do aquecedor;
• que Tg = 0°C é o ponto de fusão da água;
• que Lg = 3,3 × 105 J/kg é o calor latente de fusão do gelo;
• que cg = 2,1 × 103 J/kg.K é o calor específico do gelo;
• e que ca = 4,2 × 103 J/kg.K é o calor específico da água.
Pode-se afirmar que, após 15 minutos de funcionamento, tem-se no interior do calorímetro (assinale a alternativa correta):
Admita duas amostras de substâncias distintas com a mesma capacidade térmica, ou seja, que sofrem a mesma variação de temperatura ao receberem a mesma quantidade de calor. A diferença entre suas massas é igual a 100 g, e a razão entre seus calores específicos é igual a 6/5.
A massa da amostra mais leve, em gramas, corresponde a:
Dados: dágua = 1,0 g/cm3 ; dgelo = 0,9 g/cm3 ;
calor latente de fusão do gelo = 80 cal/g;
calor específico da água = 1 cal/gºC e
pressão atmosférica = 1 atm.
(...) Quando pressionadas por uma resposta para
"Por que sentimos frio no inverno," muitas vezes as
pessoas respondem que é pelo fato de a Terra estar mais
distante do Sol no "inverno", recebendo assim menos luz e
tornando-se mais fria. Isso está errado. (...) Se
considerarmos que a variação da distância orbital entre a
Terra e o Sol, durante o ano, é de cerca de 5.000.000
quilômetros, o que é cerca de 800 vezes maior que o raio
da Terra, podemos ver que todas as regiões da Terra são
afetadas praticamente da mesma forma por esta
variação. Portanto, não é a causa de mudanças sazonais.
No entanto, o fato de as estações serem diferentes
entre os hemisférios sul e norte sugere que a inclinação do
eixo de rotação Terra é a razão para as estações do ano. E
isso é verdade. Uma vez que a inclinação da Terra
permanece constante, durante o inverno do hemisfério
norte, o hemisfério norte aponta para longe do Sol. Este
ângulo faz com que o Sol seja mais baixo no céu, aqueça o
solo de forma menos eficiente e reduza os dias, causando
o frio. Mas a resposta "inclinação da Terra" sempre me
pareceu um pouco superficial, já que ela não responde à
pergunta mais interessante: por que sentimos frio?
A resposta mais direta é que nós não sentimos o
frio. De fato, os seres humanos e outros animais não
sentem a temperatura das coisas. O que nós realmente
sentimos é o fluxo de calor causada por diferenças de
temperatura. Sentimos "a transferência de calor." Isso
não é uma distinção trivial. Tudo num forno aquecido está
à mesma temperatura, mas tocar uma forma de bolo
metálica causará mais dor que tocar o ar circundante,
porque a transferência de calor a partir da forma é rápida
e intensa, enquanto que a troca de calor com o ar é lenta
e pouco intensa. (...)
Traduzido de: http://www.michigandaily.com/opinion/11barry-
belmont-being-cold14 . Acesso em 25.07.14.
Considere: - o calor específico da água igual a 4,2J/g.ºC. - a densidade da água de 1 g/ml.
Um bloco de gelo a -30 °C repousa sobre uma
superfície de plástico com temperatura inicial de
21 °C. Considere que esses dois objetos estejam
isolados termicamente do ambiente, mas que haja
troca de energia térmica entre eles. Durante um
intervalo de tempo muito pequeno comparado ao
tempo necessário para que haja equilíbrio térmico
entre as duas partes, pode-se afirmar corretamente
que
O calor específico deste metal, em cal/g °C, vale:
O gráfico representa, aproximadamente, como varia a temperatura ambiente no período de um dia, em determinada época do ano, no deserto do Saara. Nessa região a maior parte da superfície do solo é coberta por areia e a umidade relativa do ar é baixíssima.
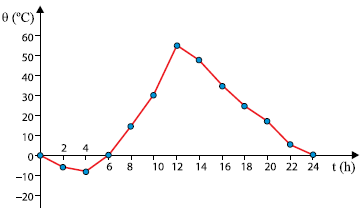
A grande amplitude térmica diária observada no gráfico pode, dentre outros fatores, ser explicada pelo fato de que
Para determinar o valor energético de um alimento, podemos queimar certa quantidade desse produto e, com o calor liberado, aquecer determinada massa de água. Em seguida, mede-se a variação de temperatura sofrida pela água depois que todo o produto foi queimado, e determina-se a quantidade de energia liberada na queima do alimento. Essa é a energia que tal alimento nos fornece se for ingerido.
No rótulo de um pacote de castanha-de-caju, está impressa a tabela a seguir, com informações nutricionais sobre o produto.
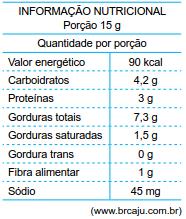
Considere que 150 g de castanha tenham sido queimados e que determinada massa m de água, submetida à chama dessa combustão, tenha sido aquecida de 15 ºC para 87 ºC. Sabendo que o calor específico da água líquida é igual a 1 cal/(g · ºC) e que apenas 60% da energia liberada na combustão tenha efetivamente sido utilizada para aquecer a água, é correto afirmar que a massa m, em gramas, de água aquecida era igual a