Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
Empregado em processos de cromação, o tríóxido de crômio, que é altamente tóxico, corrosivo e carcinogênico, é eventualmente utilizado para a produção de crômio, de acordo com a seguinte reação: 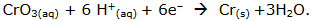
Considerando a reação acima, é correto dizer que a massa, em g, de crômio depositada por 24.125 C é,
aproximadamente


Tendo como referência essas informações, julgue o item seguinte.
Quando o cálcio-41 captura um elétron, é formado o
nuclídeo 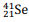 .
.


Tendo como referência essas informações, julgue o item seguinte.
A espécie formada pela ionização do átomo de cálcio possui
raio menor que o do átomo neutro de Ca.


Tendo como referência essas informações, julgue o item seguinte.
Os íons K+
e Cl−
são isótopos entre si.
Em um experimento realizado por Thomas Graham, dois gases A e B foram liberados simultaneamente nas extremidades de um tubo de vidro; esses gases difundiram-se em direção ao centro do tubo e, no instante em que se encontraram, formaram um anel de um composto AB, como mostra a figura a seguir.
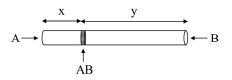
Para esses gases A e B, de massas molares MA e MB, respectivamente, verifica-se o seguinte postulado de Graham, em que vB representa a velocidade de difusão de B e vA, a velocidade de difusão de A.
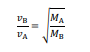
Tendo como referência essas informações e considerando que MA = 4MB, julgue o item.
Nas condições do experimento de Graham, em um tubo de
comprimento igual a 90 cm, o gás B percorrerá uma
distância y superior a 50 cm.
Em um experimento realizado por Thomas Graham, dois gases A e B foram liberados simultaneamente nas extremidades de um tubo de vidro; esses gases difundiram-se em direção ao centro do tubo e, no instante em que se encontraram, formaram um anel de um composto AB, como mostra a figura a seguir.

Para esses gases A e B, de massas molares MA e MB, respectivamente, verifica-se o seguinte postulado de Graham, em que vB representa a velocidade de difusão de B e vA, a velocidade de difusão de A.
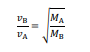
Tendo como referência essas informações e considerando que MA = 4MB, julgue o item.
Considere que o gás cloreto de hidrogênio (HCl) possa
ser obtido a partir dos gases hidrogênio (H2) e cloro (Cl2)
por meio da reação reversível H2(g) + Cl2(g) ⇌ 2 HCl(g) e que
um frasco fechado, a uma dada temperatura, contenha
esses três gases em equilíbrio, com 20% de H2 e 60% de
Cl2 em volume, a uma pressão total de 10 atm. Nessas
condições, a constante de equilíbrio, no que se refere à
pressão, é superior a 0,25.
A produção mundial de ácido cítrico é de aproximadamente 63,5 milhões de quilogramas por ano, sendo esse ácido orgânico produzido pela fermentação aeróbica da sacarose (C12H22O11) por uma cultura pura do fungo filamentoso Aspergillus niger, de acordo com a reação global representada a seguir.
C12H22O11 + 3 O2 → 2 C6H8O7 + 3 H2O
Considerando as informações anteriores, julgue o item.
Para produzir 63,5 milhões de quilogramas de ácido cítrico, a quantidade de sacarose necessária será
igual ou superior a 50 milhões de quilogramas e inferior
a 60 milhões de quilogramas.
A produção mundial de ácido cítrico é de aproximadamente 63,5 milhões de quilogramas por ano, sendo esse ácido orgânico produzido pela fermentação aeróbica da sacarose (C12H22O11) por uma cultura pura do fungo filamentoso Aspergillus niger, de acordo com a reação global representada a seguir.
C12H22O11 + 3 O2 → 2 C6H8O7 + 3 H2O
Considerando as informações anteriores, julgue o item.
Sabendo que a reação em tela tem a sua velocidade
aumentada na presença da enzima invertase extracelular, é
correto inferir que essa enzima funciona como catalisador de
uma das etapas da fermentação da sacarose realizada pelo
Aspergillus niger.
A produção mundial de ácido cítrico é de aproximadamente 63,5 milhões de quilogramas por ano, sendo esse ácido orgânico produzido pela fermentação aeróbica da sacarose (C12H22O11) por uma cultura pura do fungo filamentoso Aspergillus niger, de acordo com a reação global representada a seguir.
C12H22O11 + 3 O2 → 2 C6H8O7 + 3 H2O
Considerando as informações anteriores, julgue o item.
Caso a reação em apreço seja reversível e esteja sujeita às
leis do equilíbrio químico, um ambiente anaeróbico
favoreceria a produção de ácido cítrico.
A produção mundial de ácido cítrico é de aproximadamente 63,5 milhões de quilogramas por ano, sendo esse ácido orgânico produzido pela fermentação aeróbica da sacarose (C12H22O11) por uma cultura pura do fungo filamentoso Aspergillus niger, de acordo com a reação global representada a seguir.
C12H22O11 + 3 O2 → 2 C6H8O7 + 3 H2O
Considerando as informações anteriores, julgue o item.
A reação apresentada é de oxirredução, em que o carbono
cede elétrons para o oxigênio.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
Considerando-se que, por ano, o Brasil exporta um milhão de toneladas de suco de laranja e importa 500.000 t de ácido cítrico, é correto afirmar que, se o ácido cítrico fosse obtido diretamente do suco de laranja em vez de ser exportado, o Brasil, mantida a atual demanda interna por ácido cítrico,
teria de importar entre 100.000 t e 400.000 t de ácido cítrico por ano.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
O ácido cítrico está envolvido em uma importante via
intracelular, o ciclo de Krebs, que ocorre nas cristas
mitocondriais e é formado pela reação entre coenzima A e
ácido oxaloacético.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
Quando o presidente da Embrapii diz que a glicose é
metade da molécula de sacarose, ele se refere ao fato de
que a molécula de sacarose é formada por duas moléculas
de glicose.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
Na presença de hidróxido de sódio, o ácido cítrico reage
produzindo um sabão.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
O ácido cítrico pode sofrer desidratação intramolecular.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
A concentração em quantidade de matéria de ácido cítrico no
suco de laranja é superior a 0,01 mol/L.
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
Em solução aquosa, o ácido cítrico sofre três reações de dissociação ácida, cujas equações químicas estão corretamente expressas a seguir.
C6H8O7(aq) + H2O(l) ⇌ C6H7O7 − (aq) + H3O+ (aq)
C6H7O7 − (aq) + H2O(l) ⇌ C6H6O7 2−(aq) + H3O+ (aq)
C6H6O7
2−(aq) + H2O(l) ⇌ C6H5O7
3−(aq) + H3O+
(aq)
Com base no texto anterior e nas informações precedentes e considerando que 1 L = 1 dm3 , julgue o item.
A primeira constante de dissociação ácida do ácido cítrico
(Ka1) é superior a 10−3.