Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
O processo de obtenção do hidrogênio verde consiste na decomposição de moléculas de água em oxigênio e hidrogênio por meio da eletrólise, usando energias renováveis, conforme mostra a figura a seguir.
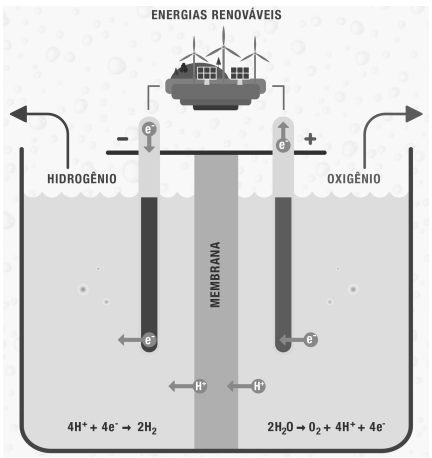
Adaptado de https://www.iberdrola.com/sustentabilidade/hidrogenio-verde.
Com base no processo eletrolítico apresentado na figura, assinale a alternativa correta.
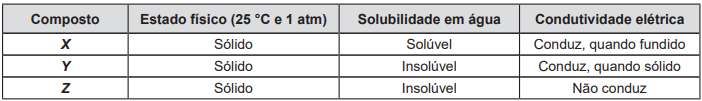
Com base no quadro, a natureza da ligação química mais provável para os compostos X, Y e Z é, respectivamente, _________, _________ e _________.
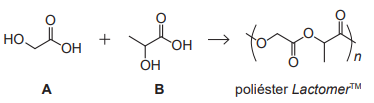
Sobre as estruturas químicas dos compostos A e B, afirma-se:
I. O composto A apresenta quatro ligações sigma, uma ligação pi e os grupos funcionais álcool e ácido carboxílico. II. O composto A apresenta oito ligações sigma, uma ligação pi e os grupos funcionais álcool e ácido carboxílico. III. O composto B apresenta cinco ligações sigma, uma ligação pi e os grupos funcionais álcool e cetona. IV. O composto B apresenta onze ligações sigma, uma ligação pi e os grupos funcionais álcool e ácido carboxílico.
Estão corretas apenas as afirmativas
As empresas farmacêuticas utilizam diferentes tecnologias para permitir a liberação controlada. Em alguns casos, por exemplo, o medicamento possui um revestimento que se dissolve depois de um período para liberar as partículas de fármaco. O revestimento tem por objetivo controlar a velocidade da reação e liberar uniformemente o fármaco no organismo.
Considerando o texto apresentado, assinale V (verdadeiro) ou F (falso) para as afirmações a seguir.
( ) Um fármaco constituído de partículas menores é absorvido mais lentamente pelo organismo do que outro com partículas maiores. ( ) A área superficial em um medicamento sólido na forma de pó é maior do que a área superficial em um medicamento na forma de comprimido. ( ) Quanto maior a espessura do revestimento do fármaco, maior o tempo para o fármaco ser absorvido pelo organismo.
O correto preenchimento dos parênteses, de cima para baixo, é
CH4(g) + 3 Cl2(g) → CHCl3(l) + 3 HCl(g)
A quantidade de cloro, em gramas, necessária para produzir 1,5 mol de clorofórmio é
Soneto da Família Nobre. Autor desconhecido. http://www.quimica.ufc.br/?q=node/126.
Neste trecho de Soneto da Família Nobre, é possível ser identificada uma propriedade do elemento químico carbono. Trata-se de
https://www.todini.com/br/produtos-quimicos/outros/acido-malonico
Substituindo cada um dos grupos carboxílicos, no exemplo dado acima, por um grupo hidroxila, obtém-se um novo composto, conhecido como
O ponto de ebulição representa a temperatura em que uma substância atinge e muda do estado líquido para o estado gasoso. Variáveis, tais como pressão atmosférica, altitude, composição e massa da substância influenciam no processo de mudança de estado físico.
Para responder à questão, você deve considerar as variáveis destacadas no texto I e o fato de uma pessoa preparar seu café, somente, quando a água atinge a temperatura de ebulição.
TEXTO II
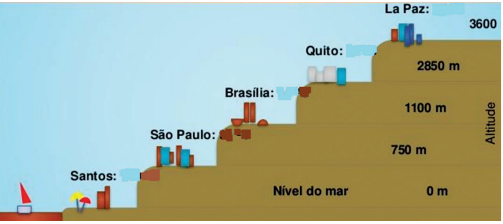
Considerando os textos I e II, analise a seguinte situação.
Uma pessoa que mora em Santos mudou-se recentemente para a cidade de La Paz – Peru. Ela decidiu medir o tempo que gasta para passar a mesma quantidade de café quando morava em Santos, usando a mesma quantidade de calor.
Nessa situação, o tempo gasto para passar o café será
A variedade alotrópica do S ocorre quando são apresentadas substâncias de

Considere o comportamento dos gases hidrogênio e cloro, respectivamente, em seus balões, nas mesmas condições de temperatura e de pressão.
As informações da imagem retratam o princípio que corresponde à lei de
A energia gerada pela fonte, acima tratada, é oriunda de uma reação de
A utilização do etanol como substituto da gasolina tem como efeito uma redução de emissões líquidas de CO2. Considerando os dados de Macedo e colaboradores (2004), o que causa o maior impacto na emissão de gases de efeito estufa é a quantidade de gasolina evitada por causa do uso de etanol.
A queima de etanol, na câmara de combustão, se dá a partir da reação completa de 1 mol do álcool com 3 mols de oxigênio gasoso, mediante a seguinte equação química:
C2H5OH + 3 O2 → 2 CO2 + 3 H2O, ΔH° = -1366,1 kJ/mol
https://www.novacana.com/sustentabilidade/demanda-terras-aumento-producao-etanol-acucar.(Adaptado).
A variação da entalpia, em função do caminho da reação para a transformação química que ocorre com o etanol na câmara de combustão, é representada no seguinte gráfico:
https://www.todamateria.com.br/tabela-periodica. Acessado em 12/10/2020.
Considerando os metais alcalinos terrosos (grupo 2 A da Tabela Periódica), é possível afirmar que seus elétrons da camada de valência estão
Referência Bibliográfica: https://www.minhavida.com.br/saude/temas/azia. (adaptado).
Os produtos finais gerados a partir da interação entre o bicarbonato de sódio e o HCl estomacal são componentes inorgânicos, quantitativamente identificados pelas seguintes funções inorgânicas:
Texto base para a questão.
A Tiquira é um destilado de mandioca muito popular no Maranhão. Alguns consideram a Tiquira a verdadeira aguardente brasileira por ser feita da mandioca, uma planta nativa.
A aguardente tiquira – destilado produzido a partir do mosto fermentado de mandioca, originalmente incolor, adquire uma cor azulada, em razão da adição de folhas ou de flores de tangerina durante o processo de destilação. A obtenção do álcool, no processo de fermentação, ocorre conforme a reação química a seguir:
C6H12O6 → CO2 + CH3CH2OH
glicose etanol
Alguns produtores informais adicionam um corante chamado violeta de metila, conforme estrutura representada a seguir, que garante um vívido azul-arroxeado à bebida. Na Química, essa substância, é utilizada como um indicador para o intervalo de pH com valores de 0 a 1,6, quando apresenta uma coloração amarelada.
Considere os seguintes dados: C = 12 g.mol -1, H = 1 g.mol -1 e O = 16 g.mol -1.
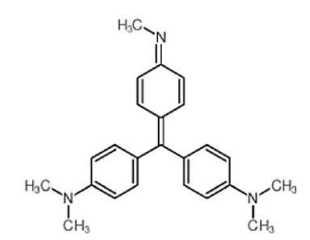
Estrutura química do indicador violeta de metila