Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
Fe(s) + 2 HCl(aq) → FeCl2(aq) + H2(g)
Então, na temperatura de 25 ºC e pressão de 1 atm, o volume de gás hidrogênio, considerado gás ideal, para inflar o balão foi de aproximadamente:
Dados:
Massas Molares (g.mol-1): H = 1,0; Cl = 35,5 e Fe = 56,0; R = 0,082 L.atm.K-1.mol-1 (Constante Universal dos Gases); T (K) = T(ºC) + 273.
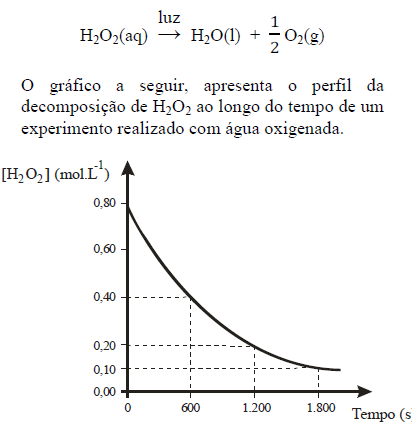
Considerando a reação química e o gráfico apresentados, e ainda que o tempo inicial é igual a zero, é correto afirmar que:
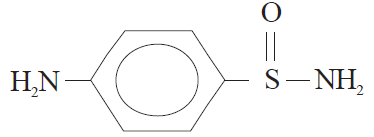
Algumas sulfonamidas podem ser potencialmente carcinogênicas e ainda podem causar efeitos colaterais, como reações alérgicas ou tóxicas em algumas pessoas.
Analisando-se os grupos funcionais presentes na p-amino benzeno sulfonamida, pode-se dizer que está presente a função:
Concentração de ácido acético: 6,0% m/V
Ao explicar que o vinagre é uma solução aquosa de ácido acético (ácido etanóico), o professor deixou o seguinte questionamento valendo um ponto na média: “Qual o pH do vinagre?” As seguintes informações foram fornecidas pelo professor:
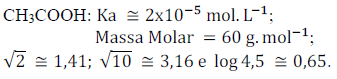
Assim, ganhará o ponto o aluno que responder que o pH é aproximadamente:
A figura a seguir, ilustra um esquema do processo eletroquímico que ocorre nas baterias de íons de lítio.

Sobre tais reações, pode-se dizer que:
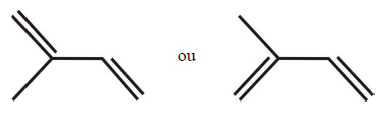
A respeito dessa molécula, é correto afirmar que:
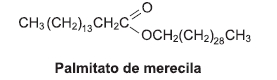
O material estrutural utilizado pelas abelhas na construção da colmeia e dos favos de mel, rico em glicídios, é o palmitato de merecila, representado pela fórmula estrutural, um dos principais constituintes da cera de abelhas.
A partir dessas informações, é correto afirmar:
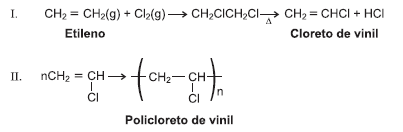
A tecnologia de “concreto de PVC” é uma forma de construção que utiliza placas leves e modulares de policloreto de vinil, de simples encaixe, preenchidas com concreto e aço. A estrutura tem alta resistência e garantia de trinta anos sem descolorir. As vantagens apontadas pelos fabricantes são a imunidade a cupins e a fungos, a facilidade de limpeza com água e sabão e o isolamento acústico e térmico. A principal desvantagem é o custo 20% mais caro que as construções convencionais.
Considerando-se as equações químicas I e II, as informações do texto, a origem da matéria-prima usada na produção de PVC e as consequências da utilização na construção civil, é correto afirmar:
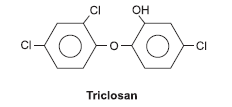
O triclosan, representado pela fórmula estrutural, é um inibidor da ação de micro-organismos, utilizado nos desodorantes e nos cremes dentais para impedir a proliferação de placas de bactérias.
A partir dessas considerações e da estrutura da molécula de triclosan, é correto afirmar:
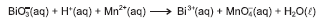
No balanceamento das equações de oxirredução, o fundamental é identificar o número de elétrons recebidos e cedidos, o número total de átomos de cada elemento químico no primeiro e segundo membros da equação química, além do total de carga elétrica em cada um de seus membros. Assim, com base nessas considerações, e a partir do balanceamento da equação química com os menores coeficientes estequiométricos inteiros, é correto afirmar:
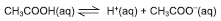
Dos sistemas em equilíbrio químico iônico em solução aquosa, um dos mais importantes é o que ocorre na ionização de ácidos e de bases, como o representado pela equação química, em que o ácido acético, em solução aquosa 0,1 mol.L–1, está 1,0% ionizado, à determinada temperatura.
Considerando-se essas informações, é correto afirmar:
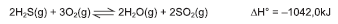
O deslocamento do equilíbrio químico de um sistema é toda e qualquer alteração de velocidade de reação direta ou inversa, que provoca modificações nas concentrações de substâncias químicas e, consequentemente, leva a um novo estado de equilíbrio.
A aplicação desse conceito de deslocamento de equilíbrio químico ao sistema representado pela equação química permite corretamente afirmar:
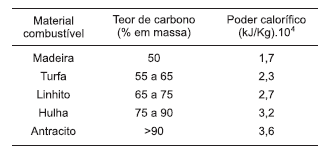
O carvão mineral é o mais abundante combustível fóssil existente na natureza. Ele é utilizado como fonte de energia desde a antiguidade e sua comercialização vem desde o Império Romano. A origem desse mineral remonta há cerca de 300 milhões de anos, no período Carbonífero, quando grande quantidade de biomassa, coberta por águas estagnadas, foi transformada em turfa, e, em seguida, em carvão. A hulha é um dos materiais carboníferos de grande importância econômica porque é uma fonte de hidrocarbonetos aromáticos, de gases combustíveis e de coque, resíduo utilizado em siderúrgicas. No Brasil, em Charqueadas, município do Rio Grande do Sul, encontra-se uma das minas de subsolo do Estado com 90% das reservas de carvão mineral do país.
A partir das informações do texto, da tabela que representa o teor de carbono de algumas espécies carboníferas e dos dados da tabela, é correto afirmar:
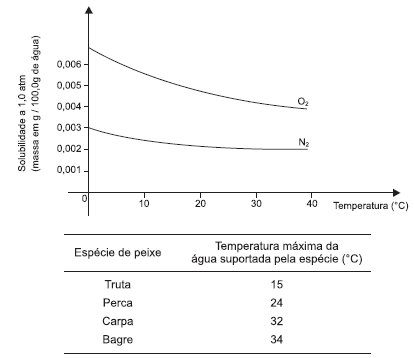
Os gases, de um modo geral, são pouco solúveis em líquidos, embora sua solubilidade dependa consideravelmente da pressão e da temperatura. A vida de animais aquáticos, como algumas espécies de peixe mostrados na tabela, pode ser facilmente afetada por variações de temperatura.
Dessa forma, admitindo-se que a variação de densidade da solução de oxigênio em água é desprezível, a análise do gráfico que representa a curva de solubilidade do oxigênio gasoso em água, em função da temperatura, e das informações da tabela e do texto, permitem corretamente afirmar:
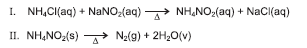
As bolinhas de tênis são feitas basicamente de borracha. Na primeira etapa de fabricação, a borracha é prensada em moldes de ferro e ganha forma de uma concha. Antes de as duas metades da bolinha serem coladas, coloca-se, no interior de uma delas, nitrito de amônia, que é obtido de acordo com a equação química I. Na etapa seguinte, as duas conchas são unidas por cola especial e, em seguida, prensadas a 200° C. Com o aquecimento, durante o processo de colagem, o nitrito de amônia se decompõe, de acordo com a equação química II, em nitrogênio, que exerce pressão no interior da bolinha. Admitindo-se que o volume da bolinha de tênis, a 25° C, é 140,0mL, que o volume de água produzido no seu interior é desprezível, é correto, a partir das informações do texto e das equações químicas I e II , afirmar:
Assim, considerando-se que um recipiente de vidro aberto, inicialmente, contendo ar a 27°C, é aquecido a 127°C e mantido a essa temperatura, no ambiente em que está, pode-se corretamente afirmar:
A partir do conhecimento dessas relações, é correto afirmar

Durante a destilação fracionada de uma mistura de etanol e de propanona, foram coletadas duas amostras codificadas aleatoriamente como BD e AD, para determinação da temperatura de ebulição, utilizando-se de termômetro, tubo capilar e banho-maria com água. Os resultados encontrados na determinação dessas amostras foram, respectivamente, 59,5° C e 69,0° C.
A partir da análise dessas informações, é correto afirmar:
I - A velocidade de reação varia linearmente com a concentração do reagente. II - A velocidade instantânea é uma função exponencial do tempo. III - A meia-vida do reagente depende da sua concentração inicial.
Quais estão corretas?