Questões de Vestibular Sobre química
Foram encontradas 6.520 questões
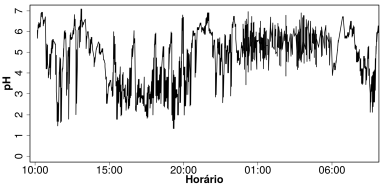
Dados: O pH normal no esôfago mantém-se em torno de 4 e o pH da saliva entre 6,8-7,2.
Assim, episódios de refluxo gastroesofágico acontecem quando o valor de pH medido é

Com base nas informações fornecidas, qual dos sais indicados a seguir é o mais eficiente como solução neutralizante?
Os grandes protagonistas na Copa do Mundo de Futebol na Rússia em 2018 foram os polímeros, e não os jogadores. Os polímeros estavam presentes nos uniformes dos jogadores e na bola. O polímero que merece destaque é o poliuretano, utilizado para a impressão térmica dos nomes, números e logos nos uniformes, além de ser utilizado como couro sintético das bolas utilizadas na competição. O poliuretano é obtido a partir da reação entre um isocianato e um poliol, conforme o esquema a seguir:
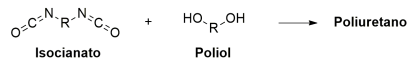
A estrutura química da unidade de repetição desse polímero é:
O níquel é empregado na indústria como catalisador de diversas reações, como na reação de reforma do etileno glicol, que produz hidrogênio a ser utilizado como combustível. O processo ocorre num tempo muito menor quando é utilizado 1 g de níquel em uma forma porosa desse material, em comparação à reação utilizando uma única peça cúbica de 1 g de níquel. Abaixo está esquematizada a equação de reforma do etileno glicol e ao lado uma imagem de microscopia eletrônica de uma amostra de níquel na forma porosa.
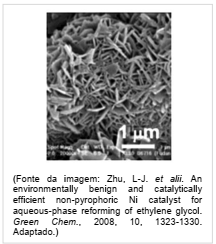
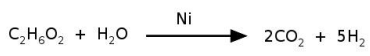
Nas condições mencionadas, a reação de reforma ocorre num tempo menor
quando usado o níquel poroso porque:
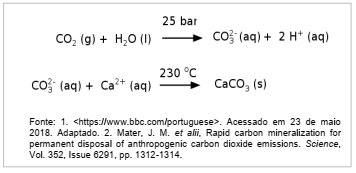
A usina de energia de Hellisheidi, na Islândia, vem testando um novo método para combater o aquecimento global: transformar o gás carbônico (CO2) em pedra. O processo ocorre em duas etapas: primeiro o CO2 é dissolvido em água em altas pressões (25 bar) e depois injetado no solo numa temperatura de 230 °C. A mineralização do gás carbônico ocorre de maneira rápida, devido à reatividade e composição do solo da região, rica em ferro, cálcio e magnésio. As duas etapas da remoção de CO2 estão esquematizadas de maneira simplificada ao lado.
A remoção desse gás da atmosfera ocorre por:
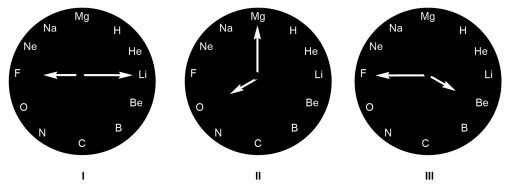
As substâncias neutras formadas a partir da leitura das horas marcadas nos relógios I, II e III são, respectivamente:
Duas soluções nomeadas X e Y foram preparadas a 25 ºC com as características dadas na tabela a seguir:
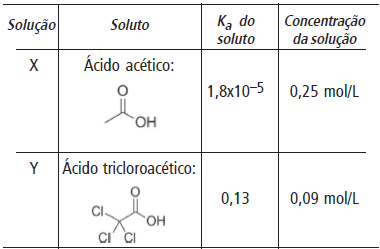
Considerando as informações fornecidas, analise os itens I a III.
I) A solução Y apresenta pH mais baixo que a solução X.
II) O ácido acético é mais fraco que o ácido tricloroacético.
III) A solução Y apresentará maior condutibilidade elétrica que a X.
Estão corretos os itens:
A figura a seguir mostra o diagrama de energia da reação A+B→C, ocorrendo via caminho 1 (linha sólida) ou 2 (pontilhado).
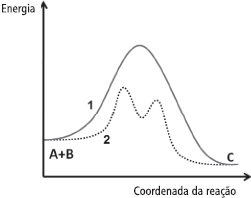
Com base no diagrama, analise os itens a seguir:
I) Existe a formação de um intermediário de reação no caminho 2.
II) Apenas um estado de transição (complexo ativado) está presente no caminho 1.
III) A reação deve se processar mais rapidamente, se ocorrer pelo caminho 1.
IV) O caminho 2 pode representar a reação A+B→C,na presença de um catalisador.
Estão corretos os itens:
Dois grandes grupos de substâncias compõem as células, as substâncias orgânicas e as inorgânicas, sendo as inorgânicas representadas pela água e pelos sais minerais. Os sais minerais atuam no corpo humano na contração muscular, coagulação sanguínea, síntese de proteínas etc. Entre os elementos que são importantes nos sais minerais, podemos citar, 20Ca, 11Na, 12Mg, 26Fe, 30Zn, 24Cr e 25Mn.
Considerando os elementos acima, assinale a alternativa correta.
Recentemente, o projeto de Lei 6.299 agregou várias propostas que tramitavam no Congresso, dentre elas alterar o nome dos agrotóxicos para “defensivos agrícolas” e “produtos fitossanitários”. Um dos agrotóxicos mais utilizados no Brasil hoje é o Glifosato®, porém é proibido nos Estados Unidos e na maioria dos países da Europa.
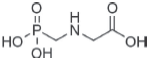
Sobre a estrutura química do Glifosato®, são feitas as afirmações abaixo:
I) A estrutura da molécula apresenta um carbono quiral, portanto pode existir numa mistura de enantiômeros R e S.
II) A molécula é um triéster de fosfato, que pode ser hidrolisada em pH neutro em presença de água.
III) Pode-se observar as funções amina e ácido carboxílico, podendo classificar a molécula como um aminoácido não natural.
IV) A molécula possui um átomo de Carbono com hibridização sp2, que pode participar da conjugação do carboxilato, quando este estiver desprotonado em meio básico.
Estão corretas apenas:
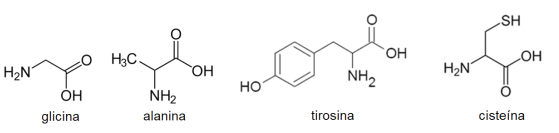
Abaixo estão apresentados alguns aminoácidos, entre eles apenas um não possui carbono quiral. Identifique-o.
A cloroquina, representada na figura abaixo, pesquisada durante a Segunda Guerra Mundial, foi de grande importância no tratamento da malária, sendo muito usada na década de 80 e considerada por mais de 40 anos como um medicamento benéfico e eficaz, bem tolerado pela maioria dos pacientes. No entanto, nas últimas décadas os parasitos da malária resistentes a esse composto difundiram-se reduzindo sua eficácia.
http://www.rbfarma.org.br/files/pag_49a55_farmacos_antimalariais.pdf . Acesso em 02/04/2018.
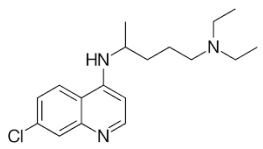
Estão presentes na cloroquina quantos carbonos primários e secundários, respectivamente?
HABER-BOSCH: O PROCESSO RESPONSÁVEL POR ALIMENTAR
MUITA GENTE NESTE PLANETA
Estima-se que aproximadamente 45% da população mundial só estão aqui em função do desenvolvimento do processo Haber-Bosch e da produção de amônia. Sem os fertilizantes nitrogenados, nós não teríamos condições de produzir a quantidade de alimentos necessária para alimentar a população que temos hoje no mundo, que está em torno de 7,3 bilhões de pessoas, com tendência a chegar a 9 ou 10 bilhões por volta de 2050. O processo Haber-Bosh descreve uma técnica para obtenção da amônia a partir do nitrogênio do ar atmosférico e do hidrogênio e de fatores como altas temperaturas e pressão.
Disponível em:<https://www.acontecenoticias.com.br/single-post/2017/09/27/Haber-Bosch-O-Processo-Respons%C3%A1velpor-Alimentar-Muita-Gente-Neste-Planeta> . Acesso em: 01/04/18.
A equação não balanceada que descreve a reação de produção de amônia é mostrada a seguir:
N2(g) +H2(g) ⇌ NH3(g)
Ao reagir 50 mols de N2 e 30 mols de H2, qual a quantidade de NH3 produzida em gramas se a reação de síntese for completa?
Dados: N=14 g/mol; H=1g/mol
As transformações químicas ocorrem todo o tempo ao nosso redor,por exemplo, é muito comum notarmos que materiais metálicos como cercas, portões, pregos, entre outros, ao ficarem expostos ao ambiente, acabam se deteriorando. Isso ocorre devido ao contato do elemento químico ferro (Fe) com átomos de oxigênio (O) presentes no ar atmosférico e na água. Podemos notar também que em regiões litorâneas esses materiais sofrem ainda mais danos devido à presença de sais e uma maior umidade. Esse fenômeno é conhecido como ferrugem e ocorre devido a uma reação de oxirredução.
Disponível em:<https://www.infoescola.com/quimica/ferrugem/>. Acesso em: 01/04/2018.
A equação global que representa a formação de ferrugem é descrita abaixo:
2Fe(s) + O2(g) + 2H2O(l) → 2Fe(OH)2(s)
De acordo com a equação química, podemos concluir que:
A dipirona (C13H16N3O4SNa) é um medicamento muito utilizado para aliviar a dor e para baixar a febre. Ana ao observar que seu filho João de 3 anos estava com febre, por indicação médica, diluiu 10 gotas do medicamento de concentração 500 mg/mL em água e deu ao seu filho. Qual a quantidade de moléculas de dipirona ingeridas por João?
Dados: 1mL = 20 gotas; Constante de Avogrado = 6x1023 moléculas/mol C=12g/mol; O=16g/mol; N=14g/mol; S=32g/mol; H=1g/mol; Na=23g/mol.
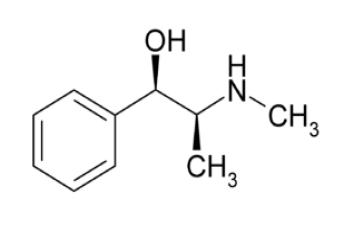 Com relação a essa molécula, podemos afirmar,
respectivamente, que sua fórmula molecular e os grupos
funcionais presentes correspondem às funções orgânicas:
Com relação a essa molécula, podemos afirmar,
respectivamente, que sua fórmula molecular e os grupos
funcionais presentes correspondem às funções orgânicas: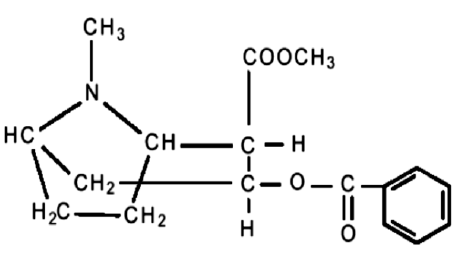 Na estrutura da cocaína apresentada acima, estão
presentes os grupos funcionais:
Na estrutura da cocaína apresentada acima, estão
presentes os grupos funcionais: 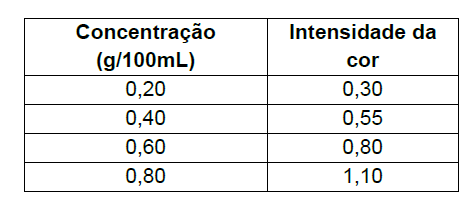
Qual é a concentração, em gramas por litro, de uma solução de glicose que, após a reação, apresenta intensidade de cor igual a 0,80?