Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
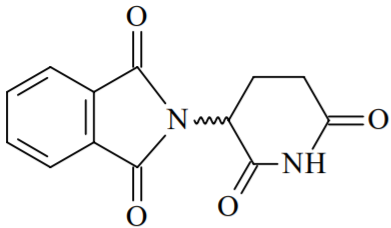
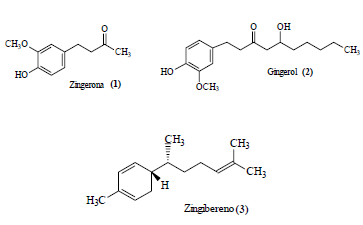
Uma mistura equivalente de seus isômeros S e R é descrita como uma mistura racêmica.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
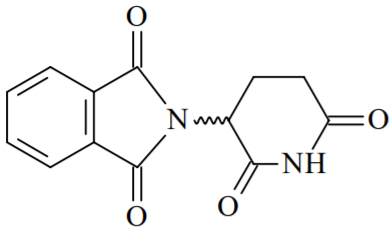
Possui duas aminas secundárias.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.

Possui um único centro quiral e apresenta dois isômeros oticamente ativos.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.

Os três anéis são aromáticos.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
O átomo de carbono possui 2 elétrons desemparelhados em um orbital do tipo p.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Um íon de carga 2+ que apresenta a distribuição eletrônica 1s2 2s2 2p6 3s2 3p4 possui 18 prótons em seu núcleo.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Ernest Rutherford, em seu modelo atômico, descrevia o átomo como uma estrutura na qual a carga positiva permanecia no centro, constituindo o núcleo, enquanto as cargas negativas giravam em torno desse núcleo.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Joseph J. Thomson, em seu modelo atômico, descrevia o átomo como uma massa de carga positiva que contém elétrons de carga negativa incrustados no seu interior que neutralizavam a massa positiva.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
De acordo com o modelo atômico de Dalton, o elétron é uma partícula maciça e indivisível.
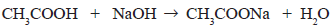
- até 200 mg/dL, DESEJÁVEL; - de 201 a 239 mg/dL, ACEITÁVEL; - a partir de 240 mg/dL, AUMENTADO.
Na análise laboratorial de uma amostra de sangue, foi determinado 2,1 g L-1 de colesterol, cuja fórmula molecular é C27H46O. Quantos mols de colesterol estão presentes aproximadamente e como está o nível de colesterol nessa amostra em relação aos valores tabelados acima?
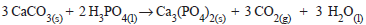
Analisando os processos (1) e (2) abaixo (no estado padrão),
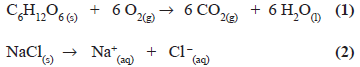
Pode-se dizer que
I. A reação que ocorre pelo caminho A é mais lenta, sem catalisador e com energia de ativação (Ea ) maior. II. A reação que ocorre pelo caminho B é mais rápida, com catalisador, sendo as energias de ativação das duas etapas (Ea1 e Ea2) menores. III.As reações que ocorrem pelo caminho A e B possuem a variação de entalpia (ΔH) > 0, portanto são endotérmicas. IV.As reações que ocorrem pelo caminho A e B possuem a variação de entalpia ( ΔH) < 0, portanto são exotérmicas. V. As reações que ocorrem pelo caminho A e B possuem velocidades iguais, pois o produto final tem a mesma energia.
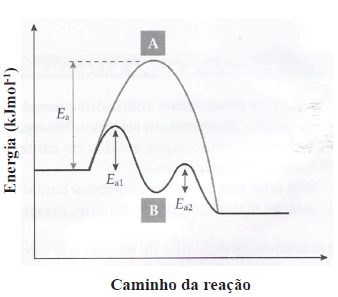
Marque a opção correta
I – pH = 5,4 II – pOH = 10 III – pOH = 8,5
Considerando a faixa de pH permitida, qual(is) a(s) indústria(s) que pode(m) lançar seu efluente nos corpos de água sem tratamento preliminar?
 (clonazepam) é um dos medicamentos
controlados mais consumidos no Brasil. Possui
propriedades farmacológicas comuns aos
benzodiazepínicos, sendo utilizado como ansiolítico
geral, sedativo, em transtornos de humor, entre
outros. Com relação à sua estrutura química, podese afirmar o seguinte:
(clonazepam) é um dos medicamentos
controlados mais consumidos no Brasil. Possui
propriedades farmacológicas comuns aos
benzodiazepínicos, sendo utilizado como ansiolítico
geral, sedativo, em transtornos de humor, entre
outros. Com relação à sua estrutura química, podese afirmar o seguinte: 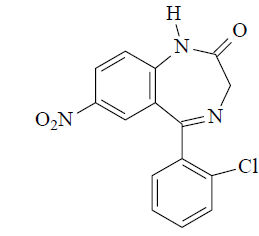
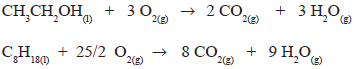
Considerando um tanque de combustível de 55 L, em que o automóvel A foi abastecido com álcool e o automóvel B com gasolina, qual o volume aproximado em L de gás carbônico, nas condições normais de temperatura e pressão, que será emitido pelos automóveis, respectivamente?
Considerar: - Volume molar dos gases nas CNTP, Vm= 22,7 L - densidade do etanol = 0,8 g.mL-1 - densidade do iso-octano = 0,7 g.mL-1
I. os compostos orgânicos 1, 2, 3 e 4 são polares e pertencem às funções químicas aldeído, éter, álcool e ácido carboxílico, respectivamente. II. os compostos 1 e 2 possuem ponto de ebulição (pe) menores que dos compostos 3 e 4, devido a apresentarem forças intermoleculares dipolodipolo. III.o composto 4 apresenta maior ponto de ebulição, devido, principalmente, às pontes de hidrogênio presentes e maior massa molecular. IV.a diferença entre o ponto de ebulição dos compostos 1 e 2 deve-se, principalmente, à massa molecular, visto serem compostos polares com a força intermolecular pontes de hidrogênio.
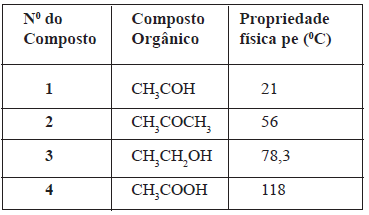
Marque a opção correta.