Questões de Vestibular
Sobre química orgânica em química
Foram encontradas 1.621 questões
Disponível em:<http:// www1.folha.uol.com.br/cotidiano/2015/08/1671619-quase-13-das-criancas-com menos-de 2-anos-bebem-refrigerante-aponta-ibge.shtml> . Acesso em: 20 ago. 15. (Adaptado.)
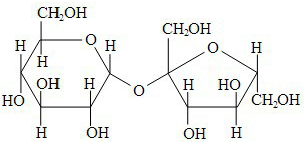
Em relação à sacarose, considere as proposições abaixo.
I É um açúcar redutor, de fórmula molecular C12H22O11, que não pode ser hidrolisado por soluções ácidas diluídas.
II É solúvel em água, devido ao rompimento da ligação entre as unidades de glicose e frutose.
III É um dissacarídeo, de caráter polar, e que apresenta na sua estrutura apenas átomos de carbono hibridizados na forma sp3 .
Das proposições acima,
Disponível em:<http://aspiraçoesquimicas.net/2014/08/feromonios-e-a-quimica-das-abelhas.html/> . Acesso em: 20 ago. 15. (Adaptado.)
Em relação às substâncias orgânicas mencionadas acima, assinale a alternativa correta.
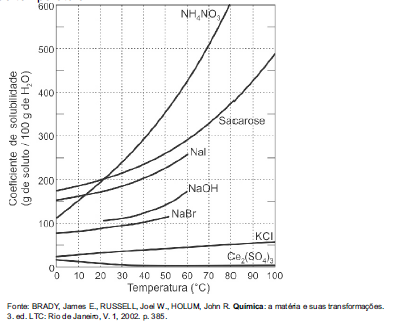
Considerando as informações apresentadas pelo gráfico acima, assinale a alternativa correta.
TEXTO 7
Memórias de um pesquisador
Não era bem vida, era uma modorra – mas de qualquer modo suportável e até agradável. Terminou bruscamente, porém, eu estando com vinte e oito anos e um pequeno bujão de gás explodindo mesmo à minha frente, no laboratório de eletrônica em que trabalhava, como auxiliar. Me levaram às pressas para o hospital, os médicos duvidando que eu escapasse. Escapei, mas não sem danos. Perdi todos os dedos da mão esquerda e três (sobraram o polegar e o mínimo) da direita. Além disso fiquei com o rosto seriamente queimado. Eu já não era bonito antes, mas o resultado final – mesmo depois das operações plásticas – não era agradável de se olhar. Deus, não era nada agradável.
No entanto, nos primeiros meses após o acidente eu não via motivos para estar triste. Aposentei-me com um bom salário. Minha velha tia, com quem eu morava, desvelava-se em cuidados. Preparava os pastéis de que eu mais gostava, cortava-os em pedacinhos que introduzia em minha boca – derramando sentidas lágrimas cuja razão, francamente, eu não percebia. Deves chorar por meu pai – eu dizia – que está morto, por minha mãe que está morta, por meu irmão mais velho que está morto; mas choras por mim. Por quê? Escapei com vida de uma explosão que teria liquidado qualquer um; não preciso mais trabalhar; cuidas de mim com desvelo; de que devo me queixar?
Cedo descobri. Ao visitar certa modista.
Esta senhora, uma viúva recatada mas ardente, me recebia todos os sábados, dia em que os filhos estavam fora. Quando me senti suficientemente forte telefonei explicando minha prolongada ausência e marcamos um encontro.
Ao me ver ficou, como era de se esperar, consternada. Vais te acostumar, eu disse, e propus irmos para a cama. Me amava, e concordou. Logo me deparei com uma dificuldade: o coto (assim eu chamava o que tinha me sobrado da mão esquerda) e a pinça (os dois dedos restantes da direita) não me forneciam o necessário apoio. O coto, particularmente, tinha uma certa tendência a resvalar pelo corpo coberto de suor da pobre mulher. Seus olhos se arregalavam; quanto mais apavorada ficava, mais suava e mais o coto escorregava.
Sou engenhoso. Trabalhando com técnicos e cientistas aprendi muita coisa, de modo que logo resolvi o problema: com uma tesoura, fiz duas incisões no colchão. Ali ancorei coto e pinça. Pude assim amá-la, e bem.
– Não aguentava mais – confessei, depois. – Seis meses no seco!
Não me respondeu. Chorava. – Vais me perdoar, Armando – disse – eu gosto de ti, eu te amo, mas não suporto te ver assim. Peço-te, amor, que não me procures mais.
– E quem vai me atender daqui por diante? – perguntei, ultrajado.
Mas ela já estava chorando de novo. Levantei-me e saí. Não foi nessa ocasião, contudo, que fiquei deprimido. Foi mais tarde; exatamente uma semana depois.
[...]
(SCLIAR, Moacyr. Melhores contos. Seleção de
Regina Zilbermann. São Paulo: Global, 2003. p.
176-177.)
O odor desagradável exalado junto com a transpiração deve-se a compostos malcheirosos produzidos a partir do metabolismo de microrganismos que utilizam o material liberado por glândulas presentes nas axilas, por exemplo. Um exemplo de substância responsável pelo mau cheiro é o ácido 3-metil-hex-2-enoico. O triclosan, um composto utilizado em desodorantes, inibe a atuação dos microrganismos e, com isso, previne o mau cheiro. Alguns desodorantes utilizam o bicarbonato de sódio, que neutraliza os compostos responsáveis pelo odor desagradável.
Sobre as informações apresentadas são feitas as seguintes afirmações:
I - O ácido 3-metil-hex-2-enoico é um composto orgânico ternário saturado, de fórmula molecular C6 H12O2 .
II - Na composição centesimal do ácido 3-metil-hex-2-enoico, observa-se que o oxigênio é o elemento que apresenta menor porcentagem em massa.
III - O bicarbonato de sódio, representado pela fórmula NaHCO3 , reage com ácido orgânico, formando sal de caráter alcalino.
IV - Sabendo-se que no triclosan existe uma hidroxila ligada em anel aromático, pode-se dizer que isso caracteriza a presença de função fenol no referido composto.
Assinale a alternativa que apresenta apenas itens corretos:
TEXTO 5
NA VIRADA DO SÉCULO, o biólogo Roosmarc conheceu o ápice da fama ao descobrir um novo gênero de primata: o sagui-anão-de-coroa-preta. Foi considerado pela revista Time o grande herói do planeta. Entre os mais de 500 primatas no mundo, Roosmarc descobrira o Callibella humilis, o macaquinho mais saltitante e alegre, anãozinho, com aquela coroa preta. Enquanto outros primatólogos matavam os animais para descrevê-los, dissecando-os em laboratórios, longe da Amazônia, ele criava macacos em sua casa. Esperava que morressem de forma natural e, aí sim, dissecava-os.
O sagui-anão-de-coroa-preta foi a sensação mundial. Então, ele viveu o ápice da glória. As publicações científicas não se cansaram de elogiá-lo. Quase todos os dias, jornais e revistas estampavam: “Protetor dos animais”, “O bandeirantes da Amazônia”, “O último primatólogo”. De Manaus para o mundo. Os ribeirinhos o saudavam; os políticos o pajeavam; os estudantes de biologia o veneravam. Sim, Roosmarc era visto e considerado como herói do planeta.
Vida simples, com suas vestes quase sempre largas cobrindo o corpo magro e alto, enfiado semanas na floresta, nunca quisera dinheiro, jamais almejara fortuna. O verdadeiro cientista, dizia, quer, antes de tudo, reconhecimento. Não havia prêmio maior do que isso. Sequer gastava o que ganhava. Aprendera com os bichos que, na vida, não se precisa de muitas coisas...
Nascera no sul da Holanda e, aos 17 anos, mudou-se para Amsterdã. Queria estudar biologia. Nos fins do ano 60, a cidade fervilhava, era a capital da contestação. John Lennon e Yoko Ono haviam escolhido a cidade para protestar contra a Guerra do Vietnã. Os rebeldes desfilavam pelas ruas, enquanto John Lennon e Yoko Ono incitavam a quebra de valores deitados uma semana num hotel da cidade, consumindo droga e criando suas canções. O gosto pela contracultura crescia, agigantava-se. Rebelde, Roosmarc desfilava pelas ruas, gritando pela paz, também queimando maconha e outras ervas.
Mas foi, nesta época, que ele se interessou pelos primatas. Depois que terminou a universidade, fez amizade com uma estudante, que também saboreava a contracultura, o desprezo a normas e procedimentos, e com ela, vivendo um romance apaixonado, deu volta ao mundo, como se fosse o famigerado navegante português Vasco da Gama. Estudante de artes plásticas, Marie tinha sede por aventuras: o novo lhe apetecia; o velho não era mais do que um mundo cinzento. A Europa, com seus prédios cinzentos e frios, uma população resignada, não lhe apetecia. Queria quebrar barreiras, outras fronteiras. Não queria apodrecer naquelas cidadezinhas holandesas, onde as mulheres envelheciam rapidamente e só cuidavam de casa. Não queria se transformar num símbolo de cama, fogão e igreja. Menosprezava o título “rainha do lar”, que os pastores tanto veneravam entre a população fiel. Tinha horror ao ver sua mãe de lenço na cabeça e avental cobrindo a gordura da barriga. Se ficasse numa daquelas cidadezinhas, em poucos anos estaria como a mãe – brigava constantemente com o seu pai, saía de casa aos domingos para assistir a mesmice do partor Simeão, e que, rapidamente, voltava para casa para preparar o almoço para os filhos. Que destino! A liberdade a chamava. Não era o que dizia a canção de John Lennon? Ao conhecer Roosmarc, o desejo por aventuras avivou como brasa viva. Quando convidada para segui-lo, e ela queria produzir desenhos e aquarelas jamais vistas no mundo, não titubeou, como se a oportunidade fosse um cavalo encilhado. E cavalo encilhado passa por nós somente uma vez ...
(GONÇALVES, David. Sangue verde. Joinville: Sucesso Pocket, 2014. p. 200-201.Adaptado.)
Beck, fino, banza, cano do diabo ou simplesmente baseado são exemplos de gírias usadas para designar um cigarro de maconha. Preparado de forma manual, um desses cigarros pode conter até um grama de maconha, quantidade suficiente para fazer muita fumaça. A maconha é produzida a partir da folha da Cannabis sativa. Como toda planta, ela é constituída de várias substâncias. Dentre elas, temos o canabidiol (C21H30O2 , de massa molar = 314,45g/mol), que pode chegar a quase 40% do extrato vegetal. O canabidiol apresenta baixa toxicidade em seres humanos e em outras espécies: a LD50 (quantidade de ingrediente ativo de uma substância tóxica necessária para matar 50% de animais testados) após a administração intravenosa em macacos foi de 212 mg/kg (SCUDERI et al., 2008).
(SCUDERI, Caterina et al. Cannabidiol in Medicine: a review of its therapeutic potential in CNS
Disorders. Phytotherapy research, n.23, p. 597-602. 9 Oct. 2008.)
Assinale a única alternativa correta com relação ao exposto anteriormente:
Para diferenciar os hidrocarbonetos etano e eteno em uma mistura gasosa, utiliza-se uma reação com bromo molecular: o etano não reage com esse composto, enquanto o eteno reage de acordo com a seguinte equação química:
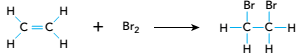
Considere um cilindro de capacidade igual a 10 L, contendo apenas esses hidrocarbonetos em uma mistura com massa igual a 200 g. Ao se adicionar bromo em excesso à mistura, todo o eteno reagiu, formando 940 g de 1,2-dibromoetano.
A concentração inicial de etano, em mol.L–1, no interior do cilindro, corresponde a:
O íon oxalacetato participa não só do ciclo de Krebs como também da produção do íon aspartato, segundo a equação abaixo:
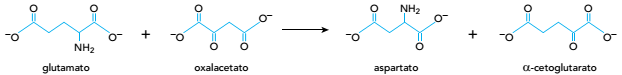
Com base nessa reação, pode-se afirmar que o aspartato é o ânion correspondente ao ácido
dicarboxílico denominado:

 . Assim, no esquema
. Assim, no esquema




Em conformidade com essas exigências, o nome oficial para o H3C-CH2-C(CH3)2-CH(CH3)-COOH é:
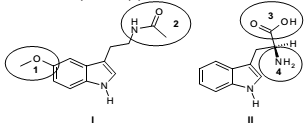
As funções representadas nas figuras pelos números 1, 2, 3 e 4 são, respectivamente:
I 2-metilbutano + bromo (luz e calor) → A + HBr
II Etano + bromo (luz e calor) → B + HBr
Os produtos indicados pelas letras A e B são respectivamente:
H3C-(CH2 )2 -CH(CH3 )-CH(C2H5 )-CH=C(C3 H7 )2
Assinale a alternativa que apresenta uma afirmação correta sobre esse composto.
Considerando a informação, assinale a alternativa que apresenta o produto da reação entre o 2 metil 2 buteno e o HCl:
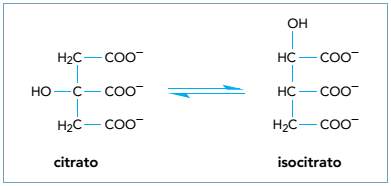
A isomeria plana que ocorre entre o citrato e o isocitrato é denominada de:
O esquema abaixo representa um corte lateral de um nanotubo. Cada esfera corresponde ao núcleo de um átomo e cada traço a uma ligação entre carbonos. Não estão indicadas no esquema as ligações do tipo pi.
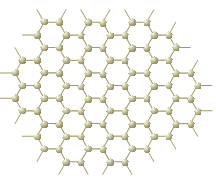
O número de ligações duplas realizadas por átomo em um nanotubo corresponde a: