Questões de Vestibular
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 996 questões
Vinagre é uma mistura homogênea cujo principal constituinte é o ácido acético. Um estudante de química analisou uma amostra de uma garrafa de 500mL de vinagre de maçã, em que, no rótulo, há a informação de que o teor do ácido acético presente na solução é de 4,2% m/v.
Considerando que o ácido acético é o único composto de caráter ácido do vinagre, analise as proposições sugeridas pelo estudante após as análises.
I- A molaridade do ácido acético na amostra analisada é 0,7mol/L.
II- Ao titular 20mL desse vinagre com hidróxido de sódio 1mol/L, foram gastos 50mL da base.
III- Uma cozinheira que utiliza 6,3g de vinagre por dia, durante 30 dias, irá utilizar 9 garrafas.
Está(ão) CORRETA(S) a(s) afirmativa(s):
Algumas substâncias de uso cotidiano são conhecidas por nomes populares desprovidos de qualquer regra de nomenclatura. Assim, temos, por exemplo, sublimado corrosivo (HgCl2 ), cal viva (CaO), potassa cáustica (KOH) e espírito de sal (HCl).
O sublimado corrosivo, a cal viva, a potassa cáustica e o espírito de sal pertencem, respectivamente, às funções:
Um grupo de alunos do curso de Química, ao entrar no laboratório para uma atividade, deparou-se com alguns recipientes não rotulados, embora todos contivessem uma substância líquida e incolor.
Considerando as substâncias, os acadêmicos determinaram as seguintes propriedades para reconhecimento: 1) massa, 2) volume, 3) ponto de ebulição, 4) densidade.
Com base nestas informações, indique quais propriedades possibilitaram aos acadêmicos a identificação das substâncias:
Um comprimido efervescente contendo 1 g de vitamina C foi dissolvido em água, de modo a obter-se 200 mL de solução. A concentração de ácido ascórbico na solução obtida é, aproximadamente,
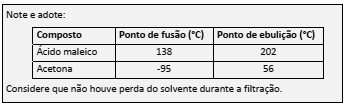
Em um experimento, determinadas massas de ácido maleico e acetona foram misturadas a 0 °C, preparando‐se duas misturas idênticas. Uma delas (X) foi resfriada a ‐78 °C, enquanto a outra (M) foi mantida a 0 °C. A seguir, ambas as misturas (M e X) foram filtradas, resultando nas misturas N e Y. Finalmente, um dos componentes de cada mistura foi totalmente retirado por destilação. Os recipientes (marcados pelas letras O e Z) representam o que restou de cada mistura após a destilação. Nas figuras, as moléculas de cada componente estão representadas por retângulos ou triângulos.
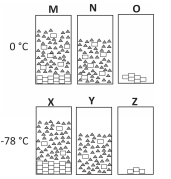
Tanto no recipiente M como no recipiente X, estão representadas soluções ___I___ de ___II___, cuja solubilidade ___III___ com a diminuição da temperatura. A uma determinada temperatura, as concentrações em M e N e em X e Y são ___IV___. Em diferentes instantes, as moléculas representadas por um retângulo pertencem a um composto que pode estar ___V___ ou no estado ___VI___.
As lacunas que correspondem aos números de I a VI devem ser corretamente preenchidas por:
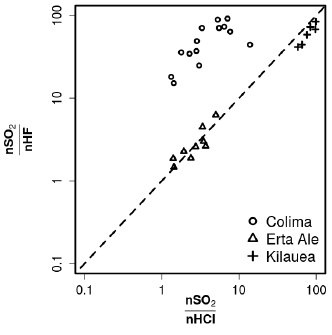
De acordo com a figura, em relação às quantidades de gases dissolvidos no magma, é correto afirmar que as concentrações de SO2 são maiores que as de HF e de HCl
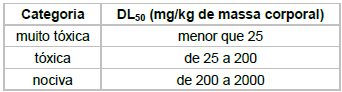
Considerando que a DL50 – dose necessária de uma dada substância para matar 50% de uma população – da cafeína é de 192 mg/kg, no teste realizado a dose aplicada foi cerca de
Diferentes métodos são utilizados por profissionais da área de Ciência Forense para determinar a quanto tempo o indivíduo veio a óbito. Pesquisadores brasileiros reportaram que existe uma relação linear entre a concentração de Fe2+ no corpo vítreo do olho com o intervalo pós-morte. Este método é baseado em uma reação de Fe2+ com orto-fenantrolina como agente cromogênico realizada em um dispositivo de papel, cujo produto da reação apresenta coloração alaranjada. Desta forma, quanto maior o tempo de intervalo pós-morte maior a intensidade de coloração do produto.
(Adaptado de: GARCIA, P.T.; GABRIEL, E.F.M.; PESSÔA, G.S.; SANTOS JUNIOR, J.C.; MOLLO FILHO, P. C.; GUIDUGLI, R.B.F.; HÖEHR, N.F.; ARRUDA, M.A.Z.; COLTRO, W.K.T, Analytica Chimica Acta, v. 974, n.29, p.69-74, 2017).
A equação química da reação de Fe2+ com orto-fenantrolina é apresentada na figura seguir.
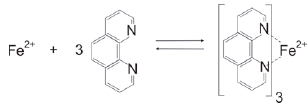
Considerando os conceitos, as definições de ácido e base e a reação química apresentada, assinale a alternativa correta.

Com base nas informações fornecidas, qual dos sais indicados a seguir é o mais eficiente como solução neutralizante?
A dipirona (C13H16N3O4SNa) é um medicamento muito utilizado para aliviar a dor e para baixar a febre. Ana ao observar que seu filho João de 3 anos estava com febre, por indicação médica, diluiu 10 gotas do medicamento de concentração 500 mg/mL em água e deu ao seu filho. Qual a quantidade de moléculas de dipirona ingeridas por João?
Dados: 1mL = 20 gotas; Constante de Avogrado = 6x1023 moléculas/mol C=12g/mol; O=16g/mol; N=14g/mol; S=32g/mol; H=1g/mol; Na=23g/mol.
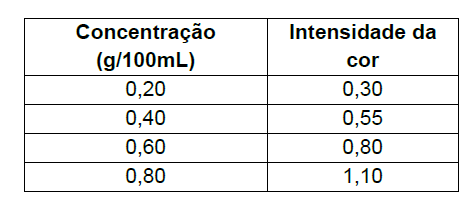
Qual é a concentração, em gramas por litro, de uma solução de glicose que, após a reação, apresenta intensidade de cor igual a 0,80?
I - O grau de ionização de um ácido fraco, como o ácido acético, aumenta com o aumento da diluição. II - A maior concentração de um ácido forte acarreta maior grau de ionização e maior constante de ionização. III- A segunda constante de ionização de um ácido poliprótico é sempre menor que a primeira constante.
Quais estão corretas?
O soro fisiológico é uma solução aquosa 0,9% em massa de NaCl. Um laboratorista preparou uma solução contendo 3,6 g de NaCl em 20 mL de água.
Qual volume aproximado de água será necessário adicionar para que a concentração corresponda à do soro fisiológico?
O ácido sulfúrico, um dos compostos mais importantes do ponto de vista industrial no mundo moderno, pode reagir com diversas substâncias.
Na coluna da esquerda abaixo, estão relacionadas substâncias que reagem com o ácido sulfúrico; na da direita, forças motrizes que favorecem a ocorrência das reações.
Associe a coluna da direita à da esquerda.
( ) KNO2
( ) Na2CO3
( ) Ba(NO3)2
1 - forma gás
2 - forma ácido fraco
3 - forma precipitado
4 - forma um sal básico
Assinale com V (verdadeiro) ou F (falso) as afirmações abaixo, referentes a compostos inorgânicos.
( ) A sílica, presente na areia, e o gás carbônico fazem parte da mesma função inorgânica: os óxidos.
( ) O número de oxidação do oxigênio, no composto OF2, é – 2.
( ) O óxido de alumínio pode comportar-se como óxido ácido ou como óxido básico.
A sequência correta de preenchimento dos parênteses, de cima para baixo, é
Assinale com V (verdadeiro) ou F (falso) as afirmações abaixo, referentes a compostos inorgânicos.
( ) O fosfato de sódio, embora seja considerado um composto iônico, possui ligações covalentes no íon fosfato.
( ) Compostos iônicos tendem a ter pontos de fusão e ebulição mais elevados do que os compostos moleculares.
( ) BeF2 não obedece à regra do octeto.
A sequência correta de preenchimento dos parênteses, de cima para baixo, é
Observe o gráfico abaixo, referente à pressão de vapor de dois líquidos, A e B, em função da temperatura.
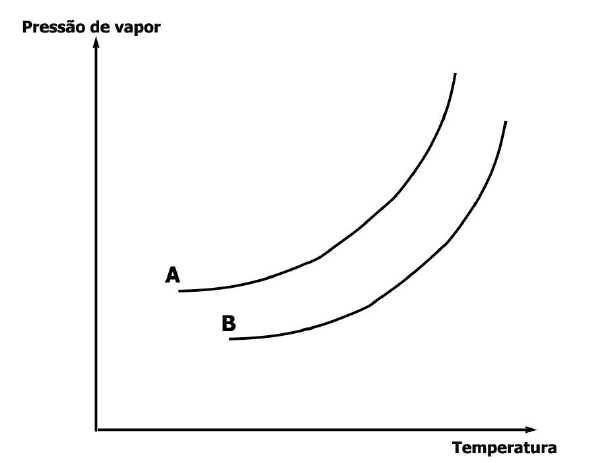
Considere as afirmações abaixo, sobre o gráfico.
I - O líquido B é mais volátil que o líquido A.
II - A temperatura de ebulição de B, a uma dada pressão, será maior que a de A.
III- Um recipiente contendo somente o líquido A em equilíbrio com o seu vapor terá mais moléculas na fase vapor que o mesmo recipiente contendo somente o líquido B em equilíbrio com seu vapor, na mesma temperatura.
Quais estão corretas?