Questões de Vestibular
Sobre substâncias inorgânicas e suas características: ácidos, bases, sais e óxidos. reações de neutralização. em química
Foram encontradas 385 questões
Na notícia “Nova Iorque planeja liderança em reciclagem”, do site da Science American Brasil, há importantes referências ao sofisticado sistema de separação dos materiais presentes no lixo dessa cidade.
“A primeira coisa que a usina do Brooklyn fará é rasgar e remover as sacolas plásticas que tantos nova-iorquinos usam para empacotar seus recicláveis. O vidro será moído, separado e transportado pelo Porto de Nova York até Nova Jersey, onde ele passará por uma nova máquina de raios-x para ser novamente separado; contaminantes como boro e vidro com chumbo também serão removidos. De volta ao Brooklyn, outros recicláveis passam por uma correia transportadora enquanto ímãs extraem metais ferrosos.
O plástico e o alumínio restantes são passados por correntes de Foucault, que extraem o alumínio.”
TWEED, Katherine. Nova Iorque planeja liderança em reciclagem. Scientifi c American Brasil.
(http://www2.uol.com.br/sciam/noticias/nova_iorque_ planeja_lideranca_em_reciclagem.html).
Sobre os materiais citados no texto, é correto afirmar
que
Durante o verão, verificam-se habitualmente tempestades em muitas regiões do Brasil. São chuvas intensas e de curta duração, acompanhadas muitas vezes de raios. No litoral, essas tempestades constituem um risco para os banhistas, pois a água salgada é eletricamente condutora. Isso se explica pelo fato de a água salgada conter grande quantidade de _________, como Na+ e Cl−, livres para transportar carga elétrica no meio. Uma maneira de liberar essas partículas é dissolver sal de cozinha em um copo de água. Nesse processo, os _________ existentes no sal sofrem _________.
As expressões que completam corretamente o texto são, respectivamente:

Desde a década de 70, não há comercialização do minério bruto ou do concentrado de nióbio (pirocloro) no mercado interno ou externo. O metal é vendido, sobretudo, na forma da liga ferro-nióbio (FeNb STD, com 66% de teor de nióbio e 30% de ferro), obtida a partir de diversas etapas de processamento. Segundo o governo, as exportações de ferro-liga de nióbio atingiram em 2012 aproximadamente 71 mil toneladas, no valor de US$ 1,8 bilhão.
(http://g1.globo.com. Adaptado.)
x Nb2 O5 (s) + y Al (s) → z Nb (s) + w Al2 O3 (s)
Nessa equação, os coeficientes estequiométricos x, y, z e w valem, respectivamente,

Desde a década de 70, não há comercialização do minério bruto ou do concentrado de nióbio (pirocloro) no mercado interno ou externo. O metal é vendido, sobretudo, na forma da liga ferro-nióbio (FeNb STD, com 66% de teor de nióbio e 30% de ferro), obtida a partir de diversas etapas de processamento. Segundo o governo, as exportações de ferro-liga de nióbio atingiram em 2012 aproximadamente 71 mil toneladas, no valor de US$ 1,8 bilhão.
(http://g1.globo.com. Adaptado.)
Na 9,75% Ca 5,66% Nb 52,51% H 0,21% O 30,52% F 1,34%
Considerando que não haja perdas, é correto afirmar que a massa de pirocloro necessária para obter 1,0 t da liga FeNb STD é, em t, aproximadamente,
Artur era um menino desses que não param quietos em casa. Estava sempre na rua brincando com os amigos, e com frequência voltava para casa machucado. Certa vez, o guri apareceu com um talho na coxa, que a mãe desinfetou com água oxigenada. Enquanto ela limpava a ferida com algodão, o pequeno notou que a água oxigenada soltava bolhas, ao encostar na carne viva. A mãe explicou que aquilo eram bolhas de oxigênio, o mesmo gás que nós respiramos no ar, e que o que ele estava vendo era uma reação química.
Quando Artur ficou maior, aprendeu na escola que água oxigenada é uma solução de peróxido de hidrogênio que se decompõe rapidamente em oxigênio e água, quando entra em contato com a enzima catalase, que existe na carne. Também aprendeu que o peróxido de hidrogênio desinfeta, mas também pode dificultar a cicatrização, porque “rouba” elétrons e destrói as proteínas que ajudam a fechar a ferida.
Com base nas informações, é correto afirmar que:
De acordo com o conhecimento químico, o sabão de cinzas se forma mediante a ocorrência de reações químicas entre a potassa, que é obtida das cinzas, e os ácidos graxos presentes na gordura animal.
A palavra potassa é usada em geral para indicar o carbonato de potássio (K2 CO3 ), que, em meio aquoso, sofre hidrólise. A produção do sabão é possível porque a hidrólise da potassa leva à formação de um meio fortemente

O gráfico abaixo mostra a variação do volume do conteúdo em cada recipiente em função do tempo.

Sabendo que a concentração inicial da solução ácida é igual a 0,10 mol.L-1 , a concentração inicial da solução básica, em mol.L-1 , corresponde a:
“Grande parte do interesse pelo sal, como os experimentos dos antigos chineses com o salitre, visava proporcionar aos militares métodos mais eficientes de detonar coisas e gente. No século XIX, descobriu- se que o clorato de potássio produzia uma explosão maior que a pólvora tradicional, o nitrato de potássio. E o magnésio tinha propriedades explosivas ainda mais impressionantes.”
KURLANSKY, Mark. Sal: uma história do mundo.
São Paulo: SENAC, 2004. p. 291.
O sal que produzia maior explosão provém da reação entre as substâncias de fórmulas
Esses metais são encontrados comumente na forma de óxidos, sendo o caráter iônico dos óxidos diretamente proporcional ao raio atômico do metal.
O metal terra rara componente do óxido de maior caráter iônico possui o seguinte símbolo:

Considerando essas informações, julgue os próximos itens.

Considerando essas informações, julgue os próximos itens.
Os fogos de artifício são dispositivos envolvidos em um cartucho de papel. Na parte inferior, está a carga explosiva, que dispara os fogos para o alto. O propelente mais utilizado é a pólvora negra, uma mistura de nitrato de potássio, enxofre e carvão. Para a produção de fogos coloridos, misturam-se sais de diferentes metais à pólvora. Elétrons dos metais, quando são excitados pelo calor, emitem, ao retornarem a níveis de energia mais baixos, radiação eletromagnética de diferentes cores. Na tabela abaixo, são listados alguns metais e a coloração característica que deles pode ser emitida.

A seguir, é apresentada uma reação da pólvora, sem balanceamento e sem os estados físicos das substâncias.

Tendo como referência as informações acima, julgue os itens seguintes.
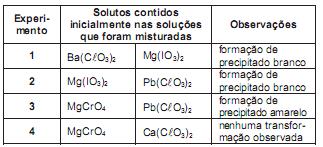
A partir desses experimentos, conclui-se que são pouco solúveis em água somente os compostos
