Questões de Vestibular
Sobre teoria atômica: átomos e sua estrutura - número atômico, número de massa, isótopos, massa atômica em química
Foram encontradas 305 questões
I. O tamanho do raio atômico dos elementos químicos cresce da direita para a esquerda nos periódicos e cresce de cima para baixo nos grupos.
II. O tamanho do raio atômico dos elementos químicos cresce da esquerda para direita nos periódicos, assim como a eletropositividade.
III. O iodo apresenta raio atômico menor do que o cloro.
IV. O nitrogênio apresenta raio atômico maior do que o flúor.
Analise a alternativa correta.
Na – 1s 2 2s 2 2p6 3s 1
Fe – 1s 2 2s 2 2p6 3s 2 3p6 4s 2 3d6
P – 1s 2 2s 2 2p6 3s 2 3p3
A partir das distribuições eletrônicas acima, assinale a alternativa incorreta.
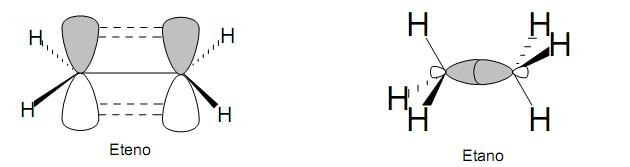
Na figura acima, temos os modelos simplificados da formação das ligações químicas de eteno e etano. De acordo com os orbitais explícitos nessas moléculas, é CORRETO afirmar que representam, respectivamente, ligações do tipo:
I. Cátions são íons de carga positiva.
II. Ligações iônicas são formadas pelo compartilhamento de elétrons.
III. O Potencial de ionização nos elementos da família 1A é diretamente proporcional ao raio atômico.
IV. Uma ligação covalente é exclusivamente uma ligação π (pi).
V. Elementos com distribuição eletrônica final em np5 , são por características, doadores de elétrons.
VI. Ligações metálicas são realizadas por todos os elementos representativos.
VII. A formação de um líquido é devido a atrações eletrostáticas entre íons.
VIII. Átomos com hibridização sp2 correspondem a elementos da família 2A da tabela periódica.
IX. Potencial de ionização corresponde à energia necessária para a retirada de um elétron da camada de valência, portanto, é um processo exotérmico.
É CORRETO o que se afirma apenas em:
I. Fissão nuclear é o processo de quebra de núcleos grandes em núcleos menores, liberando uma grande quantidade de energia, a exemplo da reação representada pela equação:
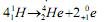
II. Na natureza existem três isótopos de carbono:
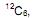
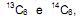 o menos abundante deles o
o menos abundante deles o 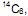 é radioativo e emite partículas β (beta), sua formação se dá na alta atmosfera onde ocorre transmutação nuclear causada pela colisão de nêutrons cósmicos (vindo do espaço) com átomos de nitrogênio do ar.
é radioativo e emite partículas β (beta), sua formação se dá na alta atmosfera onde ocorre transmutação nuclear causada pela colisão de nêutrons cósmicos (vindo do espaço) com átomos de nitrogênio do ar. III. Um artefato de madeira, cujo teor determinado de
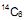 (com período de meia vida de 5.730 anos) corresponde a 25% daquele presente nos organismos vivos, pode ser identificado como sendo oriundo de uma árvore cortada no período dinástico do Egito (2920 a. C a 2575 a. C).
(com período de meia vida de 5.730 anos) corresponde a 25% daquele presente nos organismos vivos, pode ser identificado como sendo oriundo de uma árvore cortada no período dinástico do Egito (2920 a. C a 2575 a. C). IV. As plantas e os animais incorporam o isótopo de carbono-14 pelo
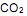 da atmosfera ou através da cadeia alimentar,e quando morrem a quantidade de carbono-14 decai e ele se desintegra por meio de caimento β (beta) de acordo com a equação:
da atmosfera ou através da cadeia alimentar,e quando morrem a quantidade de carbono-14 decai e ele se desintegra por meio de caimento β (beta) de acordo com a equação: 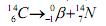
É CORRETO o que se afirma apenas em:
1s 2 2s 2 2p6 3s 2 3p6 4s 2 3d10 4p4
Podemos propor, para este elemento:
I. O número de prótons no núcleo atômico é 34.
II. É um elemento pertencente ao grupo IVA da Tabela Periódica.
III. O último elétron distribuído na camada de valência possui o número quântico magnético igual a zero.
IV. A subcamada de menor energia, pertencente à camada de valência é a 4s.
Analise as proposições e marque a opção CORRETA:
I. A eletronegatividade é a força de atração exercida sobre os elétrons de uma ligação, e relaciona-se com o raio atômico de forma diretamente proporcional, pois à distância núcleo-elétrons da ligação é menor.
II. A eletroafinidade é a energia liberada quando um átomo isolado, no estado gasoso, captura um elétron; portanto, quanto menor o raio atômico, menor a afinidade eletrônica.
III. Energia (ou potencial) de ionização é a energia mínima necessária para remover um elétron de um átomo gasoso e isolado, em seu estado fundamental.
IV. O tamanho do átomo, de modo geral, varia em função do número de níveis eletrônicos (camadas) e do número de prótons (carga nuclear).
É CORRETO o que afirma em:


A respeito do assunto abordado no texto acima, assinale a opção
correta e julgue o item.


A respeito do assunto abordado no texto acima, assinale a opção
correta e julgue o item.


Com relação ao texto, às figuras e aos múltiplos aspectos que eles suscitam, julgue o item.
 , modelados como problemas que envolvem três corpos.
, modelados como problemas que envolvem três corpos.
O teste descrito no texto se baseia na propriedade dos átomos de carbono conhecida como
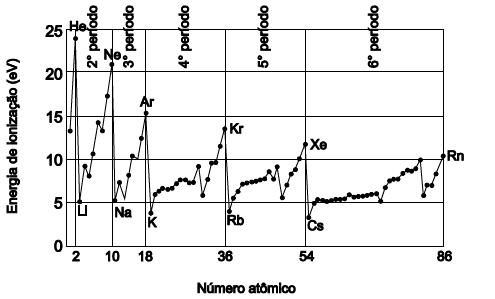
A energia de ionização de um átomo é uma propriedade periódica, cuja unidade de medida é o eletronvolt, eV, que é a energia mínima necessária para se retirar um elétron de um átomo gasoso, no estado fundamental. O gráfico representa a variação dos valores dos primeiros potenciais de ionização em função do número atômico.
Uma análise dessas informações e com base nesse gráfico, pode-se concluir:

