Questões de Vestibular
Sobre teoria atômica: modelo atômico de dalton, thomson, rutherford, rutherford-bohr em química
Foram encontradas 125 questões
O quadrinho a seguir mostra uma paródia entre situações cotidianas e descobertas científicas.

Quais feitos científicos de Mendeleev, de Watson e Crick e de
Thomson estão relacionados com o quadrinho?
A primeira teoria atômica descrita por Epicuro (341 a.C. – 271 a.C.) na carta a Heródoto e resgatada por Titus Lucretius Carus (94 a.C. – 50 a.C.) na obra De Rerum Natura (sec. I a.C.) afirma que “alguns corpos são compostos, enquanto outros são elementos de que se compõem os corpos compostos”.
Esses elementos são os átomos, indivisíveis e imutáveis. Alguns séculos depois esse postulado foi admitido por
DADOS QUE PODEM SER USADOS NESTA PROVA

DADOS QUE PODEM SER USADOS NESTA PROVA

I. O subnível “s” contém o número máximo de elétrons. II. O subnível “p” contém o triplo do número de elétrons do subnível “s”. III. O subnível “d” contém o número x + 4 de elétrons, onde x é o número de elétrons que contém o subnível “p”. IV. O subnível “f” contém menos 3 elétrons do número de elétrons que contém o subnível “d”.
De acordo com a distribuição acima apresentada, é correto afirmar que o número total de elétrons deste nível energético é
No fragmento a seguir, o autor explora conceitos químicos na forma de poesia:
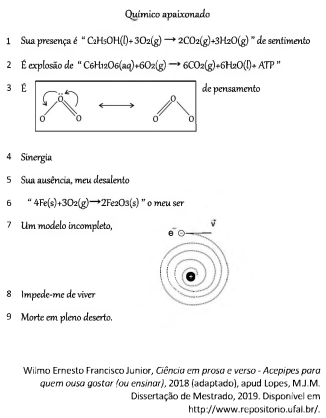
Sobre os conceitos mencionados, foram feitas as seguintes afirmações:
I. A equação química mostrada na linha 2 pode ser associada à liberação de energia, pois corresponde à reação de fotossíntese com consumo de gás carbônico.
II. A equação química apresentada na linha 6 representa uma reação na qual o número de oxidação das espécies é alterado, sendo associada a corrosão.
III. O modelo incompleto referido na linha 7 refere-se ao proposto por Thomson, que identificava a presença de partículas com carga negativa dentro de uma esfera.
Está correto o que se afirma no(s) item(ns):
Assinale a alternativa que representa o modelo atômico de Dalton.

A goethita (αFeOOH) tem sido utilizada em diversas aplicações como em medicamentos para tratamento digestivos, como catalizador para eliminação de gases sulfurosos em biodigestores, na eliminação de metais como cádmio em águas poluídas e para produção de pigmentos sintéticos amarelos usados nas indústrias de tintas. Qual a distribuição eletrônica para o íon de Ferro encontrado na goethita? (Adaptado de: Baptista, Nelson Pedro. Investigação das características f´ísicas, químicas e cristalográficas de óxido de ferro produzidos por nucleação prímaria heterogênea. Dissertação de mestrado. São Paulo, 2010 – Instituto de pesquisas tecnológicas do estado de são Paulo)
I. Os elétrons movimentam-se ao redor do núcleo em trajetórias circulares, denominadas níveis, com valores determinados de energia. II. O núcleo contém quase a totalidade da massa do átomo. III. Quando um elétron absorve um quantum de energia, ele salta para uma órbita mais energética ligeiramente mais afastada do núcleo. Dessa forma, o elétron realizou um salto quântico e atingiu um estado excitado.
Está(ão) correta(s) a(s) afirmativa(s)
Quem propôs este modelo?
A partir do século XIX, a concepção da ideia de átomo passou a ser analisada sob uma nova perspectiva: a experimentação. A cada novo fenômeno que surgia, propunha-se um novo modelo para explicá-lo. Assim, o modelo de Thomson veio depois do modelo de Dalton.
O modelo atômico proposto por Thomson avançou em relação ao modelo de Dalton porque
acrescentou a ideia de
Com esse modelo, é possível explicar
O teste de chama é uma técnica utilizada para identificar átomos ou cátions presentes em substâncias ou misturas. Por exemplo, quando uma pequena quantidade de cloreto de sódio é levada à chama de um bico de Bunsen, observa-se que a chama inicialmente azul adquire uma coloração laranja. Assim, na queima de fogos de artifício, verificamos várias cores devido aos diferentes sais utilizados na fabricação dos fogos.
Essas cores podem ser explicadas pelo modelo atômico de
Analise as afirmativas a seguir em relação aos números quânticos:
I. o número quântico principal corresponde aos níveis de energia do elétron e também é chamado por uma letra de acordo com o nível (K, L, M...).
II. os elementos representativos na tabela periódica possuem sua distribuição eletrônica terminando nos subníveis s e p, enquanto os elementos de transição interna terminam sua distribuição eletrônica no subnível d e os elementos de transição completam sua distribuição eletrônica no subnível f .
III. o número quântico de spin descreve o momento magnético do elétron.
IV. o número quântico magnético descreve o orbital e é a causa do ferromagnetismo das substâncias.
V. os quatro números quânticos somente assumem valores inteiros.
Assinale a alternativa CORRETA.
