Questões de Vestibular
Sobre teoria atômica: modelo atômico de dalton, thomson, rutherford, rutherford-bohr em química
Foram encontradas 125 questões
Esse efeito, conhecido como
Considere o enunciado para o modelo atômico:
“O átomo é uma minúscula esfera maciça, impenetrável, indestrutível, indivisível e sem carga.”
Tal enunciado refere-se ao modelo atômico proposto por:
 Oliver Sacks, Tio Tungstênio: Memórias de uma infância química.
Oliver Sacks, Tio Tungstênio: Memórias de uma infância química. De acordo com o autor,
A história do Modelo de Bohr
1. Que a energia radiada não é emitida (ou absorvida) da maneira contínua admitida pela eletrodinâmica clássica, mas apenas durante a passagem dos sistemas de um estado "estacionário" para outro diferente. 2. Que o equilíbrio dinâmico dos sistemas nos estados estacionários é governado pelas leis da mecânica clássica, não se verificando estas leis nas transições dos sistemas entre diferentes estados estacionários. 3. Que é homogênea a radiação emitida durante a transição de um sistema de um estado estacionário para outro, e que a relação entre a frequência n e a quantidade total de energia emitida é dada por E = hn, sendo h a constante de Planck. 4. Que os diferentes estados estacionários de um sistema simples constituído por um elétron que gira em volta de um núcleo positivo são determinados pela condição de ser igual a um múltiplo inteiro de h/2 a razão entre a energia total emitida durante a formação da configuração e a frequência de revolução do elétron. Admitindo que a órbita do elétron é circular, esta hipótese equivale a supor que o momento angular do elétron em torno do núcleo é igual a um múltiplo inteiro de h/2p. 5. Que o estado "permanente" de um sistema atômico - isto é, o estado no qual a energia emitida é máxima - é determinado pela condição de ser igual a h/2p o momento angular de cada elétron em torno do centro da sua órbita.
Disponível em: <https://www.if.ufrgs.br/tex/fis142/fismod/mod06/m_s04.html> Acesso em: 15 abr. 2017.
O problema que motivou Bohr a propor suas explicações e, consequentemente, seu modelo, baseou-se em qual das seguintes considerações?
Com relação a essas descrições, três afirmações foram feitas:
1) Nos átomos ou moléculas, os elétrons podem absorver ou emitir energia, passando de um orbital para outro.
2) A teoria quântica foi fundamental para o desenvolvimento do modelo atômico atual.
3) O modelo atômico de Bohr é o modelo atômico mais atual.
Está(ão) correta(s) a(s) afirmativa(s):
DADOS QUE PODEM SER USADOS NESTA PROVA:

A construção deste modelo deve-se ao fato de:
( ) Thompson afirmou que o núcleo do átomo tem carga negativa.
( ) Eletrosfera é a região do átomo que tem volume praticamente igual ao volume do átomo.
( ) Bohr disse que o próton e o elétron possuem massas iguais.
( ) Na experiência de Rutherford, a maioria da radiação emitida pelo polônio radioativo passou pela lâmina de ouro como se esta fosse uma peneira.
( ) O modelo de Dalton ficou conhecido como o “pudim de passas”.
Assinale a alternativa que corresponde à sequência correta:
Existem quatro números quânticos: número quântico principal; número quântico de momento angular ou azimutal (secundário); número quântico magnético e número quântico de spin. Esses quatro números quânticos, além de se complementarem, nos permitem fazer uma descrição completa dos elétrons nos átomos, pois eles representam o nível principal de energia do elétron, o subnível de energia, a orientação espacial da nuvem eletrônica e a orientação do próprio elétron na nuvem.
Considerando as informações, dentre as seguintes séries de números quânticos abaixo, aquela que descreve corretamente um elétron em um dado átomo é:
Considerando-se a comparação apresentada no enunciado, a presença de eletrosfera é coerente com os modelos atômicos de
Para o elétron mais energético do átomo de escândio no estado fundamental, os números quânticos principal e secundário são respectivamente
Desta forma. podemos afirmar que: 1) a emissão de luz em lâmpadas elétricas ocorre devido à excitação do núcleo do átomo. 2) a emissão de luz em lâmpadas elétricas ocorre devido à excitação do elétron do átomo. 3) os elétrons mais externos absorvem energia passando para orbitais em níveis de energia mais elevados e emitem luz ao retornarem para o orbital de origem. Está(ão) correta(s) a(s) afirmativa(s):
ELEMENTO NÚMERO MASSA
QUÍMICO ATÔMICO ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Cr 24 52,0
Cu 29 63,5
As 33 75,0
Br 35 80,0
Ag 47 108,0
Sn 50 119,0
Ir 77 192,0
Au 79 197,0
Hg 80 200,0
ELEMENTO NÚMERO MASSA
QUÍMICO ATÔMICO ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Cr 24 52,0
Cu 29 63,5
As 33 75,0
Br 35 80,0
Ag 47 108,0
Sn 50 119,0
Ir 77 192,0
Au 79 197,0
Hg 80 200,0
Atente à figura a seguir, que representa o núcleo e a eletrosfera do átomo.
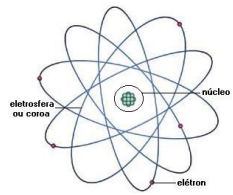
Com relação à figura acima, é correto afirmar que
ELEMENTO NÚMERO MASSA
QUÍMICO ATÔMICO ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Cr 24 52,0
Cu 29 63,5
As 33 75,0
Br 35 80,0
Ag 47 108,0
Sn 50 119,0
Ir 77 192,0
Au 79 197,0
Hg 80 200,0
