Questões de Vestibular
Foram encontradas 391 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
TEXTO 2
XX
Os Homens
nesta manhã de sangrenta primavera
parecem não mais saber
o que nunca souberam,
que a Vida é para sempre
sã ou demente
tão de repente
tão de repente!
(VIEIRA, Delermando. Os tambores da tempestade. Goiânia: Poligráfica, 2010. p. 108.)
Hb + O2
 HbO2
HbO2Com base nessas informações, analise as afirmativas a seguir:
I- O sangue, por ser uma solução tampão, não sofrerá alteração de pH, mesmo com a adição de grande quantidade de ácidos ou de bases.
II- O sangue tem pH em torno de 7, e o suco gástrico,em torno de 2. Isso significa uma diferença de concentração de íons hidrônio na ordem de 105.
III- Ao se subir a montanha Everest, a mudança na pressão atmosférica resulta no deslocamento da reação da hemoglobina com o oxigênio para a esquerda.
IV-O CO2 proveniente da respiração celular pode reagir com a água antes de ser transportado pela hemoglobina e ser transformado em íons hidrônio e carbonato (CO32–). A geometria molecular desse ânion é piramidal.
Em relação às proposições analisadas, assinale a única alternativa cujos itens estão todos corretos:
A ionização do ácido cianídrico é representada pela equação química abaixo:
HCN (aq)  H+ (aq) + CN–
(aq)
H+ (aq) + CN–
(aq)
Um experimento sobre esse equilíbrio químico, realizado a temperatura constante, analisou quatro parâmetros, apresentados na tabela:
Parâmetro Símbolo
grau de ionização α
constante de equilíbrio Ka
potencial hidrogeniônico pH
concentração de HCN [HCN]
Ao ser estabelecido o equilíbrio químico da ionização, foi adicionada certa quantidade de NaCN(s). Após a dissolução e dissociação completa desse composto, houve deslocamento do equilíbrio de ionização.
O parâmetro que sofreu redução, após a adição do composto, é representado pelo seguinte
símbolo:
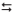 NH4(aq) + OH−
(aq) , assinale a alternativa que
apresenta a concentração do íon OH−
em mol/L e o pH da
solução nas condições dadas. Considere que para o
hidróxido de amônio Kb=1,0x10-5.
NH4(aq) + OH−
(aq) , assinale a alternativa que
apresenta a concentração do íon OH−
em mol/L e o pH da
solução nas condições dadas. Considere que para o
hidróxido de amônio Kb=1,0x10-5.CS2(l) + 3O2(g) → CO2(g) + 2SO2(g)