Questões Militares Sobre química
Foram encontradas 2.062 questões
Analise as espécies apresentadas na tabela.
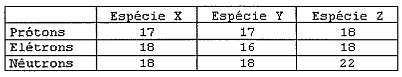
Acerca destas espécies, analise as afirmativas abaixo.
I - As espécies X e Y são átomos isótopos.
II - As espécies Y e Z estão lado a lado na classificação periódica.
III- A espécie Z representa um elemento classificado como gás nobre .
IV - As espécies X e Y são íons de um mesmo elemento.
Assinale a opção correta.
O silício é realmente um material notável.. Escapando da óbvia associação com componentes de computadores, ele permite não apenas projetar o futuro, através da informática, mas também proteger o passado. Como assim? Em condições apropriadas, o silício, que é integrante da mesma família que o carbono na classificação periódica dos elementos, forma com o hidrogênio um composto de fórmula molecular SiH4, chamado silano, a exemplo do metano (CH4) .
Um dos possíveis usos do silano é ser aplicado como revestimento de paredes e fachadas que se deseja proteger da ação criminosa de pichadores já que, após a aplicação do silano, a tinta spray não mais adere à superfície.
Neste contexto, é correto afirmar que:
Em 1869, Mendeleyev, enquanto escrevia seu livro de química inorgânica, elaborou os pressupostos que conduziram à tabela periódica atual, organizando os 63 elementos então conhecidos em ordem crescente de suas massas atômicas e agrupando-os segundo a semelhança de suas propriedades químicas e físicas. Formou-se, então, uma tabela periódica coerente e que permitia até prever algumas propriedades de elementos químicos ainda desconhecidos na época.
Em 1913, Moseley retificou a tabela de Mendeleyev colocando os elementos em ordem crescente de número atômico. A partir da descoberta do Plutônio (1940), a tabela recebeu uma última contribuição quando Seaborg reconfigurou a tabela periódica colocando a série dos actnídeos abaixo da série dos lantanídeos.
Sobre a Tabela Periódica, é correto afirmar que
Analise as afirmativas abaixo em relação a alguns conceitos fundamentais da Química.
I - Todos os átomos são iguais em qualquer substância pura.
II - Mistura é a união sem reação de mais de duas substâncias.
III- Em quaisquer condições os gases são sempre miscíveis entre si.
IV - Um sistema heterogêneo é sempre uma mistura.
Assinale a opção correta.
Observe a figura a seguir.
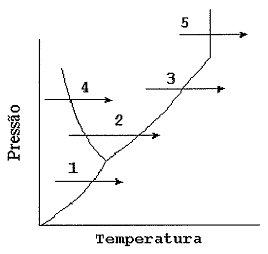
O diagrama acima, descreve o comportamento de uma substância
semelhante ao da água. Em relação às setas indicadas, qual
seta representa a mudança de fase conhecida como sublimação?
Um elemento químico teórico M tem massa atômica igual a 24,31 u e apresenta os isótopos 24M, 25M e 26M. Considerando os números de massa dos isótopos iguais às massas atômicas e sabendo-se que a ocorrência do isótopo 25 é de 10,00%, a ocorrência do isótopo 26 é
Uma amostra de 1,72 g de sulfato de cálcio hidratado (CaSO4 · n H2O), onde “n” representa o número de molécula(s) de água (H2O), é aquecida até a eliminação total da água de hidratação, restando uma massa de 1,36 g de sulfato de cálcio anidro.

A fórmula molecular do sal hidratado é:
Analise as afirmações I, II, III e IV abaixo referente(s) à(s) característica(s) e/ou informação(ões) sobre algumas substâncias, nas condições ambientes:
I- A substância é a principal componente do sal de cozinha e pode ser obtida pela evaporação da água do mar. Dentre seus muitos usos podemos citar: a produção de soda cáustica e a conservação de carnes.
II- A substância é classificada como composta, e pode fazer parte da chuva ácida. Dentre seus muitos usos, podemos citar: utilização em baterias de automóveis e na produção de fertilizantes, como o sulfato de amônio.
III-A substância em solução aquosa é vendida em drogarias e utilizada como antisséptico e alvejante. Algumas pessoas utilizam essa substância para clarear pelos e cabelos.
IV-A substância é classificada como simples, tem seu ponto de ebulição igual a -195,8 ºC, é a mais abundante no ar atmoférico e reage com o gás hidrogênio produzindo amônia.
As substâncias que correspondem às afirmações I, II, III e IV são, respectivamente,
O dissulfeto de carbono, CS2, é um líquido incolor, volátil, que pode ser produzido em erupções vulcânicas.DADOS:Sobre essa substância, considere as seguintes afirmações:
I-A geometria da molécula do dissulfeto de carbono é igual à geometria da molécula da água.
II-O dissulfeto de carbono é um líquido totalmente solúvel em água, nas condições ambientes.
III-As interações entre as moléculas do dissulfeto de carbono são do tipo dipolo induzidodipolo induzido.

Das afirmações feitas, está(ão) correta(s)
Um professor de Química, durante uma aula experimental, pediu a um de seus alunos que fosse até o armário e retornasse trazendo, um por um, nesta ordem: um oxiácido inorgânico; um diácido; um sal de metal alcalino; uma substância que, após aquecimento, pode gerar dióxido de carbono (CO2(g)); e um sal ácido.
Assinale a alternativa que corresponde à sequência de fórmulas moleculares que atenderia corretamente ao pedido do professor.
Na equação da reação de óxido-redução, representada no quadro abaixo, a soma dos menores coeficientes estequiométricos inteiros, necessários para balanceá-la, e o agente redutor são, respectivamente,

Considere a sequência de reações associadas ao processo de oxidação do dióxido de enxofre

Uma quantidade de 5828 g de mistura de óxido de sódio(Na2O) e óxido de potássio(K2O) foi tratada com uma solução de ácido clorídrico que continha 300 mols de HCl. Admitindo-se que toda a mistura de óxidos reagiu com parte do HCl, e que o excesso de HCl necessitou de 144 mols de hidróxido de sódio(NaOH) para ser totalmente neutralizado, então a composição percentual, em massa de Na2O e de K2O era, respectivamente,

Considere as seguintes afirmações:
I) O último nível de energia de um átomo, cujo número quântico principal é igual a 4, pode ter, no máximo, 32 elétrons.
II) No estado fundamental, o átomo de fósforo possui três elétrons desemparelhados.
III) O átomo de nitrogênio é mais eletronegativo que o átomo de flúor.
IV)A primeira energia de ionização do átomo de nitrogênio é menor que a primeira energia de ionização do átomo de fósforo.
V)A configuração eletrônica 1s2 2s1 2p1 x 2p1 y 2p1 z, representa um estado ativado (ou excitado) do átomo de carbono.

Das afirmações feitas, estão corretas
São dadas as seguintes informações relativas às reações que ocorrem à temperatura de 25 °C e à pressão de 1 atm.
