Questões Militares de Química - Transformações Químicas: elementos químicos, tabela periódica e reações químicas
Foram encontradas 310 questões
Com relação ao funcionamento desses tipos de extintores e aos seus componentes químicos, julgue o item a seguir.
No texto, são apresentadas fórmulas que contêm átomos de
elementos químicos de não metal e de um metal de transição.
Com relação ao funcionamento desses tipos de extintores e aos seus componentes químicos, julgue o item a seguir.
A primeira substância citada no texto — NaHCO3 — pode ser
formada pela adição de CO2 a uma solução de hidróxido de
sódio.
Considere as seguintes afirmativas:
I - Uma reação química a temperatura e pressão constantes será espontânea se a variação da energia livre de Gibbs (ΔG) for menor que zero.
II - Em um sistema reacional onde a única forma de trabalho observável é o trabalho de expansão, a variação da entalpia (ΔH) é igual à quantidade de calor liberada ou absorvida pela reação, a pressão constante.
III - Para uma substância simples que admite mais de uma forma alotrópica, não há variação de entalpia na conversão de uma forma em outra.
São corretas:
Quando um átomo, ou um grupo de átomos, perde a neutralidade elétrica, passa a ser denominado de íon. Sendo assim, o íon é formado quando o átomo (ou grupo de átomos) ganha ou perde elétrons. Logicamente, esse fato interfere na distribuição eletrônica da espécie química. Todavia, várias espécies químicas podem possuir a mesma distribuição eletrônica.
Considere as espécies químicas listadas na tabela a seguir:

A distribuição eletrônica 1s2, 2s2, 2p6, 3s2, 3p6 (segundo o Diagrama de Linus Pauling) pode
corresponder, apenas, à distribuição eletrônica das espécies
A emissão de gases derivados do enxofre, como o dióxido de enxofre (SO2), pode ocasionar uma série de problemas ambientais e a destruição de materiais como rochas e monumentos à base de calcita (carbonato de cálcio). Essa destruição ocasiona reações com a emissão de outros gases, como o gás carbônico (CO2), potencializando o efeito poluente. Considerando as equações das reações sucessivas a 27 °C e 1 atm, admitindo-se os gases como ideais e as reações completas, o volume de CO2 produzido a partir da utilização de 2 toneladas de SO2 como reagente é, aproximadamente,
Dados
Massas Atômicas: S = 32 u ; O = 16 u ; H = 1 u ; C = 12 u ; Ca = 40 u
Constante dos gases ideais: R = 0,082 atm L
L mol-1
mol-1 K-1
K-1
Volume molar nas condições em que ocorreu a reação (27° e 1 atm) = 24,6 L/mol
SO2 (g) + 1/2 O2 (g) → SO3 (g) (equação I)
SO3 (g) + H2O (ℓ) → H2SO4 (ℓ) (equação II)
H2SO4 (ℓ) + CaCO3 (s) → CaSO4 (s) + H2O (ℓ) + CO2 (g) (equação III)
Considere os seguintes processos:
I- Atração do ferro pelo ímã.
II- Combustão da gasolina.
III- Desaparecimento de bolinhas de naftalina.
IV- Enferrujamento de um prego.
São processos químicos somente
Em ambientes fechados, o superóxido de potássio (KO2) é utilizado em máscaras de respiração, para remover o dióxido de carbono e a água do ar exalado. A remoção de água gera oxigênio para a respiração por meio da reação
4KO2(s) + 2H2O(l) → 3O2(g) + 4KOH(s). (I)
O hidróxido de potássio remove o dióxido de carbono da máscara pela reação
KOH(s) + CO2(g) → KHCO3(s). (II)
P. W. Atkins e L. Jones. Princípios de química. Rio de Janeiro: LTC, 2006, p. 125.
Com base nas informações acima, julgue o próximo item.
Considerando a proporção estequiométrica entre as
substâncias envolvidas na reação representada pela
equação I, conclui-se que cada mol de superóxido de
potássio, ao reagir com quantidade suficiente de água,
produz 0,75 mol de gás oxigênio.
Em ambientes fechados, o superóxido de potássio (KO2) é utilizado em máscaras de respiração, para remover o dióxido de carbono e a água do ar exalado. A remoção de água gera oxigênio para a respiração por meio da reação
4KO2(s) + 2H2O(l) → 3O2(g) + 4KOH(s). (I)
O hidróxido de potássio remove o dióxido de carbono da máscara pela reação
KOH(s) + CO2(g) → KHCO3(s). (II)
P. W. Atkins e L. Jones. Princípios de química. Rio de Janeiro: LTC, 2006, p. 125.
Com base nas informações acima, julgue o próximo item.
A equação II representa a reação entre uma base forte e um
óxido ácido, da qual resulta o sal carbonato de potássio
Embora o peróxido de hidrogênio (H2O2) não seja considerado um radical livre, ele é responsável, direta ou indiretamente, por diversas patologias. Em termos químicos, esse óxido é fracamente reativo, porém exerce papel deletério no organismo, por ser capaz de transpor facilmente membranas celulares e gerar o radical hidroxil (•OH), seja por meio de exposição à luz ultravioleta (equação I), seja por interação com metais de transição, como o ferro, por meio do processo conhecido como reação de fenton (equação II).

Considerando as informações acima, julgue o item a seguir.
A equação I é um exemplo de reação química de decomposição, dado
que representa a reação que forma o radical hidroxil por meio da
exposição do peróxido de hidrogênio à luz ultravioleta.
Embora o peróxido de hidrogênio (H2O2) não seja considerado um radical livre, ele é responsável, direta ou indiretamente, por diversas patologias. Em termos químicos, esse óxido é fracamente reativo, porém exerce papel deletério no organismo, por ser capaz de transpor facilmente membranas celulares e gerar o radical hidroxil (•OH), seja por meio de exposição à luz ultravioleta (equação I), seja por interação com metais de transição, como o ferro, por meio do processo conhecido como reação de fenton (equação II).

Considerando as informações acima, julgue o item a seguir.
A configuração eletrônica do íon Fe3+, segundo o diagrama de Linus
Pauling, é 1s2
2s2
2p6
3s2
3p6
4s2
3d3
.
A nitroglicerina é um líquido oleoso de cor amarelo-pálida. É altamente sensível ao choque. O simples ato de balançar o líquido pode causar a explosiva decomposição em gases de nitrogênio, dióxido de carbono, água e oxigênio. A equação química abaixo representa essa reação.
4C3H5N3O9 (l ) → 6N2 (g ) + 12CO2 (g ) + 10H2O (g ) + O2 (g )
Calcule o volume de gases CO2 produzido quando uma amostra de 200 gramas de nitroglicerina é detonada. Considere os seguintes dados: Massa g/mol: H = 1; C = 12; N = 14; O = 16; Constante universal dos gases: R = 8,2 · 10−2 atm · L · K−1 · mol−1; Pressão: 1 atm; Temperatura: 27°C e Volume Molar: 22,4 L . mol-1.
Mediante análise, marque a alternativa que apresenta corretamente o volume aproximado.
O aciclovir é um antiviral utilizado no tratamento de infecções por herpes. Ele foi desenvolvido racionalmente pelos pesquisadores George Hitchings e Gertrude Elion, contemplados com Prêmio Nobel por essa descoberta. O aciclovir foi sintetizado a partir da guanina (A), gerando o composto (B). O Composto (C) reage gerando (D). O intermediário (B) reage com a cadeia lateral (D) na presença de ácido para-toluenosulfônico, para formar o derivado (E). O derivado reage à temperatura ambiente para fornecer o produto aciclovir (F).
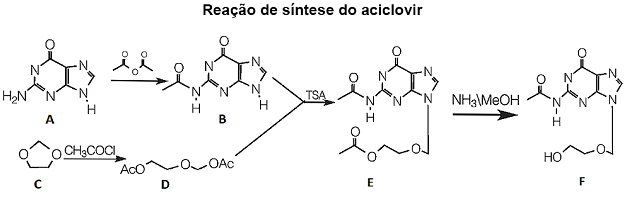
Disponível em: <http://qnesc.sbq.org.br/online/cadernos/03/sintese.pdf> )
É natural buscar a formação de classes ou grupos em função de interesses ou características comuns. Em se tratando de elementos químicos, a busca por agrupamentos com base em determinadas propriedades atômicas resultou no que se conhece hoje como a Tabela Periódica. Como consequência, tornou-se possível sistematizar, por exemplo, o conhecimento relativo às propriedades químicas e físicas dos elementos.
Sobre a propriedade do elemento Rádio (Ra) é correto afirmar que ele é o
Os elementos A, B e C têm as seguintes configurações eletrônicas em suas camadas de valência:
A — 3S1
B — 4s2 4p4
C — 3s2
Com base nessas informações, assinale a opção correta.