Questões de Farmácia - Controle de Qualidade Industrial para Concurso
Foram encontradas 961 questões
Acerca dessa situação hipotética, julgue o item que se segue.
Uma amostra submetida à diluição prévia de 400 vezes com valor de absorvância de 7,7 possui 100% do teor esperado do ativo.
Acerca dessa situação hipotética, julgue o item que se segue.
Uma amostra para doseamento pode ser preparada, fazendose duas diluições sequenciais de 1:10 em solvente apropriado.
Acerca dessa situação hipotética, julgue o item que se segue.
O medicamento de 30 mL possui 600 mg de ativo.
Acerca dessa situação hipotética, julgue o item que se segue.
O limite de quantificação da metodologia citada é de 5,0 μg/mL.
Acerca dessa situação hipotética, julgue o item que se segue.
A maior absorvância que pode ser obtida dentro dos limites da linearidade da metodologia é 15,2.
Existem diversos níveis de inativação microbiana. Para as tecnologias de tratamento de resíduos de serviços de saúde, é necessário atingir pelo menos o nível 3, com inativação de bactérias vegetativas, fungos e vírus lipo-fílicos e hidrofílicos, parasitas e micobactérias, com uma redução maior ou igual a 6 Log10, e inativação de esporos de Bacillus stearothermophilus ou Bacillus subtilis, com uma redução maior ou igual a 4 Log10.
(Environment Protection Agency Guidance for Evaluating Medical Waste Treatment Technologies. Safe management of waste from health-care activities: emerging and other communicable diseases, surveillance and control. EPA – U. S. Environment Protection Agency, 1999. Adaptado)
Em relação ao texto, é correto afirmar que
Sobre os métodos para melhoria da solubilidade do fármaco, analise as afirmativas a seguir. I. Co-solvência e controle do pH. II. Utilização de solventes não-aquosos como óleos voláteis e dimetilsulfóxido para formulações de uso oral. III. Adição de tensoativos e complexação do fármaco.
Está correto o que se afirma em
I. O estudo de exatidão tem o objetivo de verificar a recuperação de um analito em concentrações diferentes dentro de uma matriz, a partir de, no mínimo, 7 determinações. II. O estudo de reprodutibilidade deve ser obtido por meio da proximidade dos resultados obtidos no mesmo laboratório para atingir um critério comum. III. O limite de detecção deve ser demonstrado pela obtenção da menor quantidade do analito presente em uma amostra que pode ser detectado.
Está correto o que se afirma em
( ) Os métodos analíticos descritos em compêndios oficiais, deve ter a sua adequabilidade demonstrada por meio de estudos de validação parcial; ( ) É permitida a contratação de um laboratório terceirizado para realizar a caracterização de substancias de referência, devendo estar de acordo com a Resolução e a justificativa de escolha; ( ) A resolução determina que a faixa de trabalho para a validação dos métodos propostos, devem possuir níveis aceitáveis, de linearidade, exatidão e precisão.
As afirmativas são, na ordem apresentada, respectivamente,
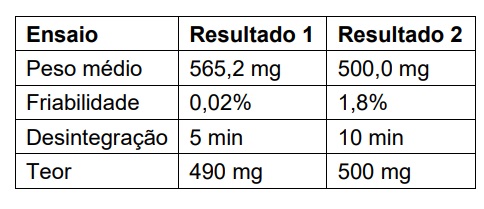
De acordo com os ensaios apresentados e o que preconiza a Farmacopeia Brasileira, analise os resultados 1 e 2 e assinale a alternativa correta.