Questões de Concurso
Comentadas sobre equilíbrio químico em química
Foram encontradas 301 questões
Considerando essas informações e que a viragem do indicador fenolftaleína ocorra na faixa de pH entre 8,2 e 9,8, julgue o item que se segue.
No ponto de viragem da fenolftaleína, durante a titulação que envolve as soluções de NaOH e HCℓ , haverá um pequeno excesso de NaOH em relação ao HCℓ .
Considerando que as constantes de ionização ácida do H2S (Ka1 e Ka2) sejam iguais a 1,0 × 10-7 e 1,0 × 10-13, que o produto de solubilidade (Kps) do CdS seja igual a 1,0 × 10-27 e que todas as soluções envolvidas apresentem comportamento ideal, julgue o item a seguir.
Em uma solução que contenha íons Cd2+ na concentração
1,0 × 10-5
mol/L, uma concentração de íons S2- igual a
1,0 × 10-20 mol/L será suficiente para iniciar a precipitação do
CdS.
Considerando que as constantes de ionização ácida do H2S (Ka1 e Ka2) sejam iguais a 1,0 × 10-7 e 1,0 × 10-13, que o produto de solubilidade (Kps) do CdS seja igual a 1,0 × 10-27 e que todas as soluções envolvidas apresentem comportamento ideal, julgue o item a seguir.
Em uma solução aquosa de H2S, a ordem
decrescente de concentração das espécies presentes
é [H2O] > [H3O+
] > [H2S] > [S2- ] > [HS- ].
Considerando que as constantes de ionização ácida do H2S (Ka1 e Ka2) sejam iguais a 1,0 × 10-7 e 1,0 × 10-13, que o produto de solubilidade (Kps) do CdS seja igual a 1,0 × 10-27 e que todas as soluções envolvidas apresentem comportamento ideal, julgue o item a seguir.
A concentração de íons S2- em uma solução aquosa de H2S
0,100 mol/L é inferior a 1,0 × 10-10.
Álcoois são de grande versatilidade do ponto de vista sintético, pois podem participar de uma série de reações. Exemplos dessa versatilidade são mostrados nas reações não balanceadas nas quais apenas o produto principal é mostrado:
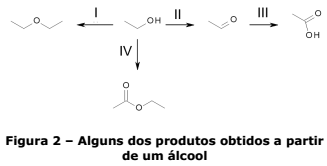
Sobre essa reação e os compostos nela
envolvidos, assinale a alternativa INCORRETA.
Devido à grande emissão de gases lançados na atmosfera, nas regiões mais populosas é evidente a ocorrência da chuva ácida. Na sua precipitação, um dos ácidos responsáveis pela acidez é o sulfúrico. Um equilíbrio envolvido na formação desse ácido na água da chuva está representado pela equação:
2SO2(g) + O2(g) ⇌ 2SO3(g)
Considere que são colocados 6 mol de SO2, 5 mol de O2 e 4 mol de SO3 num recipiente fechado de 5,0 L para reagirem até o sistema atingir o equilíbrio a dada temperatura. A variação do número de mol dos gases participantes está registrada no gráfico.
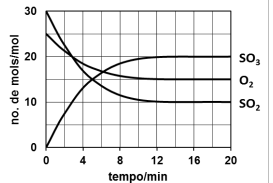
Nestas condições, a constante de equilíbrio, KC, é
igual a:
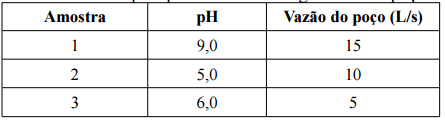
Sendo assim, o pH resultante desta mistura será:
Sabões são sais de sódio ou potássio de ácidos graxos, obtidos pela reação de gorduras e óleos (triglicerídeos) com NaOH, KOH ou Na2CO3. A reação de saponificação é representada a seguir:
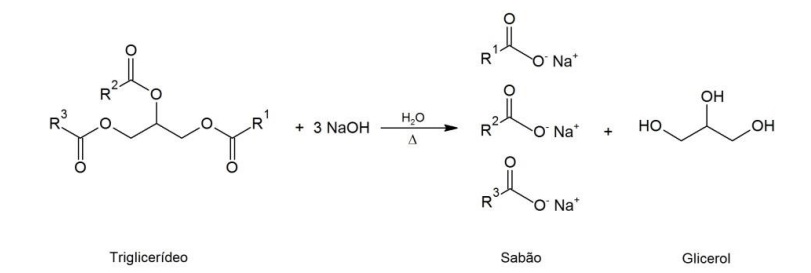
em que R1 , R2 e R3 são cadeias lineares saturadas ou insaturadas, geralmente com doze ou mais átomos de carbono.
Com base nessas informações, considere as seguintes afirmativas:
1. Uma solução aquosa de sabão puro apresenta pH < 7.
2. Adição de ácido forte a uma solução de sabão acarreta precipitação de ácidos graxos.
3. Ca(OH)2 não pode ser usado na obtenção de sabão, pois sais de cálcio de ácidos graxos são insolúveis em água.
4. A obtenção de sabão com Na2CO3 segue a mesma estequiometria que no uso do NaOH.
Assinale a alternativa correta.
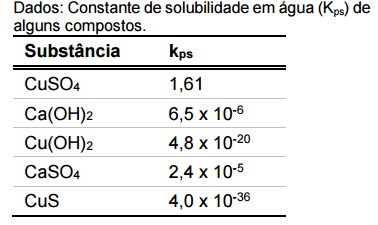
A calda bordalesa, muito utilizada como fungicida na agricultura, é preparada pela mistura de sulfato de cobre pentaidratado (CuSO4.5H2O), um pequeno excesso de cal (CaO) e água em proporção de 1:1:10 (m:m:v), respectivamente, obtendo-se uma suspensão muito fina (partículas pequenas).
De acordo com os dados de constante de solubilidade, assinale a alternativa que apresenta o constituinte principal do sólido suspenso na calda bordalesa.
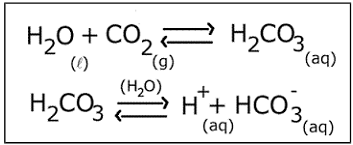
O aumento no pH sanguíneo resulta
Em um recipiente, à temperatura constante, ocorre o seguinte equilíbrio, cuja reação não se encontra balanceada:

Irá provocar deslocamento do equilíbrio, no sentido da
formação de produtos, a: