Questões de Química - Grandezas: massa, volume, mol, massa molar, constante de Avogadro e Estequiometria. para Concurso
Foram encontradas 964 questões
Um acidente ambiental provocou a contaminação das águas de um estuário com chumbo. Uma amostra de 200,0 mL foi coletada para análise e todo o chumbo foi precipitado na forma de PbSO4 devido ao tratamento da amostra com ácido sulfúrico. Sabendo que a massa obtida de PbSO4 foi 6,06 mg, qual é a concentração de chumbo na amostra, em mg/L?
Massas molares (g/mol): O = 16; S = 32; Pb = 207.
O ácido monoprótico, representado por HX, é misturado com excesso de Ba(OH)2 , reagindo segundo a equação abaixo.

Foram obtidos 15,00 g do produto BaX2 que foram quantitativamente reagidos com exatamente 59,00 mL de uma solução aquosa de ácido sulfúrico 1,00 mol L-1 , como mostrado na equação abaixo.
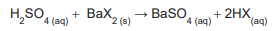
A partir dos dados do experimento, calculou-se a massa
molar de HX, em g mol -1
, e concluiu-se que era de 
Um volume de 1,00 mL de um adoçante líquido à base de sacarina sódica (representada por SacNa) foi colocado num Erlenmeyer, onde também se adicionou 100 mL de água pura. A sacarina sódica reagiu exatamente com 22,00 mL de uma solução padronizada de AgNO3 (0,500 mol L-1 ) para precipitar quantitativamente a sacarina, conforme equação abaixo. No resultado, já se considerou a correção do branco.
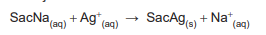
A concentração de sacarina, em g mL-1
, no adoçante, é
mais próxima de
O íon chumbo pode ser determinado por gravimetria, na forma de cromato de chumbo (PbCrO4(s)), usando agente de
precipitação homogênea. Isso é alcançado pela adição de excesso de cloreto de cromo (III), que produz o íon cromato ao
ser oxidado pelo bromato (BrO3 -), também adicionado em excesso. A sequência resumida de reações é indicada abaixo:
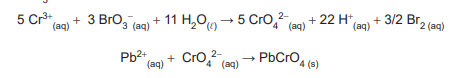
Uma alíquota de 60,000 g de resíduo foi totalmente dissolvido e submetido ao procedimento analítico gravimétrico em questão. A massa de 12,542 g de precipitado (após secagem até massa constante) foi obtida.
A percentagem (m/m) de chumbo presente na amostra foi de