Questões de Concurso
Sobre sistemas homogêneos: constantes: kc e kp. deslocamento do equilíbrio: fatores. em química
Foram encontradas 254 questões
Um frasco contém uma mistura em equilíbrio de X2(g) e X atômico, segundo a reação:
X2(g) ⇌ 2 X(g)
A pressão de equilíbrio encontrada foi de 2,4 atm em certa condição de temperatura e volume. Se X2 gasoso a
uma pressão parcial de 3 atm for adicionado à mistura em equilíbrio acima, a volume e temperatura constantes,
a nova pressão de equilíbrio será de 5,66 atm, sendo que, no processo, a pressão do X (g) atômico aumenta
65% em relação ao valor da condição inicial. Nestas condições, assinale a opção que mostra O VALOR MAIS
PRÓXIMO DE Kp para a decomposição de X2(g), na mesma temperatura:
Figura: Curvas dos valores de frações em mol para: ácido carbônico - linha pontilhada; bicarbonato - linha tracejada; carbonato - linha sólida.
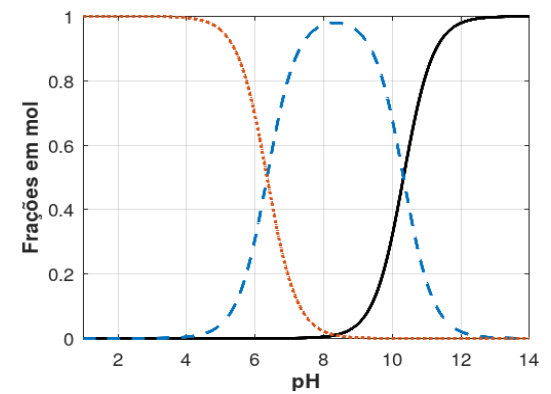
A partir das informações acima e sabendo que o Kps (constante produto de solubilidade) do CaCO3(s) (Calcita) é 4,5 x 10-9 , a 25°C , assinale a opção que mostra o valor aproximado da SOLUBILIDADE MOLAR deste carbonato, em pH 10: Dados eventualmente necessários:√4,5 = 2,12; √6,25 = 2,5; √3 = 1,73; √5 = 2,24; √10 = 3,16; √20 = 4,47.
Diante dessas informações, assinale a opção que mostra O VALOR DA CONSTANTE DE EQUILÍBRIO, Kp, para a reação de dimerização e a afirmação CORRETA que expressa a influência da pressão (FAVORECE OU DESFAVORECE) na dimerização:
Assinale a opção que indica o valor da constante de equilíbrio em função das pressões.
N2O(g) + O3(g) ⇌ N2O4(g) K = 4,4 × 102
Num sistema em equilíbrio, as concentrações de O3 e N2O4 são, respectivamente, 6,4 x 10-3 mol L-1 e 0,25 mol L-1. Qual é o valor da concentração de N2O?
Hb(aq) + O2(aq) ⇌ HbO2(aq)
Nesse sentido, alpinistas precisam passar algum tempo em acampamentos a grandes altitudes antes de prosseguir na subida, mantendo assim a homeostase da concentração de oxigênio no sangue, para que:
Um aumento de pressão no sistema onde ocorre a reação II favorece a decomposição do gás AB.
Representando-se por Kc e Kp as constantes de equilíbrio em termos de concentração e pressão, respectivamente, e considerando-se a constante universal dos gases ideais (R) igual a 0,082 atm∙L∙mol−1∙K−1, é correto afirmar que, para a reação I, com Kc = 30 a 573 K, tem-se Kc < Kp .
Considere-se que, processando-se a reação I em um recipiente fechado de 2 L na temperatura T1, o equilíbrio tenha sido atingido com 1 × 10−2 mol de A2, 2 × 10−2 mol de B2 e 4 × 10−2 mol de AB. Assim, caso a temperatura seja alterada para T2, na qual a constante de equilíbrio seja igual a 40, é correto afirmar que, a partir da condição de equilíbrio anterior, a reação favorecida será a inversa, no sentido da formação dos reagentes A2 e B2.
A relação entre as duas constantes de equilíbrio é K2= K1−2.
O ácido fosfórico é um reagente amplamente utilizado nas indústrias alimentícias, têxtil e metalúrgica. Na fabricação de fertilizantes, o H3PO4 também é frequentemente empregado na produção de superfosfatos. Em laboratórios de análises químicas, o H3PO4 é frequentemente utilizado para o preparo de soluções aquosas destinadas à realização de um grande número de procedimentos. Esse ácido se dissocia em água de acordo com as seguintes reações de hidrólise:
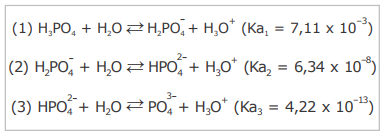
A partir das reações demonstradas acima, considere as seguintes afirmativas.
I - A partir da dissociação do H3PO4, três bases conjugadas são formadas na solução em equilíbrio químico.
II - A etapa (3) de dissociação libera a maior concentração de íons hidrônio (H3O+) na solução em equilíbrio químico.
III - A concentração do ânion 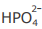 é maior que a concentração do ânion
é maior que a concentração do ânion 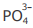 na solução em equilíbrio 4
químico.
na solução em equilíbrio 4
químico.
IV - A concentração do ânion 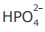 é maior que a concentração do ânion
é maior que a concentração do ânion 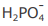 na solução em equilíbrio químico.
na solução em equilíbrio químico.
Estão corretas
(COSTA, T.S. et al. Confirmando a esterificação de Fischer por meio dos aromas. Química Nova na Escola, n. 19, p. 36-38, Maio de 2004).
Na esterificação de 1 mol de ácido acético com 1 mol de álcool etílico num recipiente de 1 litro, a 25 °C, o equilíbrio é atingido com constante de equilíbrio igual a 4. Dessa forma, qual a quantidade em mols do éster presente no equilíbrio?
O dióxido de nitrogênio (NO₂ ) é uma molécula intermediária na produção industrial de ácido nítrico (HNO₃ ), que é muito aplicado na produção de fertilizantes. O dióxido de nitrogênio existe em equilíbrio com o tetróxido de nitrogênio (N₂O₄ ), segundo a reação:
2NO₂(g) ⇄ N₂O₄(g) ∆H = −57,23 kJ/mol
Para aumentar o rendimento do dióxido de
nitrogênio na reação, segundo o princípio de Le
Châtelier, deve-se:
