Questões de Concurso
Sobre soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais. em química
Foram encontradas 1.244 questões
Ao misturar 175 mL de etanol puro com água até alcançar o volume desejado de 250 mL, a solução obtida será de etanol 70% v/v.
Em relação aos conceitos de mol, massa molar e concentração de soluções, julgue o item.
Se 4,0 g de NaOH forem solubilizados em 1.000 mL, a concentração teórica da solução será 0,1 mol/L.
A adição de 5 g de soluto em 250 mL de solvente produz uma solução 2% m/V.
“Para o preparo de uma solução de 1 litro de álcool a 70%, a partir de álcool a 95%, são necessários, aproximadamente, ______”.
Assinale a alternativa que preencha corretamente a lacuna.
“Para preparar um litro de formaldeído a 10% a partir da solução comercial a 37% deve-se utilizer _____ ml de formol a 37% para_____ ml de água destilada.”
Assinale a alternativa que preencha correta e respectivamente as lacunas.
Fonte: https://brasilescola.uol.com.br/quimica/Acido-cloridrico.htm (adaptado) acessado 21/09/2023.
Para o teste de bioacessibilidade, um técnico preparou uma solução diluída desse ácido, com concentração 1,0.10 − 8 mol. L− 1. Essa solução apresenta pH, aproximadamente, igual a
Fonte: https://brasilescola.uol.com.br/quimica/gravimetria.htm (adaptado) acessado 21/09/2023.
Uma alíquota de 50 mL de uma solução de ácido sulfúrico reagiu totalmente com uma solução de cloreto de bário, formando 9,32 g de um precipitado branco. Qual a concentração da solução de ácido sulfúrico?
6 Fe2+ (aq) + Cr2 O7 2+ (aq) + 14 H+ → 6 Fe3+ (aq) + 2 Cr3+ (aq) + 7 H2 O(l)
Com base nessas informações, a quantidade, em mol, de Fe2+ na solução de amostra é
A amostra reagiu com uma solução de íons oxalato em excesso, acarretando a precipitação de MgC2 O4 , conforme apresentado na reação I. Considere que o magnésio foi o único componente da amostra a precipitar.
Em seguida, o precipitado foi filtrado, lavado e calcinado (reação II), gerando uma amostra sólida de 3,05 g.
Reação I: Mg2+ (aq) + C2 O4 2- (aq) → MgC2 O4 (s)
Reação II: MgC2 O4 (s) → MgO (s) + CO (g) + CO2 (g)
A concentração, em g L-1, de magnésio na amostra é
Dado massas molares: Mg = 24 g mol-1 , O = 16 g mol-1 , C = 12 g mol-1
Nessa análise, a absortividade do analito, em L g-1 cm-1 , é
A concentração, em g L-1 , de hidróxido de potássio na solução comercial correspondeu a, aproximadamente,
Dado massas molares: K = 39 g mol-1, H = 1 g mol-1, O = 16 g mol-1
A massa, em gramas, de soluto a ser empregada no preparo dessa solução corresponde a
Dado massas molares: Ca = 40 g mol-1 Br = 80 g mol-1
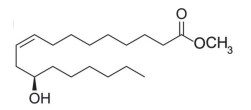
De acordo com as regras de nomenclatura da IUPAC, o nome do ricinoleato de metila é
Coluna 1 1. Densidade. 2. Concentração comum. 3. Normalidade.
Coluna 2
( ) Corresponde à relação entre a massa do soluto e o volume da solução. Pode ser expressa em g/L.
( ) É uma importante propriedade física da matéria, correspondendo à relação entre a massa da solução e o volume da solução. Pode ser expressa em g/cm³.
( ) É a relação entre o equivalente-grama do soluto (eg) e o volume da solução (em litros, por exemplo).
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
I. Mistura de acetona e água.
II. Cloreto de sódio dissolvido em água.
III. Carbonato de bário sólido em água.