Questões de Concurso
Comentadas sobre termodinâmica: energia interna, trabalho, energia livre de gibbs e entropia em química
Foram encontradas 82 questões
Considere as três reações abaixo:
(1) Ca(s) + ½O2 (g) ⇋ CaO(s)
(2) C12H22O11(s) + 12O2 (g) → 12CO2 (g) + 11H2 O(l)
(3) N2
(g) + 3H2
(g) → 2NH3
(g)
Sobre os valores esperados da variação da
entropia padrão das reações (∆r
S°), podemos dizer que:
Note que a absorvância não é uma quantidade medida diretamente, mas é obtida por meio de cálculo matemático a partir dos valores de transmitância.
Assinale a opção que apresenta a relação matemática que define corretamente a absorvância.
A variação de energia livre relacionada à reação de combustão do etanol, apresentada pela equação a seguir, é mais próxima do comportamento descrito pela seguinte letra (correspondente no gráfico):
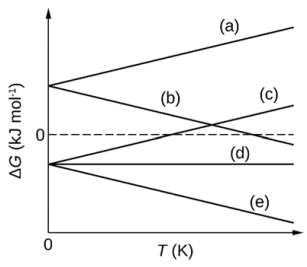
C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(g)
Se a ANM se comportar como um vaso perfeitamente adiabático, não ocorrerá trocas de calor entre ela e o meio externo.
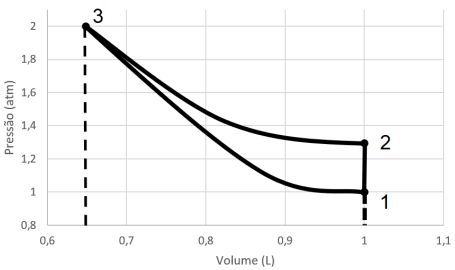
I. A variação de entropia ao longo do ciclo é nula. II. A variação de trabalho ao longo do ciclo é nula. III. A variação de energia interna ao longo do ciclo é nula.
Assinale
Pedro mora em Campos do Jordão, cidade situada a cerca de 1600m de altitude. Ao visitar sua tia que mora em Praia Grande, no litoral, aqueceu água para preparar café.
Pedro observou que a temperatura de ebulição da água na Praia Grande é _____________ ele observa na ebulição da água em Campos do Jordão, pois em maior altitude, a pressão atmosférica _____________.
As lacunas são preenchidas, correta e respectivamente, por:
No fenômeno de transferência de massa para uma mistura gasosa binária formada pelos gases A+B, o fluxo molar do componente A na direção z (NA, mol.s-1.m-2) pode ser calculado pela expressão:
NA=NA+NBNA. zDAB . c. ln [(NA+NBNA)−(ccA1)(NA+NBNA)−(ccA2)]
Essa equação é aplicada para difusão na direção de z com NA e NB constantes e em estado estacionário. Nesse contexto, assinale a opção CORRETA.
A primeira lei da termodinâmica define a conservação da energia, e a segunda lei estabelece os fundamentos para a compreensão da espontaneidade dos fenômenos na natureza. A grandeza central na qual a segunda lei é estabelecida é a
2 POCl3(g) → 2 PCl3(g) + O2(g)
Nas condições-padrão a 298 K, a variação de entalpia (ΔH0 ) e a variação de entropia (ΔS 0 ) para esse processo valem, respectivamente, 572 kJ e 179 J/K. A partir das informações apresentadas, analise as afirmações a seguir.
I. O processo de decomposição do cloreto de fosforila é endotérmico. II. O processo leva à diminuição da desordem do sistema. III. O processo é não-espontâneo nas condições-padrão.
Está correto apenas o que se afirma em
Considerando-se a usina como um sistema termodinâmico, nele ocorre um processo
Esse processo químico
Nessas condições, o valor da energia livre de Gibbs padrão da reação, em kJ mol-1, é mais próximo de
Dado
Constante de Faraday (F) = 96500 C mol-1
Em um equipamento de proteção radiológica, uma peça de 0,7 kg de chumbo tem sua temperatura elevada de 30ºC para 70ºC ao receber uma determinada quantidade de calor.
Sendo o calor específico do chumbo igual a 130 J kg-1
K-1
,
a quantidade de calor, em joules, recebida pela peça é
igual a
No que se refere à entropia e ao terceiro princípio da termodinâmica, julgue o item seguinte.
Para um sistema irreversível, a entropia pode ser escrita,
matematicamente, como a quantidade de calor dividida pela
temperatura.
No que se refere à entropia e ao terceiro princípio da termodinâmica, julgue o item seguinte.
Considere que um molde de aço de 40 g, com capacidade
calorífica à pressão constante cp = 0,5 kJ · kg−1
· K−1
,
inicialmente a 450 ºC, tenha sido resfriado em um óleo com
capacidade calorífica à pressão constante
cp = 2,5 kJ · kg−1
· K−1
, inicialmente a 25 ºC. Nessa situação,
a variação de entropia será superior a +16 kJ/K,
considerando-se a ausência de perdas térmicas.
Com relação à espontaneidade e ao segundo princípio da termodinâmica, julgue o item que se segue.
Reações químicas espontâneas têm maior probabilidade de
ocorrência em sistemas isentrópicos.
Com relação à espontaneidade e ao segundo princípio da termodinâmica, julgue o item que se segue.
Em sistemas reais, o balanço de entropia é um fator
importante no cálculo dos trabalhos real e ideal.
Com relação à espontaneidade e ao segundo princípio da termodinâmica, julgue o item que se segue.
Uma reação química com variação de entropia negativa e
variação de entalpia positiva é espontânea.