Questões de Concurso
Sobre transformações químicas: elementos químicos, tabela periódica e reações químicas em química
Foram encontradas 1.169 questões

É correto APENAS o que se afirma em
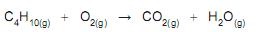
A massa de butano, em gramas, que mais se aproxima do valor que dá origem a 67,2 L de CO2 , nas condições normais de temperatura e de pressão, e considerando o comportamento de gás ideal (no qual o volume molar é igual a 22,4 L), é
Na comparação de dois átomos, tem-se que o raio atômico do
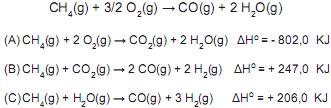
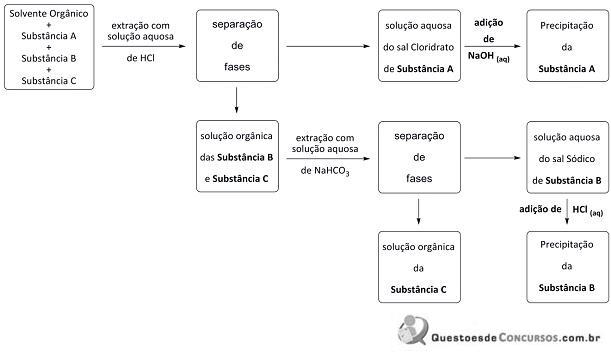
Sabendo que os valores de Ka do ácido clorídrico (HCl) e Ka do bicarbonato de sódio (NaHCO3 ) medidos em água são respectivamente 1,0 x 107 e 4,7 x 10-11 , podemos afirmar que a ordem crescente de valores de Ka das Substância A, Substância B e Substância C deve ser:
O enxofre
A partir das informações do texto, é correto concluir que a reação AgCL(s) → Ag(s) + ½ CL2(g) é catalisada por luz ultravioleta.
Sabendo-se que o sódio e o cloro estão no mesmo período da Tabela Periódica e que o sódio pertence ao grupo 1 e o cloro, ao grupo 17, é correto concluir que a energia de ionização do cloro é superior à do sódio.
A massa de óxido de cálcio, em kg, e o volume de dióxido de carbono, em L, medidos nas condições normais de temperatura e pressão, produzidos pela pirólise de uma tonelada de carbonato com um grau de pureza de 50%, são, respectivamente, iguais a
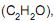 o volume de dióxido de carbono gasoso produzido, nas condições normais de temperatura e pressão, quando 126,0 gramas de etileno reagem com excesso de oxigênio, em L, é igual a
o volume de dióxido de carbono gasoso produzido, nas condições normais de temperatura e pressão, quando 126,0 gramas de etileno reagem com excesso de oxigênio, em L, é igual aPb(NO3)2(aq) + Na2SO4(aq) → PbSO4(s) + 2NaNO3(aq)
A quantidade máxima de sulfato de chumbo II que pode ser obtida a partir da reação de 6,62 g de Pb(NO3)2 com Na2SO4 em excesso é, aproximadamente, em g, igual a Dados: M(Pb(NO3)2) = 331 g/mol M(PbSO4) = 303 g/mol
I - O que caracteriza a reação, em meio aquoso, de um ácido com uma base é a formação de H2O.
II - O oxigênio nos peróxidos possui número de oxidação 1-, exceto no H2O2.
III - O dióxido de carbono, CO2é um óxido que reage com água, formando ácido carbônico.
É correto APENAS o que se afirma em
A tabela periódica foi desenvolvida a partir da segunda metade do século XIX e permitiu sistematizar os conhecimentos sobre as propriedades dos elementos químicos. Ao longo dos anos, diversas versões foram formuladas, até se chegar ao modelo atual, apresentado ao final desta prova objetiva.
Com relação à estrutura atômica dos elementos químicos, à tabela periódica e à construção dessa tabela, julgue os itens que se seguem.
Os elementos químicos pertencentes ao grupo dos halogênios caracterizam-se por serem os que apresentam as mais elevadas energia de ionização e eletronegatividade.


