Questões de Concurso
Sobre transformações químicas em química
Foram encontradas 1.966 questões
Na figura a seguir é esboçado o gráfico do fator de compressibilidade dos gases genéricos A e B, em função da pressão, sob temperatura ambiente.
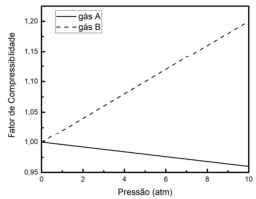
Em relação ao gás A, sob temperatura ambiente e na faixa de
pressões mostrada, o gás B apresenta
No que se refere às ligações químicas, à geometria molecular e a assuntos correlatos, julgue o item.
Os pares eletrônicos da camada de valência do átomo
central de uma molécula tendem a se orientar de forma
que sua energia total seja máxima, ou seja, os pares de
elétrons ficam tão distantes quanto possível do núcleo
e, ao mesmo tempo, ficam o mais próximo possível entre
si, a fim de maximizar as repulsões intereletrônicas.
Acerca da estrutura atômica da matéria e dos métodos de separação e de composição das misturas, julgue o item.
As aplicações de novas estruturas químicas permanecem
desafiadoras. Assim, é possível a construção de novos
arranjos de átomos que, possuindo propriedades
particulares interessantes, terão aplicações ainda não
previstas.

A queima de 46 kg de tolueno, em uma reação de combustão completa, produz mais de 150 kg de gás carbônico.
( ) Afinidade eletrônica é a quantidade de energia requerida para tirar um elétron da camada de valência de um átomo em seu estado eletrônico fundamental e no estado gasoso.
( ) Energia de ionização é definhada como a variação de energia que ocorre quando um elétron é adicionado a um átomo no estado gasoso, formando um íon negativo. Os halogênios possuem os maiores valores de energia de ionização, justamente por necessitarem de um elétron para completar o octeto, ficando com a configuração de gás nobre.
( ) Eletronegatividade é a capacidade que um átomo possui de atrair os elétrons envolvidos em uma ligação química. Os valores de eletronegatividade são baseados em outras propriedades dos átomos, inclusive a energia de ionização, portanto, elementos com baixa energia de ionização exibirão baixa eletronegatividade.
( ) O raio atômico representa a medida entre o núcleo e a camada de valência do átomo. Os raios atômicos diminuem em uma mesma família da tabela periódica e a diminuição é bastante pronunciado para os metais alcalinos. Ele é inversamente proporcional à eletronegatividade porque quanto ´menor for a força que o núcleo atrai a eletrosfera, maior é o raio.
Assinale a alternativa que apresenta a sequência correta de cima para baixo.
Sabendo-se que o volume inicial era 120L, o volume final é de cerca de:
Quando se passa a estudar gases reais, usa-se o modelo que insere um fator de compressibilidade, ou a equação de Van der Waals, que insere termos:
A periodicidade da eletronegatividade na Tabela Periódica sofre influência do efeito de blindagem.
Todos os elementos químicos antigamente classificados como semimetais foram reclassificados como metais.
O modelo de Dalton foi o primeiro modelo atômico quantizado.
A tabela periódica de Mendeleev foi organizada em ordem crescente de massa atômica.
Mendeleev foi o primeiro cientista a organizar os elementos químicos em uma ordem periódica.
Com relação ao assunto do texto anterior, julgue o item seguinte.
O gás hidrogênio é um gás nobre.
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

Em geral, o desvio do comportamento ideal de um gás é mais evidenciado em pressões mais altas e em temperaturas mais baixas.
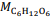 = 180 g/mol e
= 180 g/mol e 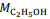 = 46 g/mol.
= 46 g/mol. A química distanciou-se da alquimia a partir dos ensaios de Robert Boyle, um dos primeiros pesquisadores a dar forma científica ao atomismo, opondo-se a Aristóteles e Paracelso.