Questões de Concurso
Sobre transformações químicas em química
Foram encontradas 1.983 questões
Se esse recipiente encontra-se nas condições normais de temperatura e de pressão e se a mistura for considerada uma mistura gasosa ideal, o valor da pressão parcial de amônia é, em atm, de
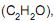 o volume de dióxido de carbono gasoso produzido, nas condições normais de temperatura e pressão, quando 126,0 gramas de etileno reagem com excesso de oxigênio, em L, é igual a
o volume de dióxido de carbono gasoso produzido, nas condições normais de temperatura e pressão, quando 126,0 gramas de etileno reagem com excesso de oxigênio, em L, é igual aPb(NO3)2(aq) + Na2SO4(aq) → PbSO4(s) + 2NaNO3(aq)
A quantidade máxima de sulfato de chumbo II que pode ser obtida a partir da reação de 6,62 g de Pb(NO3)2 com Na2SO4 em excesso é, aproximadamente, em g, igual a Dados: M(Pb(NO3)2) = 331 g/mol M(PbSO4) = 303 g/mol
I - O que caracteriza a reação, em meio aquoso, de um ácido com uma base é a formação de H2O.
II - O oxigênio nos peróxidos possui número de oxidação 1-, exceto no H2O2.
III - O dióxido de carbono, CO2é um óxido que reage com água, formando ácido carbônico.
É correto APENAS o que se afirma em
MnO2 + 4HCl ? MnCl2 + 2H2O + Cl2
Admitindo-se uma pureza de 87% para o dióxido de manganês e um rendimento de reação de 90%, a massa de MnO2 , em g, necessária para produzir 20,16L de gás cloro, medidos a 0 ºC e 1atm, é
(Dados: Massas molares em g/mol: Mn = 55; O = 16; H = 1; Cl = 35,5; Volume molar a 0 ºC e 1atm = 22,4L)
H2CrO4 + NaHSO3 + H2SO4 ? Cr2(SO4)3 + Na2SO4 + H2O
A soma dos coeficientes mínimos desta equação é:
(Dados: Massas molares em g/mol: H2SO4 = 98; NaOH = 40; Mg = 24; Ca = 40; Fe = 56; Zn = 65; Pb = 207)


Com relação ao assunto abordado nos textos, assinale a opção correta.




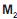 O e MO. Considere as afirmações abaixo sobre esse elemento e seus compostos.
O e MO. Considere as afirmações abaixo sobre esse elemento e seus compostos.I - O elemento M pertence ao grupo dos metais alcali- nos.
II - No composto MO, o oxigênio apresenta estado de oxidação -1.
III - O elemento M apresenta dois estados de oxidação.
IV - No composto
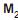 O, o oxigênio apresenta estado de oxidação -2.
O, o oxigênio apresenta estado de oxidação -2.São corretas APENAS as afirmativas