Questões de Concurso Público INB 2018 para Engenheiro Químico
Foram encontradas 9 questões
C6 H12O6 (s) + 6O2 (g) → 6CO2 (g) + 6H2O (g)
Nessas condições, e considerando que os gases são ideais, é correto afirmar que a variação de entalpia da mesma reação é, em quilojoules, aproximadamente igual a:
Dado: Constante dos gases (R) = 8,31 JK–1mol–1
COLUNA I 1. Processos mecânicos 2. Processos físicos 3. Processos biotecnológicos 4. Processos químicos
COLUNA II ( ) Utiliza fungos ou bactérias que produzem enzimas capazes de quebrar as cadeias poliméricas da lignina. ( ) É um processo caro, pois a biomassa passa por processo de moagem, em que há um grande consumo de energia. ( ) Método mais comum para esse processo é o cozimento com hidróxido de sódio e sulfeto de sódio. ( ) O material é aquecido pela passagem de vapor d’água, sofrendo hidrólise.
Assinale a sequência CORRETA.
2H2 (g) + 2NO (g) → N2(g) + 2H2O (g)
Para compreender a velocidade da reação química em função das concentrações dos reagentes, um técnico realizou os seguintes experimentos.
Experimento 1 – Quando dobrou a concentração do gás hidrogênio e reduziu à metade a concentração do óxido nítrico, a velocidade da reação dobrou.
Experimento 2 – Quando quadruplicou a concentração do gás hidrogênio e dobrou a concentração do óxido nítrico, a velocidade da reação química quadruplicou.
A partir dessas informações, é correto afirmar que a expressão matemática da Lei de Velocidade é representada por:
COOH – CHOH – CH2 – COOH → CH3 – CH2 – OH + 2CO2
Em relação ao processo de fermentação do ácido málico, analise as afirmativas a seguir. I. A fermentação ocorre com a diminuição do pH. II. A fermentação ocorre com oxidação do carbono carbonílico. III. Pela ação das bactérias láticas, ocorre a transformação do ácido málico em ácido lático. Estão corretas as afirmativas:
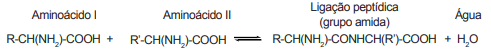 Considere que 2 mols de molécula do aminoácido I são adicionados para reagir com 1 mol de molécula do aminoácido II.
Quando o equilíbrio químico é estabelecido (equilíbrio 1), 20% do aminoácido I é consumido. Em seguida, adicionou-se
certa quantidade de mols de molécula do aminoácido II, e 10% do aminoácido I foi consumido até reestabelecer um novo
equilíbrio (equilíbrio 2).
Nessas condições, qual é a razão aproximada entre o primeiro e segundo equilíbrios?
Considere que 2 mols de molécula do aminoácido I são adicionados para reagir com 1 mol de molécula do aminoácido II.
Quando o equilíbrio químico é estabelecido (equilíbrio 1), 20% do aminoácido I é consumido. Em seguida, adicionou-se
certa quantidade de mols de molécula do aminoácido II, e 10% do aminoácido I foi consumido até reestabelecer um novo
equilíbrio (equilíbrio 2).
Nessas condições, qual é a razão aproximada entre o primeiro e segundo equilíbrios?Considere, em um sistema ideal, que uma chaminé recebeu 2,4 x 1019 moléculas de SO2 que foram misturadas com 10 g do carbonato de cálcio. Nessas condições, quantos miligramas, aproximadamente, de sulfato de cálcio ficariam retidos na chaminé?
