Questões de Concurso Público SEED-PR 2022 para Área de Conhecimento: Química
Foram encontradas 40 questões
Ano: 2022
Banca:
Instituto Consulplan
Órgão:
SEED-PR
Prova:
Instituto Consulplan - 2022 - SEED-PR - Área de Conhecimento: Química |
Q2116722
Química
O composto 1 foi isolado das flores de açafrão (Carthamus
trinctorius) e o composto 2 das folhas e flores do picão (Bidens
pilosa), que possui propriedades antimicrobianas e, quando
irradiada com luz ultravioleta, apresenta atividade contra larvas
de mosquitos e nematoides.
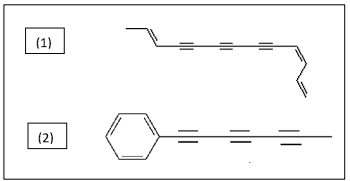
(Barbosa, 2011.)
O nome sistemático dos compostos 1 e 2 são, respectivamente:

(Barbosa, 2011.)
O nome sistemático dos compostos 1 e 2 são, respectivamente:
Ano: 2022
Banca:
Instituto Consulplan
Órgão:
SEED-PR
Prova:
Instituto Consulplan - 2022 - SEED-PR - Área de Conhecimento: Química |
Q2116723
Química
Na ciência moderna, consideramos natural supor que existem
átomos e moléculas. Na verdade, já foi usada a teoria atômica
para explicar algumas das propriedades da matéria. Entretanto, a evidência científica da existência dos átomos é relativamente recente e o progresso da química foi muito lento
antes de essa evidência ser observada. O conceito de átomo
começou há, aproximadamente, 2.500 anos quando filósofos
gregos expressaram a hipótese de que a matéria era composta
de pequenas partículas indivisíveis. Sobre o modelo dos
átomos, marque V para as afirmativas verdadeiras e F para as
falsas.
( ) De acordo com a teoria de Bohr, o elétron do átomo de hidrogênio no estado fundamental pode absorver várias quantidades discretas de energia e, assim, elevar-se a um nível de energia mais alto. ( ) A teoria atômica de Dalton explicou as leis da combinação química propondo que a matéria consiste em átomos indestrutíveis com massas que não mudam no decorrer das reações químicas. ( ) Quando elétrons absorvem ou emitem energia ao passarem de uma órbita eletrônica para outra, a energia é dada pela equação: E = mZ2e 4 . h. ( ) Os raios catódicos são um fluxo de elétrons que se movem em linha reta e são dependentes do material dos eletrodos e do gás residual que existe no tubo.
A sequência está correta em
( ) De acordo com a teoria de Bohr, o elétron do átomo de hidrogênio no estado fundamental pode absorver várias quantidades discretas de energia e, assim, elevar-se a um nível de energia mais alto. ( ) A teoria atômica de Dalton explicou as leis da combinação química propondo que a matéria consiste em átomos indestrutíveis com massas que não mudam no decorrer das reações químicas. ( ) Quando elétrons absorvem ou emitem energia ao passarem de uma órbita eletrônica para outra, a energia é dada pela equação: E = mZ2e 4 . h. ( ) Os raios catódicos são um fluxo de elétrons que se movem em linha reta e são dependentes do material dos eletrodos e do gás residual que existe no tubo.
A sequência está correta em
Ano: 2022
Banca:
Instituto Consulplan
Órgão:
SEED-PR
Prova:
Instituto Consulplan - 2022 - SEED-PR - Área de Conhecimento: Química |
Q2116724
Química
As forças entre as moléculas governam as propriedades físicas
da matéria e contribuem para explicar as diferenças entre as
substâncias que estão a nossa volta. Elas explicam porque o
dióxido de carbono é um gás que exalamos, porque a madeira
é um sólido sobre o qual podemos ficar em pé e porque o gelo
flutua na água. Sobre as forças intermoleculares, analise as
afirmativas a seguir.
I. As interações dipolo-dipolo são mais fracas do que as forças entre íons e diminuem rapidamente com a distância, especialmente nas fases líquida e gás, em que as moléculas estão em rotação. II. O aumento do ponto de ebulição dos gases nobres, do hélio ao xenônio, se deve à energia das interações de London que diminui com o número de elétrons. III. As repulsões entre moléculas são o resultado da superposição de orbitais de moléculas vizinhas e do princípio da exclusão de Pauli.
Está correto o que se afirma em
I. As interações dipolo-dipolo são mais fracas do que as forças entre íons e diminuem rapidamente com a distância, especialmente nas fases líquida e gás, em que as moléculas estão em rotação. II. O aumento do ponto de ebulição dos gases nobres, do hélio ao xenônio, se deve à energia das interações de London que diminui com o número de elétrons. III. As repulsões entre moléculas são o resultado da superposição de orbitais de moléculas vizinhas e do princípio da exclusão de Pauli.
Está correto o que se afirma em
Ano: 2022
Banca:
Instituto Consulplan
Órgão:
SEED-PR
Prova:
Instituto Consulplan - 2022 - SEED-PR - Área de Conhecimento: Química |
Q2116725
Química
A química orgânica originou-se das crenças do século XVIII de que os compostos orgânicos poderiam ser formados apenas pelos seres vivos. Essa ideia foi desmentida em 1828, pelo químico alemão, Friedrich Wöhler, quando sintetizou a ureia, uma substância orgânica encontrada na urina dos mamíferos, por meio do aquecimento de cianeto de amônio, substância inorgânica. Sobre as funções orgânicas, assinale a afirmativa INCORRETA.
Ano: 2022
Banca:
Instituto Consulplan
Órgão:
SEED-PR
Prova:
Instituto Consulplan - 2022 - SEED-PR - Área de Conhecimento: Química |
Q2116726
Química
A periplanona B, feromônio sexual da barata, contém dois
éteres cíclicos em sua estrutura. Esse composto é ativo em
quantidade extremamente baixa, sendo 0,01 g suficiente para
atrair 100 bilhões de baratas. Outro composto natural que
apresenta o grupo éter em sua estrutura é a azadiractina, isolada da árvore Azadirachta indica. Este composto apresenta
potentes atividades nematicida e antialimentar para insetos.
Sobre os éteres, analise as afirmativas a seguir.
I. Nos éteres, o oxigênio apresenta hibridação sp3 e o ângulo entre os grupos ligados ao oxigênio é de, aproximadamente, 110°. II. A solubilidade dos éteres em água diminui com o aumento do número de átomos de carbono. III. As temperaturas de ebulição dos éteres são mais altas que as dos alcanos de massa molar semelhante e bem mais baixa que as dos álcoois de mesma massa molar.
Está correto o que se afirma em
I. Nos éteres, o oxigênio apresenta hibridação sp3 e o ângulo entre os grupos ligados ao oxigênio é de, aproximadamente, 110°. II. A solubilidade dos éteres em água diminui com o aumento do número de átomos de carbono. III. As temperaturas de ebulição dos éteres são mais altas que as dos alcanos de massa molar semelhante e bem mais baixa que as dos álcoois de mesma massa molar.
Está correto o que se afirma em