Questões de Concurso
Foram encontradas 1.519 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
( ) Em contato com ácidos, as bases reagem por reação de neutralização, formando sal e água como produtos.
( ) As bases sofrem ionização em água, liberando íons hidroxila (OH – ).
( ) Na ionização em água, as bases aumentam a concentração de íons (OH – ).
( ) As soluções básicas são caracterizadas por valor de pH acima de 7.
A sequência correta, de cima para baixo é:
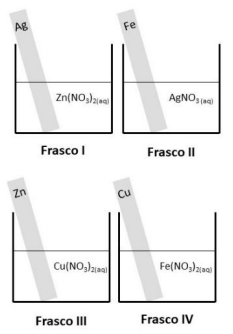
Observe, ainda, a tabela de potenciais padrão de redução (E0).

Durante essa aula experimental os alunos deverão observar evidência de fenômeno químico nos frascos:
Observe a tabela a seguir.
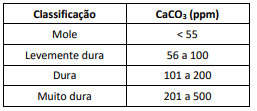
A análise de 120,0g de uma amostra de água de um manancial indicou a presença de 15,0mg de CaCO3. Essa amostra deve classificada como
• Porcentagem em massa: 70 % m/m
• Massa molar: 63 g/mol
• Densidade: 1,4 g/mL
Qual o valor da concentração da solução de ácido nítrico, em mol/L, preparada pelo químico?
Cr2 O72– (aq) + 6 Fe2+ (aq) + 14 H+ (aq) ⇌ 6 Fe3+ (aq) + 2 Cr3+ (aq) + 7 H2O
Com base na reação global dessa titulação, qual o valor mais próximo do percentual de ferro em massa no comprimido?