Questões de Concurso
Foram encontradas 1.661 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O quadro a seguir apresenta as concentrações de cinco soluções ideais obtidas com diferentes solutos totalmente dissociados.
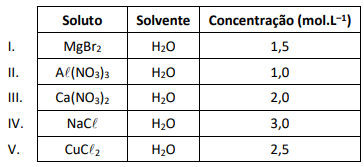
A solução que apresenta a menor pressão de vapor é a
Assinale a opção que indica a concentração de cloreto de sódio nessa água, em ppm.
Com relação às propriedades de tais substâncias, e considerando a teoria de Arrhenius, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Em solução aquosa, ácidos liberam prótons H+ e bases liberam ânions H- . ( ) Quando colocados em água, ácidos sofrem ionização e bases, dissociação iônica. ( ) Os ácidos são líquidos corrosivos e perigosos, por isso não podem entrar em contato com a pele nem ser ingeridos.
As afirmativas são, respectivamente,
2HCl (aq) + CaCO3 (s) → CaCl2 (aq) + H2O (l) + CO2 (g)
Pensando nas condições normais de temperatura e pressão (CNTP), vamos calcular a massa de água, em gramas, e o volume de gás carbônico, que pode se formar a partir de 80g de carbonato de cálcio. Dados as massas atômicas de Ca= 40; C = 12; O=16. Assinale a alternativa que apresenta os valores encontrados.
O Regulamento Técnico SVS/MS nº 540/1997 considera o fermento químico como um aditivo, e como tal, necessita obrigatoriamente ser registrado na ANVISA de acordo com as orientações da Resolução nº 23 (ANVISA, 2000).
Basicamente, os fermentos químicos são constituídos de uma mistura de pirofosfato ácido de sódio, bicarbonato de sódio e fécula de mandioca. Além do conhecido bicarbonato de sódio, assinale a alternativa que apresente alguns ácidos que podem fazer parte da composição.