Questões de Concurso
Foram encontradas 2.902 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Em análises cromatográficas, a separação dos componentes da amostra é efetuada na coluna, em que a natureza do suporte sólido, o método de empacotamento, o comprimento, o diâmetro e a temperatura de operação são fatores importantes para obter-se a resolução desejada, com a respectiva identificação dos componentes pelo detector. Acerca desse assunto, julgue o item subsecutivo.
O espectrômetro de massas, um instrumento analítico que se
baseia nos fenômenos de ionização, é capaz de detectar
compostos presentes, como ultratraços, em nível de
picograma.
Em análises cromatográficas, a separação dos componentes da amostra é efetuada na coluna, em que a natureza do suporte sólido, o método de empacotamento, o comprimento, o diâmetro e a temperatura de operação são fatores importantes para obter-se a resolução desejada, com a respectiva identificação dos componentes pelo detector. Acerca desse assunto, julgue o item subsecutivo.
Em cromatografia gasosa, a análise de ultratraços de metais,
no nível de picograma, requer detectores muito sensíveis,
como a célula de condutividade térmica.
Em análises cromatográficas, a separação dos componentes da amostra é efetuada na coluna, em que a natureza do suporte sólido, o método de empacotamento, o comprimento, o diâmetro e a temperatura de operação são fatores importantes para obter-se a resolução desejada, com a respectiva identificação dos componentes pelo detector. Acerca desse assunto, julgue o item subsecutivo.
Quando a separação cromatográfica é realizada em um modo
de fase normal, a fase estacionária é um hidrocarboneto
apolar; ao passo que, quando é feita em um modo de fase
reversa, a superfície da fase estacionária tem uma
característica polar.
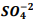 seguindo a reação: BαSO4(s) ⇔
seguindo a reação: BαSO4(s) ⇔ 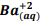 +
+ 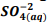 , onde Kps = [ Bα+2] [
, onde Kps = [ Bα+2] [ 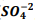 ] = 1, 1 x10−10. Verifica-se que:
] = 1, 1 x10−10. Verifica-se que: I. A partir da concentração de
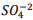 acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10−9 M jáhouve precipitação de BαSO4.
acima de0,025M inicia a precipitação de Ba+2. II. Em concentrações menores que 4,4 x10−9 M jáhouve precipitação de BαSO4. Assinale a alternativa correta:
X KO2(s) + Y CO2(g) ⇔ W K2CO3(s) + Z O2(g).
Calcule a massa de KO2 necessária para reagir com 50 l de CO2 a 25°C e 1,0 atm. A massa molar do KO2 é 71,1 g/mol. Considere o volume molar 24,5l/mol.
Assinale a alternativa que contém os valores de X, Y, W e Z e a massa de KO2 consumida na reação.