Questões de Concurso
Foram encontradas 747 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Com relação aos processos termodinâmicos que envolvem liberação e aproveitamento de energia, julgue o item que se segue.
O poder calorífico de um combustível não pode ser calculado
a partir dos poderes caloríficos de seus componentes.
Com relação aos processos termodinâmicos que envolvem liberação e aproveitamento de energia, julgue o item que se segue.
O calor desprendido em uma reação química é quantificado
pela entalpia de reação, cujo valor independe da temperatura
de reação.
Com relação aos processos termodinâmicos que envolvem liberação e aproveitamento de energia, julgue o item que se segue.
Em um processo termodinâmico cíclico, isto é, que se
origina e termina em um mesmo estado, a variação da
energia interna é nula.
Com relação a gases reais e a desvio da idealidade, julgue o item a seguir.
Na equação do virial, usada na mistura de gases reais, os
coeficientes dependem exclusivamente da temperatura.

A figura precedente mostra o gráfico do coeficiente de compressibilidade (Z) dos gases O2 e CO2 em função da pressão para a temperatura T2. Considerando a situação hipotética apresentada e as informações fornecidas, que a constante universal dos gases seja igual a 0,082 atm × L × mol-1 × K-1 , que a 300 K e 1,00 atm o O2 (g) e o CO2 (g) apresentem comportamento de gás ideal, e que a 300 atm e a uma temperatura T2 o O2 (g) e o CO2 (g) obedeçam a equação de estado de van der Waals expressa como: 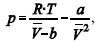 julgue o item que segue.
julgue o item que segue.
A partir do gráfico apresentado, conclui-se que o CO2 (g)
apresenta a constante b na equação de van der Waals inferior
à do O2 (g).