Questões de Concurso
Foram encontradas 8.687 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I - Para algumas moléculas, a TLV considera a excitação de elétrons para um orbital de maior energia durante a formação da ligação química.
II - A TLV considera apenas a sobreposição de orbitais atômicos não hibridizados na formação da ligação sigma (σ).
III - A TLV utiliza o conceito de ressonância para explicar as ligações químicas em determinadas moléculas.
Está correto o que se afirma acima em:
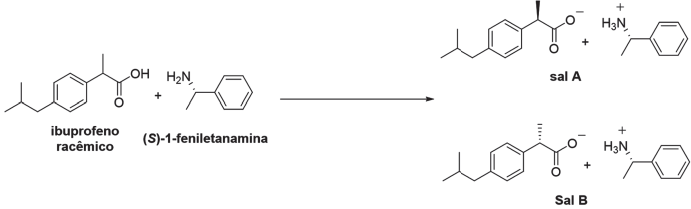
Nesse processo, o(s)
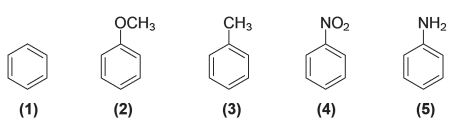
A ordem crescente de reatividade desses compostos em reações de SEAr é
A radiação ionizante apresenta diversos efeitos sobre a saúde humana.
Os efeitos
Considerando-se uma massa inicial de 3,0 g desse radioisótopo, o seu tempo de meia vida e a massa restante após um período de 5 dias são, respectivamente,
Dado: ln2 = 0,692 e-1 = 0,368
Considerando-se comportamento ideal, qual será a pressão, em kPa, quando o cilindro de gás for resfriado a 8º C?
Qual a massa de CO2, em gramas, produzida na combustão completa de 370 mg de varfarina?
Dado: massa molecular da varfarina = 308 g mol-1 massa molecular do CO2 = 44 g mol-1
Abaixo estão representadas quatro estruturas.
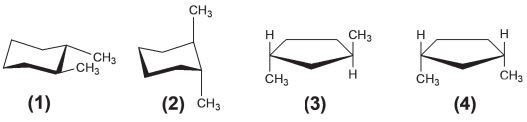
As estruturas
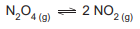
O valor da avaliação de Energia Livre de Gibbs da reação (∆Gr º ) é

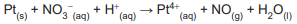
A soma dos coeficientes estequiométricos de reagentes e produtos na reação balanceada é
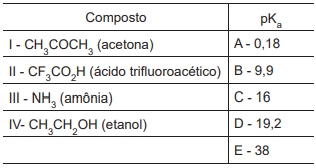
Com base na capacidade de liberar íons H+ em solução, a correta relação entre o composto e seu valor de pKa é:
A hidrólise de ésteres
I - O calor liberado na hidrogenação do benzeno é menor que o liberado na hidrogenação de um trieno não aromático.
II - O benzeno sofre reações de adição de bromo (Br2 ) nas suas duplas ligações.
III - Segundo a Teoria do Orbital Molecular (TOM), o benzeno possui três orbitais moleculares π ligantes preenchidos com elétrons, além de apenas um orbital molecular antiligante.
IV - Por possuir ligações duplas e simples, há ligações carbono-carbono com diferentes comprimentos no benzeno.
Está correto APENAS, o que se afirma em
HARRIS D. C. Análise Química Quantitativa. 6ª edição. Rio de Janeiro: LTC, 2005.
Durante estudo sobre erro do indicador, o analista fez uma titulação de 10,00mL de Ácido fraco (HA) 0,100mol/L (pka = 4,8) com NaOH 0,100mol/L e obteve um volume final de 9,80mL de base. O quadro abaixo apresenta três indicadores e suas faixas de viragem.
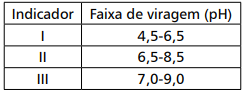
Para que o analista tenha observado esse ponto final, o(s) indicador(es) utilizado(s) foi/foram apenas
Dados: Log 49 = 1,7
SO3(g) +H2SO4(l) → H2 S2 O7(l) (Equação1) H2S2O7(l) + H2O(l) → 2H2 SO4(l) (Equação2)
CAMPOS, R. V. Ácico Sulfúrico. Rev. Virtual Quim. 2011, 3(3), 210-214 (adaptado).
Para a produção do ácido sulfúrico 98% m/m, a indústria partiu de 800kg de SO3 e 980kg de H2SO4, além de água o suficiente para obtenção desse produto. A massa de ácido sulfúrico 98% m/m que se pode obter, em kg, é
Dados: Massa molar: O=16g/mol; H=1g/mol; S=32g/mol
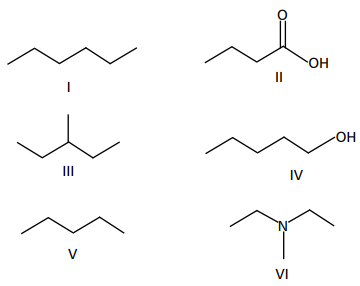
Em relação às propriedades físico-químicas dos compostos, é INCORRETO afirmar que
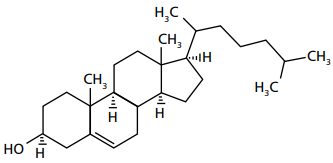
Sobre a estrutura acima, analise se as afirmativas são verdadeiras (V) ou falsas (F):
( ) Apresenta a função fenol. ( ) Apresenta isomeria óptica. ( ) Possui quatro centros de quiralidade. ( ) Possui baixa solubilidade em água. ( ) É um composto meso.
A sequência correta é
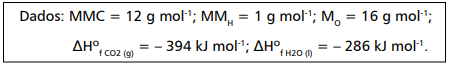
Considerando essas informações, o calor de formação estimado para a glicose, em kJ mol-1, é