Questões de Concurso
Foram encontradas 8.680 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Acerca das cromatografias líquida e gasosa e da espectrometria de massa, julgue o próximo item.
O gráfico a seguir representa corretamente o espectro de massa por ionização por elétrons do íon molecular do composto CH3COCl.
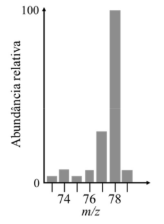
Situação hipotética: Uma amostra contendo apenas metilbenzeno e etoxibenzeno, com coluna de microesferas de zircônia (ZrO2) recoberta com poli(butadieno) foi eluída com acetonitrila a 20% em volume em água. O seguinte gráfico mostra um cromatograma obtido por cromatografia líquida para essa amostra.
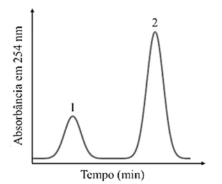
Assertiva: Nesse gráfico, os picos 1 e 2 se referem aos compostos etoxibenzeno e metilbenzeno, respectivamente.
Na cromatografia líquida, em uma separação por partição de fase normal, o soluto menos polar passa proporcionalmente mais tempo na fase estacionária e é o último soluto a eluir da coluna.
Acerca das cromatografias líquida e gasosa e da espectrometria de massa, julgue o próximo item.
Na cromatografia de gás, a fase móvel interage com as
moléculas do analito e, por isso, o gás da fase móvel deve
apresentar alta reatividade e ser escolhido de acordo com as
características do analito.
A diferença entre a espectrometria de absorção atômica (AAS) e a espectrometria de emissão atômica por plasma acoplado indutivamente (ICP-AES) é que a AAS é capaz de quantificar a maioria dos ânions e dos metais, enquanto a ICP-AES é inapropriada para dosagem de ânions.
Considerando-se o gráfico I, que mostra a curva de calibração obtida a partir da leitura da absorbância de determinado analito a 350 nm em diferentes concentrações, e o gráfico II, que ilustra o espectro obtido para uma amostra desse analito nas mesmas condições experimentais usadas para a construção da curva de calibração, é correto afirmar que a concentração do analito na amostra é maior que 15 mg/L.
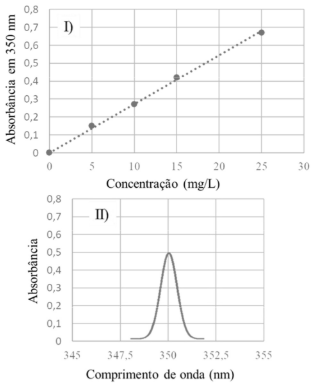
Situação hipotética: A absortividade molar de um analito é igual a 500,0 mol • cm−1 • L−1 quando medida a uma concentração igual a 1,0 × 10−3 mol/L em um espectofotômetro de absorção no ultravioleta visível, em determinado comprimento de onda. Assertiva: Nas mesmas condições experimentais, para que a absorbância seja igual a 0,4, o caminho óptico da cubeta contendo o analito deverá ser maior que 1,0 cm.
O esquema a seguir representa corretamente a montagem de um fotômetro de chama.
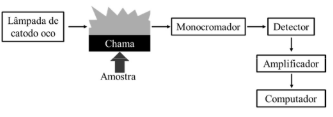
Considerando a espectrofotometria, a fotometria e a colorimetria, julgue o item seguinte.
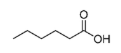
Para a identificação do ácido caproico, cuja estrutura molecular está representada a seguir, a espectrometria de absorção molecular no infravermelho é mais adequada que a espectrometria de absorção molecular no ultravioleta visível.
A absorbância de uma amostra é definida como o inverso da fração de luz que passa por essa amostra.
Quanto maior for a inclinação da curva de calibração, dentro da faixa dinâmica linear, maior será o limite de quantificação (LOQ) de um método.
Em um fotômetro usado para medidas colorimétricas, um filtro é usado após a cubeta, para maximizar a luz absorvida pela amostra.
Na titulação representada pela equação seguinte, o potencial no ponto de equivalência é igual à média aritmética dos potenciais padrão de redução dos dois pares redox envolvidos na reação.
U4+ + 2 Ce4+ + 2 H2O ⇌ UO2 2+ + 2 Ce3+ + 4 H+
Situação hipotética: Um minério contendo magnetita (Fe3O4) foi analisado pela dissolução de uma amostra em HCl concentrado, o que resultou em uma mistura de Fe2+ e Fe3+. Depois de adicionado HNO3 para oxidar o Fe2+ a Fe3+, a solução resultante foi diluída com água e todo o Fe3+ foi precipitado como Fe(OH)3 pela adição de NH4OH. Após filtragem e enxágue, o resíduo foi calcinado, resultando em Fe2O3 puro. Assertiva: Nesse caso, a massa de Fe3O4 presente na amostra é corretamente calculada multiplicando-se por 2/3 a massa de Fe2O3 obtida ao final do processo.
Situação hipotética: Para a determinação da concentração de Cu2+ em uma bebida supostamente contaminada, foi utilizada a volumetria de complexação com EDTA. O álcool de uma alíquota de 100 mL dessa bebida foi evaporado, e o volume novamente completado a 100 mL com água pura. Após ser tamponada a pH 10, essa alíquota de 100 mL foi titulada com 12,5 mL de EDTA 0,004 mol/L. O único metal presente na amostra era o cobre, cuja massa molar é de 63,55 g/mol. Assertiva: Nessa situação, a concentração de cobre na bebida é maior que 25 mg/L.
Situação hipotética: Dois ácidos monopróticos, um forte e um fraco, têm a mesma concentração e o mesmo volume inicial e foram titulados com uma mesma solução de NaOH. O gráfico a seguir mostra as curvas de titulação desses dois ácidos monopróticos.
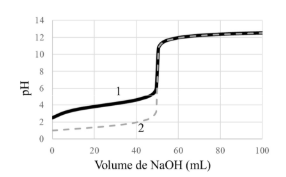
Assertiva: No gráfico, a curva 1 representa a titulação do ácido fraco.
Na titulação de um ácido monoprótico cuja constante de dissociação ácida seja Ka = 1 × 10−4, o indicador ácido-base escolhido terá o melhor rendimento se tiver pKa = 4.
No que concerne a volumetria, gravimetria e potenciometria, julgue o item a seguir.
Situação hipotética: Para padronizar uma solução de NaOH, um químico dissolveu em água 200 mg do padrão primário biftalato de potássio (KHC8H4O4; M = 204,1 g/mol), em um erlenmeyer. A solução resultante foi então titulada usando-se uma bureta e fenolftaleína como indicador. Foram consumidos 5,0 mL da solução de NaOH até o ponto final.
Assertiva: Nesse caso, a concentração da solução de NaOH
era menor que 0,2 mol/L.
O álcool em gel é principalmente composto de uma solução aquosa de álcool etílico a 70% (em massa). Para que o produto adquira a consistência de gel, são adicionados à formulação polímeros carbômeros, como o ácido poliacrílico, e outros compostos, como a trietanolamina, a glicerina e o álcool isopropílico (propan-2-ol). A próxima tabela apresenta a estrutura molecular de algumas dessas substâncias.
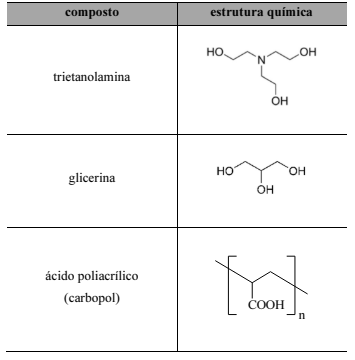
O carbopol, representado na tabela, pode ser obtido a partir da polimerização do ácido prop-2-enoico.
O álcool em gel é principalmente composto de uma solução aquosa de álcool etílico a 70% (em massa). Para que o produto adquira a consistência de gel, são adicionados à formulação polímeros carbômeros, como o ácido poliacrílico, e outros compostos, como a trietanolamina, a glicerina e o álcool isopropílico (propan-2-ol). A próxima tabela apresenta a estrutura molecular de algumas dessas substâncias.

A nomenclatura oficial da glicerina é propano-1,2,3-triol.