Questões de Vestibular
Sobre interações atômicas: geometria molecular, polaridade da ligação e da molécula, forças intermoleculares e número de oxidação. em química
Foram encontradas 339 questões
Em uma indústria do Estado de São Paulo que produz ácido sulfúrico 98% a partir da queima de enxofre elementar, com capacidade de produção inicial de 600 toneladas por dia, ocorreu uma emissão de gás dióxido de enxofre (SO2). Essa emissão de gás ultrapassou as fronteiras da fábrica de ácido sulfúrico e atingiu a população do entorno. Várias pessoas apresentaram agravos à saúde relacionados ao caso, como irritação das vias aéreas, desmaios, vômitos e enjoos, demandando atendimento hospitalar de emergência em hospitais da região. Também foram acionados o Serviço de Atendimento Médico de Urgência (SAMU) e o Corpo de Bombeiros.
JÚNIOR, L.M.; LORENZI, R.L. Revista brasileira de saúde ocupacional. São Paulo: 32(116): 31-37, 2007. (Adaptado)
Sobre o assunto, é CORRETO afirmar que:
a molécula de SO2 é apolar devido à sua geometria.
Considerando uma espécie química monoatômica que tem 78 prótons, 117 nêutrons e 74 elétrons, analise as seguintes afirmações:
I.É um metal de transição do bloco d.
II.Essa espécie química é um cátion, com estado de oxidação +4.
III.O número de massa do elemento é 117.IV.Essa espécie química é um ânion, com estado de oxidação –4.
Está correto somente o que se afirma em
PCl3 BF3 SO2 SO4 2- NH4 + 1 2 3 4 5
Qual molécula ou íon apresenta geometria molecular angular?
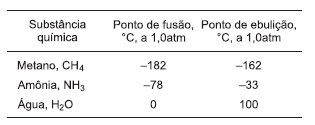
De acordo com o modelo de estrutura interflexível de Titã proposto por pesquisadores de algumas Universidades, com base nos dados da tabela e considerando-se que a pressão da atmosfera da maior lua de Saturno é igual a 1,0atm, é correto afirmar:

Cientistas descobriram que a cloração da água para desinfecção produz compostos halogenados secundários, como triclorometano e tribromometano, apresentados na tabela, dentre outras substâncias químicas halogenadas classificadas como carcinogênicas. A recomendação da Organização Mundial da Saúde, OMS, é reduzir a quantidade do cloro adicionada à água e monitorar a concentração dos compostos halogenados para que estejam dentro dos limites estabelecidos.
Com base nas informações e nos dados fornecidos na tabela associados aos conhecimentos sobre a relação entre as estruturas
e propriedades dos compostos moleculares, é correto afirmar:
A ferrugem contém uma substância que é formada pela reação do oxigênio do ar com o ferro presente em uma superfície metálica. Esse processo pode ser representado pela seguinte equação química:
4 Fe(s) + 3 O2 (g) ---- > 2 Fe2 O3 (s)
Nesse processo, o oxigênio sofre a transformação química denominada:
Não produzir qualquer tipo de resíduo ou poluente é o principal atributo em favor do hidrogênio como combustível para gerar energia elétrica. Ele faz funcionar células de combustível, equipamentos que produzem eletricidade sem danos ambientais. Como uma das fontes de hidrogênio é a água, uma das alternativas, em consonância com a preocupação ambiental, é o reuso da água como produção de energia renovável, utilizando esgotos e efluentes industriais.
O grupo de professores da Escola de Engenharia de São Carlos/USP desenvolveu um método para produzir hidrogênio em um reator de fluxo contínuo, constantemente alimentado com rejeitos que seriam, muitas vezes, descartados sem tratamento em rios e lagoas. No sistema, bactérias anaeróbicas do gênero Clostridium, que não precisam de oxigênio para viver, aderem a partículas de polietileno dentro de um reator.
Nos automóveis, movidos a células de combustível, o consumo de hidrogênio varia de 1,0 a 10,0g/km rodado, segundo um professor do grupo.
(OLIVEIRA, 2009, p. 100).
Leia o texto para responder à questão.
Lâmpadas sem mercúrio
Agora que os LEDs estão jogando para escanteio as lâmpadas fluorescentes compactas e seu conteúdo pouco amigável ao meio ambiente, as preocupações voltam-se para as lâmpadas ultravioletas, que também contêm o tóxico mercúrio.
Embora seja importante proteger-nos de muita exposição à radiação UV do Sol, a luz ultravioleta também tem propriedades muito úteis. Isso se aplica à luz UV com comprimentos de onda curtos, de 100 a 280 nanômetros, chamada luz UVC, que é especialmente útil por sua capacidade de destruir bactérias e vírus.
Para eliminar a necessidade do mercúrio para geração da luz UVC, Ida Hoiaas, da Universidade Norueguesa de Ciência e Tecnologia, montou um diodo pelo seguinte procedimento: inicialmente, depositou uma camada de grafeno (uma variedade cristalina do carbono) sobre uma placa de vidro. Sobre o grafeno, dispôs nanofios de um semicondutor chamado nitreto de gálio-alumínio (AlGaN). Quando o diodo é energizado, os nanofios emitem luz UV, que brilha através do grafeno e do vidro.
(www.inovacaotecnologica.com.br. Adaptado.)

Analise as estruturas das clorofilas a e b.
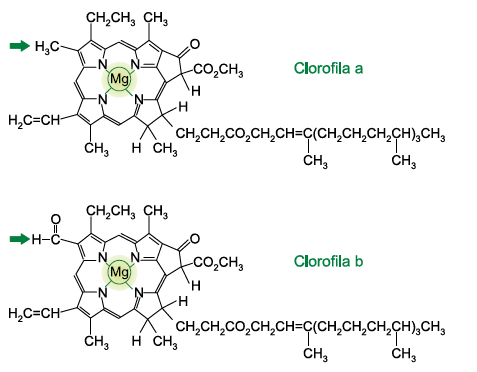
(www.infoescola.com)
As clorofilas a e b estão presentes na estrutura celular denominada __________, sendo que a clorofila ___________é a principal responsável pelo processo de fotossíntese. Nas duas clorofilas, o elemento magnésio encontra-se sob a forma de íons com número de carga _________ . A diferença entre as duas estruturas é a presença, na clorofila b, de um grupo da função orgânica ___________, em vez de um dos grupos metil da clorofila a.
As lacunas do texto são preenchidas, respectivamente, por:
Cd(s) + NiO2(s) + 2H2O(l) → Cd(OH)2(s) + Ni(OH)2(s).
Considere as seguintes afirmações a respeito dessa reação:
I. O cádmio se oxida.
II. O dióxido de níquel é o agente redutor.
III. O cádmio é o agente oxidante.
IV. O número de oxidação do níquel varia de +4 para +2.
Está correto o que se afirma em
DADOS QUE PODEM SER USADOS NESTA PROVA:

ELEMENTO NÚMERO MASSA
QUÍMICO ATÔMICO ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Na 11 23,0
Si 14 28,1
P 15 31,0
S 16 32,0
Cl 17 35,5
K 19 39,0
Cr 24 52,0
Cu 29 63,5
As 33 75,0
Br 35 80,0
Ag 47 108,0
Sn 50 119,0
Ir 77 192,0
Au 79 197,0
Hg 80 200,0
O composto é o _______________________1 e a geometria de sua molécula é _______________2 .
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
QUÍMICO ATÔMICO
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Fe 26 56,0
Cu 29 63,5
Zn 30 65,4
Ag 47 108,0
Sn 50 119,0
Xe 54 131,0
W 74 184,0
Atente para os seguintes antioxidantes e as indicações em negrito.
I. Licopeno: C4H6 – CH2 – C35H48 (átomo de carbono) II. Vitamina A: C18H26 = CH – CH2 – OH (átomo de carbono)
A soma dos números de oxidação dos átomos indicados acima é
DADOS QUE PODEM SER USADOS NESTA PROVA:
ELEMENTO NÚMERO MASSA ATÔMICA
H 1 1,0
C 6 12,0
N 7 14,0
O 8 16,0
F 9 19,0
Si 14 28,0
S 16 32,0
Cl 17 35,5
Ca 20 40,0
Mn 25 55,0
Fe 26 56,0
Br 35 80,0
Rb 37 85,5
Zr 40 91,0
Ag 47 108,0
Cd 48 112,5
Ba 56 137,0
Pb 82 207,0
U 92 238,0
Pu 94 244,0
Observe a reação a seguir:
5C6H12O6 + 24NO-3 + 24H+ → 30CO2 + 42H2O + 12N2 + energia
Essa reação trata-se basicamente de um processo de respiração anaeróbica realizada por bactérias