Questões de Vestibular
Sobre interações atômicas: geometria molecular, polaridade da ligação e da molécula, forças intermoleculares e número de oxidação. em química
Foram encontradas 329 questões
Sobre o "gás Sarin", é possível inferir que:
Um joalheiro bastante experiente lapidou um pedaço de vidro e um diamante do mesmo tamanho, cortando-os em inúmeras facetas e, a seguir, os poliu de forma a ficarem idênticos. Contudo, o vidro não apresenta o mesmo brilho do diamante ao ser incidido pela luz.
Fonte: SOUZA, Líria Alves de. "Brilho do diamante"; Brasil Escola. Disponível em . Acesso em 20 de maio de 2018. (adaptado)
O vidro, mesmo após todo esse processo, não exibe o mesmo brilho pois o diamante é um sólido
A partir dessas informações, é correto afirmar:
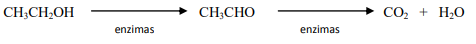
Disponível em: < http://qnesc.sbq.org.br/online/qnesc05/quimsoc.pdf > Acesso em: 1 nov. 2011 (adaptado).
Dadas as massas molares (g.mol-1): C = 12, H = 1, O = 16
De acordo com os seus conhecimentos de química é incorreto afirmar que:
O gás oxigênio é imprescindível para a vida dos seres vivos aeróbios. É o segundo gás mais abundante da atmosfera, e é pouco solúvel em água. Ademais, a sua diminuição por despejos de esgotos não tratados diretamente nos rios e córregos é preocupante por comprometer a fauna aquática.
Sobre o gás oxigênio, são feitas abaixo algumas afirmações. Assinale a correta.
I. CaC2(s) + N2(g) 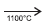 CaNCN(s) + C(s)
CaNCN(s) + C(s)
II. CaNCN(s) + 5H2O(ℓ) → CaCO3(s) + 2NH4OH(aq)
Quando carbeto de cálcio, CaC2, é aquecido em um forno elétrico, na presença de nitrogênio atmosférico, a 1100ºC, dá origem à cianamida de cálcio, empregada largamente como fertilizante nitrogenado de ação lenta, pois leva alguns meses, no solo, para se hidrolisar de acordo com a equação química II. Como a cianamida de cálcio não é arrastada pelas chuvas, é um fertilizante melhor do que o nitrato de amônio, NH4NO3, e a ureia, CO(NH2)2.
Uma análise dessas informações permite afirmar:
Considere a sequência das substâncias em soluções ácidas.
SO42- → S2O62- → SO2 → S2O32- → S8.
O enxofre apresenta, respectivamente, maior e menor número de oxidação em:

O diagrama representa a entalpia de formação do pentacloreto de fósforo a partir de duas variedades alotrópicas de fósforo, o fósforo branco e o fósforo vermelho.
A partir da análise desse diagrama, é correto afirmar:
A partir da utilização desses modelos de ligação química na compreensão da estrutura molecular de algumas substâncias, é correto afirmar:
São dadas três substâncias:
I - água
II - gás carbônico
III - trióxido de enxofre
Assinale a alternativa em que são determinadas,
respectivamente, a polaridade e a geometria das
moléculas constituintes das substâncias.
As propriedades físico-químicas das substâncias são afetadas pelas interações intra e intermoleculares.
Com base nos conhecimentos de química e nos dados da tabela, é correto afirmar:
As moléculas de CH4
e CCl4
possuem momento dipolar permanente.
As propriedades físico-químicas das substâncias são afetadas pelas interações intra e intermoleculares.
Com base nos conhecimentos de química e nos dados da tabela, é correto afirmar:
A geometria da molécula do SF6 é octaédrica.
As propriedades físico-químicas das substâncias são afetadas pelas interações intra e intermoleculares.
Com base nos conhecimentos de química e nos dados da tabela, é correto afirmar:
O SO2 é uma molécula apolar, pois possui geometria linear.
Em 18 de Fevereiro de 2015, o Google Doodle fez uma homenagem ao 270o aniversário do inventor da pilha elétrica, Alessandro Volta, um físico italiano que tinha como uma de suas paixões a eletricidade. A unidade elétrica volt é uma homenagem a esse inventor.
Volta também estudou Química, essa ciência teve grande importância no que diz respeito à pilha elétrica.

<http://tinyurl.com/m5dagtf> Acesso em: 20.02.2015. Adaptado. Original colorido.
Na imagem, podemos observar uma pilha e duas semirreações que representam os processos de oxidação e de redução,
envolvidos na confecção dessa pilha, cujos potenciais padrão de redução são:
I. Zn2+/Zn: - 0,76 V
II. 2H+/H2 : 0,00 V
Um dos materiais usados na confecção da pilha é o zinco, cujo símbolo é Zn e apresenta
• Número atômico: 30
• Massa atômica: 65,4 u
• Ponto de fusão: 419,5 °C
• Ponto de ebulição: 907 °C
• Configuração por camadas:
K L M N
2 8 18 2
