Questões de Vestibular
Sobre interações atômicas: geometria molecular, polaridade da ligação e da molécula, forças intermoleculares e número de oxidação. em química
Foram encontradas 339 questões
1) O NOX do cobalto é +3, pois tem-se o íon Co3+ .
2) Apresenta ligações iônicas e covalentes coordenadas.
3) O íon nitrato apresenta carga 1−.
Está(ão) correta(s):
I- Sua Geometria é angular.
II- Forma Ligações de Pontes de Hidrogênio.
III- Solubiliza substâncias de baixa polaridade como, por exemplo, os óleos.
IV- Apresenta ligações tipo covalentes polarizadas.
V- Apresenta-se nos três estados físicos da matéria.

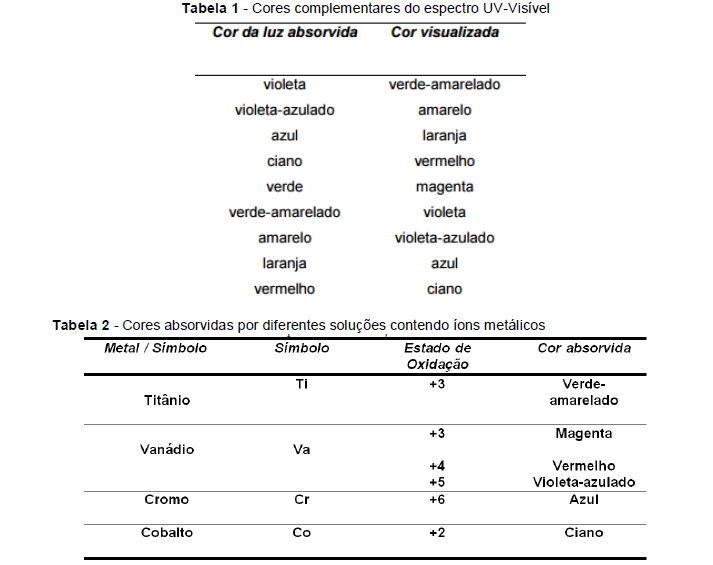
Na dissolução de três compostos metálicos foram visualizadas as seguintes colorações:
Sistema 1 - Violeta Sistema 2 - Ciano Sistema 3 - Laranja
Os íons presentes no sistema 1, 2 e 3 são, respectivamente:
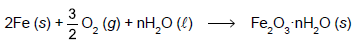
A tabela fornece os potenciais-padrão de redução (Eº) de algumas semirreações, a 25 ºC.

Com base nas informações fornecidas, pode-se afirmar que:
I. O ferro presente na hematita apresenta número de oxidação igual a +2.
II. De acordo com o processo, para cada mol de hematita adicionada, são utilizados 3 mol de monóxido de carbono.
III. Para um rendimento global igual a 50%, a massa de ferro formada a partir de 1280 kg de hematita é de 448 kg.
IV. O gás carbônico dissolvido em água forma uma solução que apresenta valor de pH maior do que 7.
Dadas as massas molares (g/mol): C = 12, O = 16 e Fe = 56.
A respeito dessas substâncias, assinale a alternativa correta.
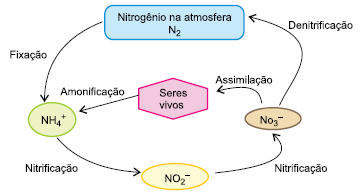
No ciclo do nitrogênio, a etapa que envolve oxidação é a

A questão abaixo se refere à figura acima. O cloreto de
amônio possui fórmula estequiométrica NH4Cl e, na
forma sólida, ele se cristaliza de acordo com uma
estrutura tridimensional, chamada célula unitária, na qual
oito íons cloreto (Cl-
) ocupam os vértices de um cubo, e o
íon amônio (NH4+
) está localizado no centro desse cubo.
Em relação ao íon amônio, o átomo de nitrogênio ocupa
exatamente o centro do cubo, e os átomos de hidrogênio
formam uma figura geométrica cujos vértices se
localizam nas diagonais do cubo. Sabendo que o diâmetro
de um íon Cl-
e a distância entre os centros de dois íons
Cl-
que ocupam as extremidades de uma mesma aresta do
cubo são iguais a 362 picômetros, assinale o que for
correto.