Questões de Vestibular
Sobre interações atômicas: ligações iônicas, ligações covalentes e ligações metálicas. ligas metálicas. em química
Foram encontradas 222 questões
 Os percentuais de cobre e estanho na mencionada liga são, respectivamente,
Os percentuais de cobre e estanho na mencionada liga são, respectivamente, 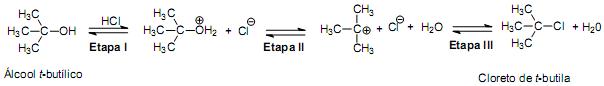
A análise da figura permite perceber que, na etapa
I. Cátions são íons de carga positiva.
II. Ligações iônicas são formadas pelo compartilhamento de elétrons.
III. O Potencial de ionização nos elementos da família 1A é diretamente proporcional ao raio atômico.
IV. Uma ligação covalente é exclusivamente uma ligação π (pi).
V. Elementos com distribuição eletrônica final em np5 , são por características, doadores de elétrons.
VI. Ligações metálicas são realizadas por todos os elementos representativos.
VII. A formação de um líquido é devido a atrações eletrostáticas entre íons.
VIII. Átomos com hibridização sp2 correspondem a elementos da família 2A da tabela periódica.
IX. Potencial de ionização corresponde à energia necessária para a retirada de um elétron da camada de valência, portanto, é um processo exotérmico.
É CORRETO o que se afirma apenas em:
Analise as alternativas a seguir:
I. Ambos os elementos químicos, carbono e hidrogênio, adquirem estabilidade ao se ligarem covalentemente, pois passam a ter configurações dos gases nobres neônio e hélio, respectivamente.
II. A geometria tetraédrica da molécula de metano é possível ser confirmada pela análise da distribuição eletrônica do carbono no estado fundamental.
III. Para a molécula do metano a substituição de dois átomos de hidrogênio por dois de cloro, através da reação de halogenação de hidrocarbonetos, produz uma mistura de isômeros.
É INCORRETO o que se afirma em:


A respeito do assunto abordado no texto acima, assinale a opção
correta e julgue o item.
No Quadro abaixo, estão relacionadas algumas características de materiais metálicos identificados como I, II, III e IV.
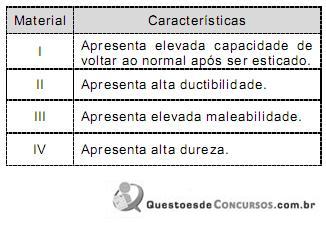
Para a construção do dispositivo eletrônico, deve ser utilizado o material identificado como
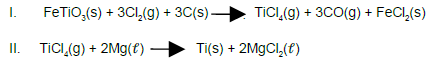
O titânio, metal leve utilizado na construção de equipamentos industriais, aeronaves e na confecção de implantes dentários e de cerdas de escovas de dente, é resistente a corrosão e a temperaturas altas.
O processo de produção do titânio, a partir da ilmenita representada pela fórmula molecular FeTiO3 , inclui, resumidamente, as equações químicas I e II, em destaque.
A partir dessas considerações e das equações químicas, que representam o processo de produção do titânio, é correto afirmar:
A seguir estão representadas quatro estruturas de substâncias.
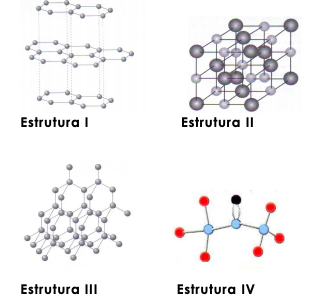
Considerando-se essas estruturas, é correto afirmar:

Desde eras remotas o ser humano extrai da natureza corantes, numa busca incessante pela diversidade de cores. São exemplos, o índigo, extraído da planta Indigofera tinctoria, e a brasileína, da Caesalpinia echinata (pau-brasil), entre muitos outros extraídos de vegetais. No entanto, poucas substâncias de origem animal foram utilizadas como corantes têxteis. Apesar disso, os corantes vermelhos provenientes de insetos, o quermes e a cochinilha, foram muito apreciados. Por exemplo, o Império Romano valorizava-os tanto que era um dos tributos que as nações conquistadas tinham de pagar. O imperador Nero chegou a punir com a morte o uso da púrpura de Tiro, corante obtido a partir de espécies de um molusco do género Murex.
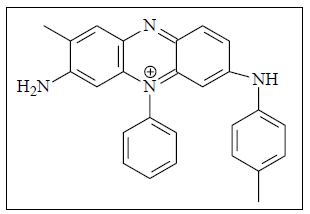
A história mostra que a determinação da estrutura da mauveína não foi fácil de ser alcançada. De modo satisfatório, a estrutura química deste corante só foi conseguida em 1994. De fato existem quatro compostos denominados de mauveína, sendo um deles (mauveína A) apresentado ao lado.
Com base nesta estrutura, pode-se dizer que a mauveína A é um composto
A tabela a seguir apresenta os comprimentos das ligações químicas presentes na molécula do cis-1,2-dicloroeteno:

• os núcleos atômicos têm dimensões desprezíveis;
• os comprimentos das ligações correspondem à distância entre os núcleos.
A distância, em nanômetros, entre os dois núcleos de hidrogênio na molécula do cis-1,2-dicloroeteno equivale a:
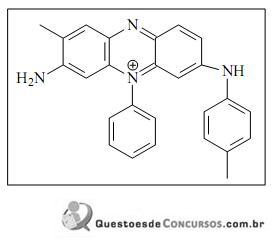
Com base nesta estrutura, pode-se dizer que a mauveína A é um composto

Considerando essas informações, julgue os itens seguintes.

(Dado: 1 mol equivale a 6.1023 moléculas.)

As lacunas do texto podem ser preenchidas corretamente por

