Questões de Vestibular
Sobre interações atômicas: ligações iônicas, ligações covalentes e ligações metálicas. ligas metálicas. em química
Foram encontradas 218 questões
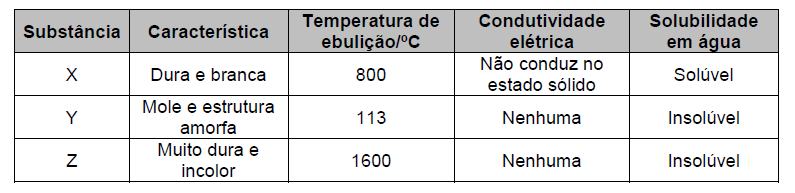
A partir das informações fornecidas nesse quadro, é CORRETO afirmar que as substâncias sólidas X, Y e Z são, respectivamente,
I. O composto X é um sólido cristalino de cor branca.
II. Uma solução aquosa do composto X muda para vermelho o papel tornassol azul.
III. A solução, mesmo concentrada, do composto X é má condutora de eletricidade.
IV. A reação do composto X com hidróxido de sódio forma um composto bom condutor de eletricidade.
A partir desses testes, é CORRETO afirmar que o composto X deve ser o
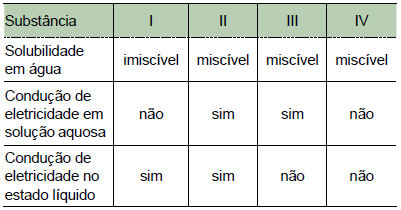
A natureza iônica é observada somente


representa a curva de aquecimento, sob pressão
de 1,0 atm, em cal × °C de 10,0 g de um material
hipotético. Sobre esse material, assinale o que for
correto.
É uma propriedade comum a todos esses compostos:
1 - A substância apresenta altos pontos de fusão e ebulição; 2 - A substância conduz energia elétrica no estado sólido.
ASSINALE a alternativa que indica a substância testada pelo estudante.
A nitroglicerina é um líquido oleoso de cor amarelopálida, e é altamente sensível a choque. O simples ato de balançar o líquido pode causar a explosiva decomposição em gases de nitrogênio, dióxido de carbono, água e oxigênio. Em virtude de a nitroglicerina ser tão instável, é difícil usá-la como um explosivo controlável. O inventor sueco, Alfred Nobel descobriu que a mistura de nitroglicerina com um material sólido absorvente como terra diatomácea ou celulose resulta em explosivo sólido (dinamite), que é muito mais seguro que a nitroglicerina pura.
Sobre o texto acima, é INCORRETO afirmar que:
Considere as seguintes informações sobre uma liga metálica de bismuto:

As características dessa liga metálica permitem seu uso em

A questão abaixo se refere à figura acima. O cloreto de
amônio possui fórmula estequiométrica NH4Cl e, na
forma sólida, ele se cristaliza de acordo com uma
estrutura tridimensional, chamada célula unitária, na qual
oito íons cloreto (Cl-
) ocupam os vértices de um cubo, e o
íon amônio (NH4+
) está localizado no centro desse cubo.
Em relação ao íon amônio, o átomo de nitrogênio ocupa
exatamente o centro do cubo, e os átomos de hidrogênio
formam uma figura geométrica cujos vértices se
localizam nas diagonais do cubo. Sabendo que o diâmetro
de um íon Cl-
e a distância entre os centros de dois íons
Cl-
que ocupam as extremidades de uma mesma aresta do
cubo são iguais a 362 picômetros, assinale o que for
correto.

A questão abaixo se refere à figura acima. O cloreto de
amônio possui fórmula estequiométrica NH4Cl e, na
forma sólida, ele se cristaliza de acordo com uma
estrutura tridimensional, chamada célula unitária, na qual
oito íons cloreto (Cl-
) ocupam os vértices de um cubo, e o
íon amônio (NH4+
) está localizado no centro desse cubo.
Em relação ao íon amônio, o átomo de nitrogênio ocupa
exatamente o centro do cubo, e os átomos de hidrogênio
formam uma figura geométrica cujos vértices se
localizam nas diagonais do cubo. Sabendo que o diâmetro
de um íon Cl-
e a distância entre os centros de dois íons
Cl-
que ocupam as extremidades de uma mesma aresta do
cubo são iguais a 362 picômetros, assinale o que for
correto.
As lacunas do texto devem ser preenchidas por:
As lacunas do texto devem ser preenchidas por:
