Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
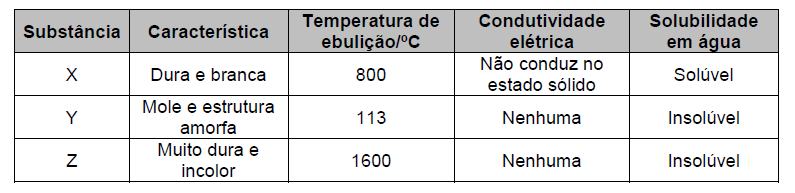
A partir das informações fornecidas nesse quadro, é CORRETO afirmar que as substâncias sólidas X, Y e Z são, respectivamente,
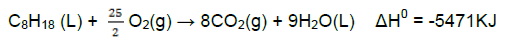
Nestas condições, é CORRETO afirmar que a razão entre as energias gastas em um ano, nessa jornada, pelo automóvel e o estudante na bicicleta, é aproximadamente
I. O composto X é um sólido cristalino de cor branca.
II. Uma solução aquosa do composto X muda para vermelho o papel tornassol azul.
III. A solução, mesmo concentrada, do composto X é má condutora de eletricidade.
IV. A reação do composto X com hidróxido de sódio forma um composto bom condutor de eletricidade.
A partir desses testes, é CORRETO afirmar que o composto X deve ser o
Pressão Osmótica é a pressão que deve ser aplicada à solução para evitar que ocorra o fluxo osmótico, ou seja, a passagem de solvente do meio mais diluído para o meio mais concentrado através de uma membrana semipermeável. O sangue e o soro fisiológico (0,9% em massa de NaCl) apresentam a mesma pressão osmótica. Uma célula de hemoglobina foi colocada em uma solução 0,20 mol/L de NaCl.
Fonte: Adaptado de: https://mundoeducacao.bol.uol.com.br/quimica/pressao-osmotica.htm – Acesso em 14 de Maio de 2019.
Em relação à solução, essa célula estará em meio:
Considere as semiequações e potenciais padrão de redução (ε 0 ) para o estanho e o ferro.
Fe2+(aq) + 2e- → Fe(s) ε 0 = -0,44 V
Sn2+(aq) + 2e- → Sn(s) ε 0 = -0,14 V
A corrosão da lata revestida com estanho é explicada pelo(a):
BaSO4 (s) → Ba2+(aq) + SO4 2- (aq) K2SO4 (s) → 2K+ (aq) + SO4 2- (aq)
A função do sulfato de potássio nessa situação é:
2NaN3 (s) → 2Na (s) + 3N2 (g)
Fonte: https://www.scientificamerican.com/article/how-do-air-bags-work/
Considere a pressão atmosférica de 1 atm, a temperatura de 300 K e R (constante universal dos gases ideais) = 0,08 atm L mol-1 K -1 .
O volume de gás nitrogênio, em m³ , liberado pela decomposição de 65 g de azida de sódio, é:
Com relação aos polímeros, três afirmações foram feitas:
1) Os polímeros são compostos por monômeros (unidades) que se repetem.
2) As ligações entre os monômeros (unidades) dos polímeros são iônicas.
3) As principais propriedades dos polímeros estão associadas à estrutura do monômero utilizado.
Está(ão) correta(s) a(s) afirmativa(s):
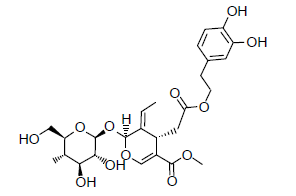
três afirmações foram feitas:
1) Possui os grupos éster, éter e álcool.
2) Possui átomos de carbono com geometria tetraédrica ou trigonal planar.
3) Apresenta isomeria ótica, pois possui carbonos assimétricos (quirais).
Está(ão) correta(s) a(s) afirmativa(s):
H2(g) + S(s)
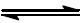 H2S(g)
H2S(g)
as quantidades de gás hidrogênio e sulfeto de hidrogênio são 0,40 g e 0,47 g, respectivamente, determine a constante de equilíbrio, Kc para a reação em estudo.
Dados: Massas molares em g . mol−1 : H = 1; S = 32.
1) Na água com gás a velocidade de reação deve ser menor do que em água natural.
2) Em água gelada a velocidade de reação deve ser menor que em água natural.
3) No terceiro dia a vitamina C efervescente se dissolveu mais rápido que nos dias anteriores.
Está(ão) correta(s) apenas:
I. Zn(s) + 2OH− (aq) → ZnO(s) + H2O(l) + 2e− , E° = +1,26 V
II. 2MnO2(s) + H2O(l) + 2e− → Mn2O3(s) + 2OH− (aq), E° = +0,26 V
É correto afirmar sobre as pilhas alcalinas:
1) A reação (I) ocorre no ânodo; a reação (II) ocorre no cátodo.
2) A concentração do eletrólito alcalino (KOH) é mantida constante.
3) O potencial de cela (∆E°) desenvolvido através da célula eletroquímica, envolvendo as duas reações (I e II), será de +1,52 V.
Está(ão) correta(s) a(s) afirmativa(s):
C6H12O6(s) + 6 O2 (g) → 6 CO2(g) + 6 H2O(l)
Calcule a entalpia padrão de combustão da glicose sabendo as entalpias padrão de formação:
∆Hf°(C6H12O6,s) = −1.268 kJ∙mol−1 ∆Hf°(CO2,g) = −393,51 kJ∙mol−1 ∆Hf°(H2O,l) = −285,83 kJ∙mol−1
2 CrO42-(aq) + H+(aq)
 Cr2O72-(aq) + H2O(l)
Cr2O72-(aq) + H2O(l)
À partir deste equilíbrio, foram feitas três afirmações:
1) Em pH ácido, o equilíbrio será deslocado para a formação do íon dicromato.
2) Em pH básico, o equilíbrio será deslocado para a formação de íon cromato.
3) O equilíbrio químico não é dinâmico, por isso acima de pH 7 deve ocorrer o consumo total de íons dicromato.
Está(ão) correta(s) a(s) afirmativa(s):
H2(l) + ½ O2(l) → H2O(g), ∆H = -242 kJ.mol-1
Levando-se em consideração a aplicação, e que todo o combustível é consumido, qual é a energia (J) liberada para propulsão do ônibus espacial?
À partir dessas informações, foram feitas três afirmações:
1) À temperatura ambiente, as moléculas dos componentes da gasolina e as do oxigênio não têm energia suficiente para iniciar a combustão.
2) A reação de combustão entre as moléculas dos componentes da gasolina e as do oxigênio pode ser iniciada na presença de um cigarro aceso, provocando uma explosão.
3) Entre as moléculas dos componentes da gasolina podemos encontrar compostos derivados do benzeno, que são compostos cancerígenos.
Está(ão) correta(s) a(s) afirmativa(s):
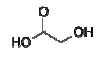 e é produzido pela reação do ácido cloroacético com o
hidróxido de sódio seguida por uma re-acidificação. A
reação pode ser equacionada da seguinte maneira:
e é produzido pela reação do ácido cloroacético com o
hidróxido de sódio seguida por uma re-acidificação. A
reação pode ser equacionada da seguinte maneira:
ClCH2CO2H + NaOH → HOCH2CO2H + NaCl
Desta forma, alguns milhões de quilogramas de ácido glicólico são produzidos anualmente.
Calcule a quantidade de ácido glicólico produzida a partir de 200 g de ácido cloroacético e 70,0 g de hidróxido de sódio. Dados: Massas molares em g . mol−1 : H = 1; C = 12; O = 16; Na = 23; Cl = 35,5.
x Au(s) + y NO3− (aq) + w H+ (aq) + z Cl− (aq) → a AuCl4− (aq) + b H2O(l) + d NO(g)
Após balancear a equação acima com os menores números possíveis, correspondentes, a soma dos coeficientes estequiométricos será:
Dados: Massas molares em g . mol−1 : H = 1; C = 12; N = 14; O = 16.
Fórmula molecular da creatinina: C4H7N3O