Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
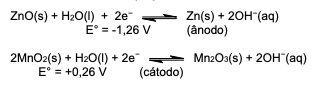
Qual é o potencial de célula (ΔE°) desenvolvido entre os polos positivo e negativo da pilha alcalina?
Dados: Massas molares em g.mol−1: Fe = 56; S = 32; O = 16.
Com relação a essa descrição, três afirmações foram feitas:
1) Be, Mg, Ca e Sr fazem parte do grupo dos metais alcalino-terrosos, grupo que apresenta facilidade em perder 2 elétrons, formando cátions bivalentes. 2) He, Ne, Ar e Kr são chamados de gases inertes, por possuírem a última camada de elétrons completa, dificultando assim a formação de ligações e a associação com outros átomos. 3) N, S, Se e Te fazem parte do grupo dos calcogênios, que apresentam a propriedade de formar duas ligações.
Está(ão) correta(s) a(s) afirmativa(s):
Os pesticidas, em geral, são classificados como inseticidas, herbicidas, fungicidas e outros. As estruturas de três herbicidas são apresentadas a seguir. A respeito desses compostos, podemos afirmar:
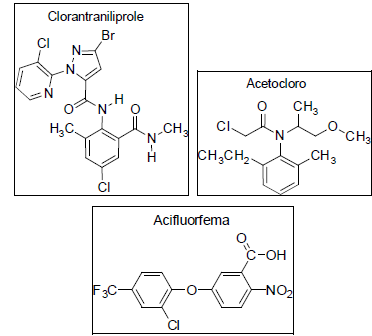
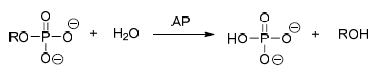
Considere as afirmações e assinale a alternativa correta.
Em relação a estes compostos, podemos afirmar que
1) X (Z =13) e Y (Z = 8)
2) A (Z = 19) e B (Z = 17)
As fórmulas dos compostos formados pelos átomos descritos em 1 e 2 são:
Admita uma solução aquosa de sulfato de ferro(II) que passou por um processo de eletrólise durante duas horas, empregando-se uma corrente elétrica com intensidade (i) de 5 A, e a semirreação a seguir:
Fe2 + (aq) + 2e- → Fe(s)
Considerando a Constante de Faraday = 96 500 C/mol, 1 hora = 3 600 s e massa molar do ferro (Fe) = 56 g/mol, a massa aproximada de ferro metálico que pode ser depositada no cátodo, nessas condições, é
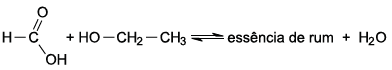 A nomenclatura IUPAC do éster formado que possui essência
de rum é
A nomenclatura IUPAC do éster formado que possui essência
de rum é 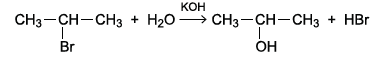
Essa equação representa uma reação orgânica de
Analise a cadeia carbônica do seguinte composto:
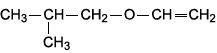
Essa cadeia carbônica é classificada como:
Compressas de emergência quentes são usadas como primeiro socorro em contusões sofridas em práticas esportivas. Essa compressa constitui-se de um saco de plástico contendo uma ampola de água e um produto químico seco, por exemplo, o cloreto de cálcio (CaCℓ2 ). Com uma leve pancada, a ampola se quebra e o cloreto de cálcio se dissolve, conforme a reação representada pela equação:
CaCℓ2 (s) + H2 O (ℓ) → CaCℓ2 (aq) ∆H = −82,7 kJ/mol
Nesse processo,
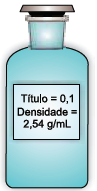

Considerando a massa molar desse composto igual a 106 g/mol, a concentração aproximada, em g/L e em mol/L, de Na2CO3 nessa solução é, respectivamente,
Considere a reação química que ocorre dentro de um recipiente fechado, à temperatura constante, e o gráfico com os valores das concentrações de estado de equilíbrio químico das espécies participantes.
H2
(g) + Cℓ2
(g) 2HCℓ (g)
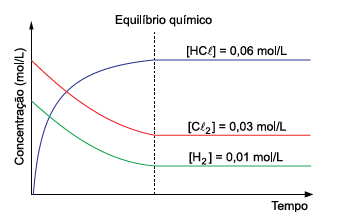
Considerando os dados da reação e do gráfico, pode-se concluir que o valor da constante de equilíbrio químico (Kc
) para
essa reação é
O gás butano (C4 H10) é um combustível não renovável derivado do petróleo, cuja combustão incompleta ocorre quando a quantidade de oxigênio é insuficiente para que ocorra a combustão completa.
Considere a equação da reação de combustão incompleta do gás butano:
2C4 H10 (g) + 9O2 (g) 8CO (g) + 10H2 O (g)
A massa do gás monóxido de carbono (massa molar = 28 g/mol) formada quando 522 kg de gás butano (massa molar = 58 g/mol) sofrem combustão incompleta, numa reação com rendimento total, é de
Leia o texto para responder à questão.
Na Estação de Tratamento de Água (ETA), diferentes substâncias químicas são adicionadas à água nos diversos tanques por onde ela passa. No tanque de floculação, por exemplo, a adição de certas substâncias químicas estimula a formação de um composto gelatinoso, o hidróxido de alumínio, que provoca a aglutinação das partículas de sujeira. Essas partículas aderem ao composto gelatinoso, formando flóculos sólidos de tamanho maior, que são facilmente sedimentáveis.

(www.sobiologia.com.br. Adaptado.)
A substância química gelatinosa formada no tanque de floculação apresenta caráter __________ e valor de pH ____________ 7 a 25 ºC. Ao combinar-se com um ácido, essa substância forma ____________e _____________ , ocorrendo uma reação de _____________.
Completam as lacunas do texto, respectivamente,