Questões de Vestibular Sobre química
Foram encontradas 6.520 questões
HNO3(l) + SO2(g) + H2O(l) → H2SO4(l) + NO(g)
são feitas as seguintes afirmações:
I. O nitrogênio sofre redução. II. O enxofre ganha elétrons. III. O agente redutor é o SO2. IV. O agente oxidante é o HNO3.
São corretas as seguintes afirmativas:

Para esses dois compostos, pode-se afirmar que:
Certo isótopo desse elemento possui 86 prótons, 86 elétrons e número de massa 222, logo o número de nêutrons desse isótopo é
Se o jogador não se organizar em relação à sua dieta e suplementação, poderá perder força, rendimento e velocidade dentro do campo.
Uma alimentação balanceada deve apresentar alguns itens, como:
I. Carboidratos II. Proteínas III. Gorduras IV. Vitaminas e Minerais
(http://www.anutricionista.com/como-deve-ser-o-cardapio-de-um-jogador-de-futebol.html Acesso em: 14.02.2014. Adaptado)
Considerando os quatro itens mencionados no texto, assinale a alternativa que exemplifica cada um deles, respectivamente.
Na indústria têxtil, é uma prática comum aplicar goma aos tecidos no início da produção, para torná-los mais resistentes. Esse produto, entretanto, precisa ser removido posteriormente, no processo de desengomagem. Nesse processo, os produtos têxteis são mergulhados em um banho aquoso com uma enzima do grupo das amilases.
Os gráficos nas figuras 1 e 2 representam a eficiência da atividade dessa enzima em diferentes valores de temperatura e pH.
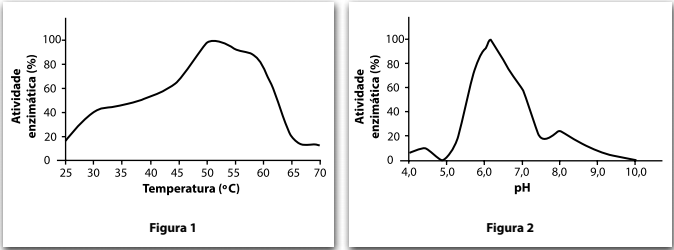
Com base nas informações apresentadas, está correto afirmar que, para se obter a máxima eficiência da ação da enzima no
processo industrial citado no texto, seria necessário manter o banho aquoso de desengomagem a
Após identificar a presença de álcool etílico, H3 C-CH2 -OH, em amostras de leite cru refrigerado usado por uma empresa na produção de leite longa vida e de requeijão, fiscais da superintendência do Ministério da Agricultura, Pecuária e Abastecimento recomendaram que os lotes irregulares dos produtos fossem recolhidos das prateleiras dos supermercados, conforme prevê o Código de Defesa do Consumidor. Segundo o Ministério, a presença de álcool etílico no leite cru refrigerado pode mascarar a adição irregular de água no produto.
(http://tinyurl.com/m8hxq6b Acesso em: 21.08.2014. Adaptado)
Essa fraude não é facilmente percebida em virtude da
grande solubilidade desse composto em água, pois
ocorrem interações do tipo
O uso de flúor é eficaz no combate à cárie dentária. Por isso, foram estabelecidos protocolos de utilização do flúor na área de saúde bucal como a adição de flúor na água de abastecimento público e em pastas dentais. A escovação dental é considerada um dos métodos mais eficazes na prevenção da cárie, ao aliar a remoção da placa à exposição constante ao flúor.
Todavia, a exposição excessiva pode causar alguns malefícios à saúde. Para isso, foram estabelecidos níveis seguros de consumo do flúor, quando este oferece o máximo benefício sem risco à saúde. As pastas de dente apresentam uma concentração de flúor que varia entre 1 100 e 1 500 ppm.
É importante ressaltar que as pastas de dente com flúor devem ser utilizadas durante a escovação e não ingeridas.
(http://tinyurl.com/ovrxl8b Acesso em: 29.08.2014. Adaptado)
A concentração máxima de flúor presente nas pastas de
dente mencionada no texto, em porcentagem em massa,
corresponde a
A história do seriado Breaking Bad gira em torno de um professor de Química do ensino médio, com uma esposa grávida e um filho adolescente que sofre de paralisia cerebral. Quando é diagnosticado com câncer, ele abraça uma vida de crimes, produzindo e vendendo metanfetaminas.
O uso de drogas pode desestabilizar totalmente a vida de uma pessoa, gerando consequências devastadoras e permanentes. Muitas vezes, toda a família é afetada.
As metanfetaminas são substâncias relacionadas quimicamente com as anfetaminas e são um potente estimulante que afeta o sistema nervoso central.
(http://tinyurl.com/pffwfe6 Acesso em: 13.06.2014. Adaptado)
Considere os elementos químicos e seus respectivos números atômicos, representados na figura.

(http://tinyurl.com/kun3zgs Acesso em: 30.08.2014.)
Esses elementos podem formar o composto
A história do seriado Breaking Bad gira em torno de um professor de Química do ensino médio, com uma esposa grávida e um filho adolescente que sofre de paralisia cerebral. Quando é diagnosticado com câncer, ele abraça uma vida de crimes, produzindo e vendendo metanfetaminas.
O uso de drogas pode desestabilizar totalmente a vida de uma pessoa, gerando consequências devastadoras e permanentes. Muitas vezes, toda a família é afetada.
As metanfetaminas são substâncias relacionadas quimicamente com as anfetaminas e são um potente estimulante que afeta o sistema nervoso central.
(http://tinyurl.com/pffwfe6 Acesso em: 13.06.2014. Adaptado)
A metanfetamina, N-metil-1-fenilpropano-2-amina, fórmula C10H15N , apresenta os isômeros representados pelas fórmulas estruturais:
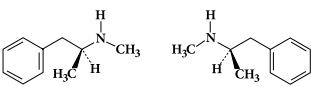
A análise das estruturas nos permite concluir, corretamente,
que os compostos são isômeros
Em 2014, na Alemanha, um elemento pesado foi confirmado por experimentos com um colisor de partículas e ocupará sua justa posição como Elemento 117 na Tabela Periódica.
Bombardeando amostras de berquélio radioativo com átomos de cálcio, pesquisadores criaram átomos com 117 prótons, originando um elemento químico, aproximadamente, 42% mais pesado que o chumbo e com meia-vida relativamente longa. Os físicos apelidaram, temporariamente, o novo integrante da Tabela Periódica como “ununséptio” (Uus), alusão direta ao numeral 117, que é a soma dos 20 prótons do cálcio com os 97 do berquélio.
(http://tinyurl.com/m8nlkq2 Acesso em: 13.06.2014. Adaptado)
De acordo com o texto, a massa atômica aproximada do ununséptio é
