Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
Relacione corretamente as equações com as reações químicas do cotidiano apresentadas abaixo, numerando a Coluna II de acordo com a Coluna I.
Coluna I
(1) 2NaHCO3 →Na2CO3 + CO2 + H2O
(2) Mg(OH)2 + CO2→MgCO3 + H2O
(3) 2NH3 + CO2 →CO(NH2)2 + H2O
(4) NaHCO3 + HCℓ→NaCℓ + H2CO3
Coluna II
( ) Produção de substância usada como fertilizante.
( ) Ação do sal de fruta no estômago humano.
( ) Feitura do bolo de chocolate.
( ) Absorção
do gás de
ambientes
fechados.
A sequência correta, de cima para baixo, é:
Um belo exemplo de como a química está presente em todo lugar são os vaga-lumes, nos quais ocorre uma reação química do tipo bioluminescente que “acende” seus corpos, produzindo um lindo efeito com a participação do oxigênio que age como agente oxidante e, dessa forma, uma reação de oxidação-redução é responsável pela emissão de luz. Atente ao que se diz a esse respeito:
I. Em uma reação de oxidação-redução, todos os átomos passam por variação do número de oxidação.
II. Geralmente não há oxidação sem redução e vice-versa.
III. As reações de dupla troca são de oxidação-redução.
IV. As reações de combustão (queima na presença de oxigênio) são também processos redox.
V. Os termos oxidante e redutor costumam referir-se às espécies químicas, e não somente a determinado átomo.
Está correto o que se afirma somente em
O nitreto de boro possui uma estrutura cúbica que se assemelha à estrutura do diamante e uma estrutura hexagonal semelhante à do grafite. Uma das variedades é usada em bases para mascarar rugas, porque reflete a luz. Considerando essa substância, analise as seguintes assertivas:
I. A variedade de nitreto de boro utilizada para cosméticos possui estrutura cúbica.
II. O boro não forma compostos binários iônicos.
III. O boro forma com o nitrogênio ligações covalentes apolares.
IV. O boro cristalino não reage com a água nem com o oxigênio gasoso.
Está correto o que se afirma somente em
Isomeria é o fenômeno pelo qual duas substâncias compartilham a mesma fórmula molecular, mas apresentam estruturas diferentes, ou seja, o rearranjo dos átomos difere em cada caso. Observe as estruturas apresentadas a seguir, com a mesma fórmula molecular C4H10O:
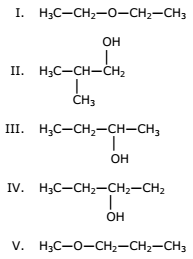
Assinale a opção em que as estruturas estão
corretamente associadas ao tipo de isomeria.
TEXTO 8
IX
Horas depois, teve Rubião um pensamento horrível. Podiam crer que ele próprio incitara o amigo à viagem, para o fim de o matar mais depressa, e entrar na posse do legado, se é que realmente estava incluso no testamento. Sentiu remorsos. Por que não empregou todas as forças, para contê-lo? Viu o cadáver do Quincas Borba, pálido, hediondo, fitando nele um olhar vingativo; resolveu, se acaso o fatal desfecho se desse em viagem, abrir mão do legado.
Pela sua parte o cão vivia farejando, ganindo, querendo fugir; não podia dormir quieto, levantava-se muitas vezes, à noite, percorria a casa, e tornava ao seu canto. De manhã, Rubião chamava-o à cama, e o cão acudia alegre; imaginava que era o próprio dono; via depois que não era, mas aceitava as carícias, e fazia-lhe outras, como se Rubião tivesse de levar as suas ao amigo, ou trazê-lo para ali. Demais, havia-se-lhe afeiçoado também, e para ele era a ponte que o ligava à existência anterior. Não comeu durante os primeiros dias. Suportando menos a sede, Rubião pôde alcançar que bebesse leite; foi a única alimentação por algum tempo. Mais tarde, passava as horas, calado, triste, enrolado em si mesmo, ou então com o corpo estendido e a cabeça entre as mãos.
Quando o médico voltou, ficou espantado da temeridade do doente; deviam tê-lo impedido de sair; a morte era certa.
— Certa?
— Mais tarde ou mais cedo. Levou o tal cachorro?
— Não, senhor, está comigo; pediu que cuidasse dele, e chorou, olhe que chorou que foi um nunca acabar. Verdade é, disse ainda Rubião para defender o enfermo, verdade é que o cachorro merece a estima do dono; parece gente.
O médico tirou o largo chapéu de palha para concertar a fita; depois sorriu. Gente? Com que então parecia gente? Rubião insistia, depois explicava; não era gente como a outra gente, mas tinha coisas de sentimento, e até de juízo. Olhe, ia contar-lhe uma...
— Não, homem, não, logo, logo, vou a um doente de erisipela... Se vierem cartas dele, e não forem reservadas, desejo vê-las, ouviu? E lembranças ao cachorro, concluiu saindo.
Algumas pessoas começaram a mofar do Rubião e da singular incumbência de guardar um cão em vez de ser o cão que o guardasse a ele. Vinha a risota, choviam as alcunhas. Em que havia de dar o professor! sentinela de cachorro! Rubião tinha medo da opinião pública. Com efeito, parecia-lhe ridículo; fugia aos olhos estranhos, olhava com fastio para o animal, dava-se ao diabo, arrenegava da vida. Não tivesse a esperança de um legado, pequeno que fosse. Era impossível que lhe não deixasse uma lembrança.
(ASSIS, Machado de. Quincas Borba. São Paulo: Ática, 2011. p. 30-31.)
TEXTO 4
Não desejei a morte de minha filha. Ou desejei? Aí é que reside a dúvida, é onde habita o nó que nada nem ninguém no mundo tem o poder de desatar. O inconsciente, desculpe-me a vulgaridade do termo, minha filha, é uma merda. Sendo autônomo, o inconsciente age por si, sem pedir licença nem se revelar. Desejei ou não a morte de minha filha, hein? Você pode responder a essa pergunta? Alguém pode? Eu não posso. Busquei na fonte a resposta e ela não veio. Como minha filha havia feito, busquei nas águas do Cristal a cura imediata para uma dor que parecia infinda. A ferida tinha sido cavada pelas águas, então elas que tratassem de cicatrizá-la. O rio recusou meu corpo, mas não a dor. Nem o aconselhamento. Pediu tempo, apenas. Permaneci plantada no barranco, juntando ao seu caudal minhas lágrimas secas. Disseram que eu tinha enlouquecido, talvez tivesse mesmo. Em diálogo profundo, as águas me fizeram compreender verdades para as quais eu nunca havia me atinado. Todo rio tem seu leito, suas margens, seu limite, toda vez que ele avança além de seu leito original provoca estragos, descalabros. O rio de nossa vida não é diferente. Ele também está sujeito a limitações intransponíveis. Existe você e você; seu campo de visão, a capacidade de administrar o próprio caudal. Tem a hora de abrir e a hora de fechar as comportas. Felicidade ou dor, a escolha é sua, depende do grau de intensidade que você der a cada coisa. Hoje posso dizer que me conheço um pouquinho, mesmo assim, perguntas continuam sem resposta.
(BARROS, Adelice da Silveira. Mesa dos inocentes. Goiânia: Kelps, 2010. p. 23.)
O Texto 4 faz menção a rio, que, muitas vezes é o destino final dos dejetos produzidos pela nossa sociedade. São várias as substâncias que os homens despejam nos rios, causando com isso diversos problemas ambientais. Dentre essas substâncias, podemos encontrar vários compostos inorgânicos, como sais, bases e ácidos. Analise as afirmativas a seguir:
I - A hidrólise de um sal proveniente de ácido forte e uma base fraca em água resultará na redução do pH.
II - Na hidrólise de um sal proveniente de um ácido fraco e base forte, a redução do pOH está em função do deslocamento do equilíbrio (da reação de autoionização da água) para a direita.
III - A adição de NaCl à água provoca a hidrólise desta, por se tratar de um sal proveniente de uma ácido e uma base fracos.
IV - A adição NaCl à água provoca a hidrólise desta, alterando-lhe o equilíbrio iônico.
Em relação às proposições analisadas, assinale a única alternativa cujos itens estão todos corretos:
Marque a alternativa que apresenta todos os itens corretos:
TEXTO 2
O milagre de viajar
Quisera eu, então, decifrar
os dias repletos de sombras moventes,
à exaltação do que, insalubre, vaga
pelos olhos dos homens.
Quisera, enfim,
saber por que das causas e quilhas
de barco nenhum
flui das tinas
dos dias
o fumo
o rum(o)
do que se foi e nunca mais será,
como da via o milagre
de viajar!
(VIEIRA, Delermando. Os tambores da tempestade. Goiânia:
Poligráfica, 2010. p. 142.)
No Texto 2 o verso “o rum(o)” remete a duas possibilidades de leitura: “o rum” e “o rumo”. Diz-se do rum, bebida alcoólica, que, dependendo do consumo, a pessoa realmente “perde o rumo”. O álcool presente no rum age no sistema nervoso central e deixa a pessoa mais corajosa.
Entre os álcoois, o etanol é obtido pela fermentação de açúcares, causada por micro-organismos específicos. Com base no texto e em seus conhecimentos, analise as proposições a seguir:
I - A reação do propan-2-ol com o ácido bromídrico produz o 1-bromo-propano.
II - Os álcoois, devido à presença da hidroxila ligada ao carbono sp2, têm caráter básico.
III - Os álcoois sofrem reações de substituição da hidroxila, cuja ordem de reatividade é: álcoois terciários são mais reativos que secundários, e estes mais reativos que álcoois primários.
Assinale a alternativa que apresenta todos os itens corretos:
TEXTO 1
Democracia
Punhos de redes embalaram o meu canto
para adoçar o meu país, ó Whitman.
Jenipapo coloriu o meu corpo contra os maus-
[olhados,
catecismo me ensinou a abraçar os hóspedes,
carumã me alimentou quando eu era criança,
Mãe-negra me contou histórias de bicho,
moleque me ensinou safadezas,
massoca, tapioca, pipoca, tudo comi,
bebi cachaça com caju para limpar-me,
tive maleita, catapora e ínguas,
bicho-de-pé, saudade, poesia;
fiquei aluado, mal-assombrado, tocando maracá,
dizendo coisas, brincando com as crioulas,
vendo espíritos, abusões, mães-d’água,
conversando com os malucos, conversando sozinho,
emprenhando tudo que encontrava,
abraçando as cobras pelos matos,
me misturando, me sumindo, me acabando,
para salvar a minha alma benzida
e meu corpo pintado de urucu,
tatuado de cruzes de corações, de mãos-ligadas,
de nomes de amor em todas as línguas de branco, de
[mouro ou de pagão.
(LIMA, Jorge de. Melhores poemas. São Paulo: Global, 2006. p. 74.)
O Texto 1 faz alusão metafórica ao ato de adoçar. O principal açúcar usado para adoçar alimentos é a sacarose, um dissacarídeo formado por dois monossacarídeos, glicose e frutose. A glicose é o açúcar mais simples que circula em nosso sangue, cuja concentração deve ser mantida entre 80 e 120 mg por 100 mL de sangue. A frutose é uma cetose, e a glicose é uma aldose. Sobre essa temática, analise os itens a seguir:
I - Se em um determinado exame a concentração de glicose foi de 0,5 g/L de sangue, esse resultado corresponde à faixa normal de glicose presente no sangue.
II - As reações de adição de hidrogênios a aldeídos formam álcoois primários, enquanto que nas cetonas formam álcoois secundários.
III - O composto com fórmula molecular C6 H12O pode formar os isômeros 4-metil-pentan-2-ona e 2,3-dimetilbutanal.
Estão corretos os itens:
A dopamina é um neurotransmissor importante em processos cerebrais. Uma das etapas de sua produção no organismo humano é a descarboxilação enzimática da L-Dopa, como esquematizado:
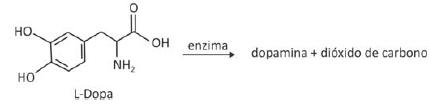
Sendo assim, a fórmula estrutural da dopamina é:
Células a combustível são opções viáveis para gerar energia elétrica para motores e outros dispositivos. O esquema representa uma dessas células e as transformações que nela ocorrem.
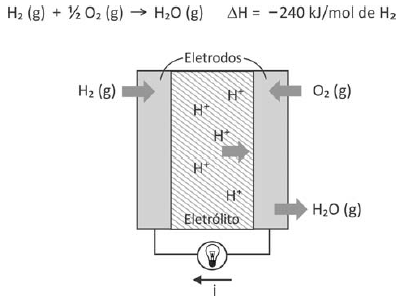
A corrente elétrica (i), em ampère (coulomb por segundo), gerada por uma célula a combustível que opera por 10 minutos e libera 4,80 kJ de energia durante esse período de tempo, é
Note e adote:
Carga de um mol de elétrons = 96.500 coulomb.
Sob certas condições, tanto o gás flúor quanto o gás cloro podem reagir com hidrogênio gasoso, formando,respectivamente, os haletos de hidrogênio HF e HCl, gasosos. Pode-se estimar a variação de entalpia (ΔH) de cada uma dessas reações, utilizando-se dados de energia deligação. A tabela apresenta os valores de energia de ligação dos reagentes e produtos dessas reações a 25 ºC e 1 atm.

Com base nesses dados, um estudante calculou a variação de entalpia (ΔH) de cada uma das reações e concluiu,corretamente, que, nas condições empregadas.
Para aumentar o grau de conforto do motorista e contribuir para a segurança em dias chuvosos, alguns materiais podem ser aplicados no para-brisa do veículo, formando uma película que repele a água. Nesse tratamento, ocorre uma transformação na superfície do vidro, a qual pode ser representada pela seguinte equação química não balanceada:
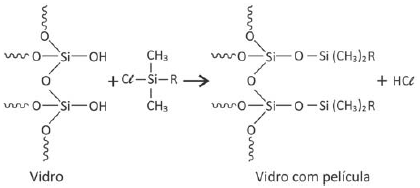
Das alternativas apresentadas, a que representa o melhor material a ser aplicado ao vidro, de forma a evitar o acúmulo de água, é:
Note e adote:
R = grupo de átomos ligado ao átomo de silício.
Note e adote: Composição aproximada do ar em volume: 80% de N2 e 20% de O2.
Em uma aula experimental, dois grupos de alunos (G1 e G2) utilizaram dois procedimentos diferentes para estudar a velocidade da reação de carbonato de cálcio com excesso de ácido clorídrico. As condições de temperatura e pressão eram as mesmas nos dois procedimentos e, em cada um deles, os estudantes empregaram a mesma massa inicial de carbonato de cálcio e o mesmo volume de solução de ácido clorídrico de mesma concentração.
O grupo G1 acompanhou a transformação ao longo do tempo, realizada em um sistema aberto, determinando a variação de massa desse sistema (Figura 1 e Tabela).
O grupo G2 acompanhou essa reação ao longo do tempo, porém determinando o volume de dióxido de carbono recolhido (Figura 2).
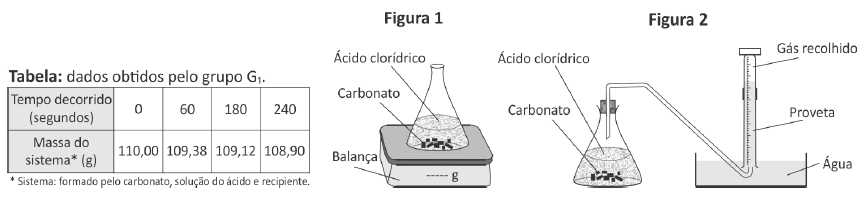
Comparando os dois experimentos, os volumes aproximados de CO2, em litros, recolhidos pelo grupo G2 após 60, 180 e 240 segundos devem ter sido, respectivamente,
Note e adote:
massa molar do CO2: 44 g/mol;
volume molar do CO2: 24 L/mol;
desconsidere a solubilidade do CO2 em água.
Um estudante realizou um experimento para avaliar a reatividade dos metais Pb, Zn e Fe. Para isso, mergulhou, em separado, uma pequena placa de cada um desses metais em cada uma das soluções aquosas dos nitratos de chumbo, de zinco e de ferro. Com suas observações, elaborou a seguinte tabela, em que (sim) significa formação de sólido sobre a placa e (não) significa nenhuma evidência dessa formação:

A seguir, montou três diferentes pilhas galvânicas, conforme esquematizado.

Nessas três montagens, o conteúdo do béquer I era uma solução aquosa de CuSO4 de mesma concentração, e essa solução era renovada na construção de cada pilha. O eletrodo onde ocorria a redução (ganho de elétrons) era o formado pela placa de cobre mergulhada em CuSO4 (aq). Em cada uma das três pilhas, o estudante utilizou, no béquer II, uma placa de um dos metais X (Pb, Zn ou Fe), mergulhada na solução aquosa de seu respectivo nitrato.
O estudante mediu a força eletromotriz das pilhas, obtendo os valores: 0,44 V; 0,75 V e 1,07 V.
A atribuição correta desses valores de força eletromotriz a
cada uma das pilhas, de acordo com a reatividade dos metais
testados, deve ser
