Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
Para o exercício, adote os seguintes valores quando necessário:

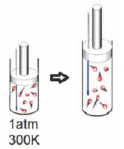
Com base no texto, é possível afirmar que a água do Rio Doce
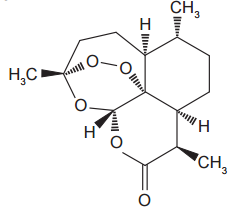
Com base nas informações, é correto afirmar que a artemisina apresenta
I. A pólvora negra é uma mistura de carvão vegetal, nitrato de potássio e enxofre em que predominam substâncias representadas, respectivamente, por: C, KNO3 e S.
II. A neutralização do hidróxido de amônio é representada por: NH4 Cl(s) + H2 O(l) → NH4 + (aq) + OH- (aq) + H+ (aq) + Cl- (aq).
III. A combustão de uma porção de palha de aço é representada pela seguinte equação: 2 Fe(s) + O2(g) → 2 FeO(s)
IV. Os elementos químicos do terceiro período da tabela periódica − que estão, respectivamente, no segundo e terceiro grupos − são representados por: Mg e Al.
De acordo com as informações acima, são corretas apenas as afirmativas
A seguir está representada a estrutura de uma substância orgânica de origem natural.
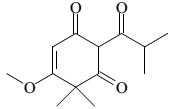
Nessa substância estão presentes as funções orgânicas
Considere as seguintes semicélulas e os respectivos potenciais-padrão de redução, numerados de I a VI.
I) Mn2+ (aq)/Mn(s) E0 =-1,18 V
II) Al3+ (aq)/Al(s) E0 =-1,66 V
III) Ni2+ (aq)/Ni(s) E0 =-0,25 V
IV) Pb2+ (aq)/Pb(s) E0 =-0,13 V
V) Ag+ (aq)/Ag(s) E0 = +0,80 V
VI) Cu2+ (aq)/Cu(s) E0 = +0,34 V
As duas semicélulas que formariam uma pilha com maior diferença de potencial são
Uma solução aquosa de nitrato de prata (0,050 mol L -1 ) é usada para se determinar, por titulação, a concentração de cloreto em uma amostra aquosa. Exatos 10,00 mL da solução titulante foram requeridos para reagir com os íons Cl- presentes em 50,00 mL de amostra. Assinale a concentração, em mol L-1 , de cloreto, considerando que nenhum outro íon na solução da amostra reagiria com o titulante.
Dado: Ag+ (aq) + Cl- (aq) → AgCl(s)
Na bancada de um laboratório, existem quatro soluções aquosas, cada uma contendo dissolvido um dos seguintes eletrólitos listados abaixo.
I. NaCl
II. NaOH
III. HCl
IV. CH3COONa
Considerando concentrações, em quantidade de matéria, equivalentes, as soluções teriam os valores de pH na seguinte ordem crescente:
Em linhas gerais, o consumo de água aumentou de forma considerável em todo o planeta ao longo do tempo. Em 1900, o mundo consumia cerca de 580 km³ de água; já em 1950, esse consumo elevou-se para 1400 km³, passando para 4000 km³ em 2000. Segundo previsões da ONU, é provável que em 2025 o nível de consumo eleve-se para 5200 km³. A despeito dessa elevação da utilização da água, registra-se também o aumento do número de pessoas sem fácil acesso à água potável, totalizando 1,1 bilhão em todo o planeta a sofrer com esse problema.
Além da utilização exagerada na área doméstica e no plano individual, soma-se o intensivo consumo de água nas atividades econômicas, notadamente a agricultura e a indústria, isso sem contar o grande volume desperdiçado. Não por acaso, a maior parte do consumo mundial de água acontece nos países desenvolvidos. Os emergentes ou subdesenvolvidos consomem em menor quantidade em razão do menor acesso à água e da menor intensidade das práticas econômicas. Segundo a ONU, o consumo dos países centrais é seis vezes maior do que o consumo dos países periféricos.
Fonte: http://brasilescola.uol.com.br/geografia/consumo-agua-no-mundo.htm
O monóxido de carbono é um gás incolor, sem cheiro ou sabor, inflamável e perigoso devido à sua grande toxicidade e por ser um asfixiante químico. O CO é liberado no ambiente por fontes naturais, por exemplo, atividade vulcânica, descargas elétricas e emissão de gás natural. Tudo isso é produto da combustão incompleta, ou seja, queima em condições de pouco oxigênio de combustíveis fósseis (lenha, carvão vegetal e mineral, gasolina, querosene, óleo diesel, gás). Em uma reação de combustão, em recipiente fechado, envolvendo o monóxido de carbono, mantido à temperatura constante, foram colocados o monóxido de carbono e gás oxigênio, cujas pressões parciais foram determinadas respectivamente com 4 atm e 1,6 atm , respectivamente. A reação ocorreu e após certo tempo, quando o equilíbrio foi atingido, verificou-se que a pressão parcial do gás oxigênio, foi de 608 mmHg. Analisando o texto, e a reação não balanceada, dada abaixo, assinale a alternativa CORRETA.
http://www.ecycle.com.br/.
