Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
Em seu artigo “Mecanismos Redox de Compostos Aromáticos, Aminoácidos e Proteínas, em Eléctrodos de Carbono”, Teodor Adrian Enache, pesquisador da Faculdade de Ciências e Tecnologia, da Universidade de Coimbra, Portugal, discute a reação entre oxidação e aminoácidos.
Assinale a afirmação verdadeira a respeito dessa
reação.
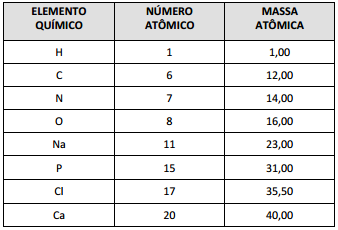
DADOS QUE PODEM SER USADOS NESTA PROVA
O fermento é responsável pelo aumento do volume de um bolo, que acontece assim: a temperatura alta faz com que o fermento libere gás carbônico; esse gás se expande e faz o bolo crescer. Quando adicionado na massa, o fermento sofre uma transformação química a partir da reação entre bicarbonato de sódio e fosfato dihidrogenado de cálcio:
NaHCO3 + Ca(H2 PO4)2 —–>
Assinale a opção que apresenta corretamente os
produtos ajustados dessa reação química.
DADOS QUE PODEM SER USADOS NESTA PROVA

Um carro estacionado na sombra durante um dia, com as janelas fechadas, pode conter de 400 a 800 mg de benzeno. Se está ao sol, o nível de benzeno subirá de 2000 a 4000 mg. A pessoa que entra no carro e mantém as janelas fechadas, inevitavelmente aspirará, em rápida sucessão, excessivas quantidades dessa toxina. O benzeno é uma toxina que afeta os rins e o fígado, e o que é pior, é extremamente difícil para o organismo expulsar esta substância tóxica. Por essa razão, os manuais de instruções de uso dos carros indicam que antes de ligar o ar condicionado, deve-se primeiramente abrir as janelas e deixá-las abertas por um tempo de dois minutos.
Com relação ao benzeno, assinale a afirmação
correta.
DADOS QUE PODEM SER USADOS NESTA PROVA

DADOS QUE PODEM SER USADOS NESTA PROVA

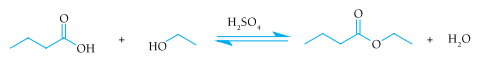
As curvas de produção de butanoato de etila para as reações realizadas com e sem a utilização do ácido sulfúrico como catalisador estão apresentadas no seguinte gráfico:
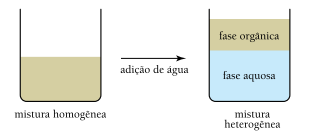
Na fase aquosa da mistura heterogênea, apenas a substância orgânica de maior solubilidade em água está presente. Essa substância é denominada:
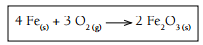
Nesse processo, o oxigênio sofre a transformação química denominada:
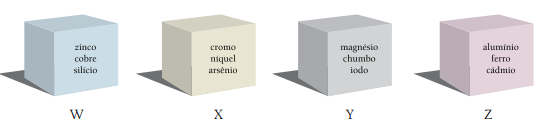
A única caixa que contém apenas metais está indicada pela seguinte letra:
Os aminoácidos que possuem um centro quiral apresentam duas formas enantioméricas. Observe, abaixo, a estrutura química de quatro aminoácidos.
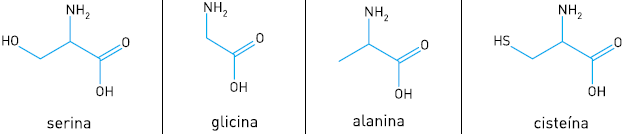
O único desses aminoácidos que não apresenta enantiômeros é:
Uma amostra de 5 L de benzeno líquido, armazenada em um galpão fechado de 1500 m3 contendo ar atmosférico, evaporou completamente. Todo o vapor permaneceu no interior do galpão.
Técnicos realizaram uma inspeção no local, obedecendo às normas de segurança que indicam o tempo máximo de contato com os vapores tóxicos do benzeno.
Observe a tabela:
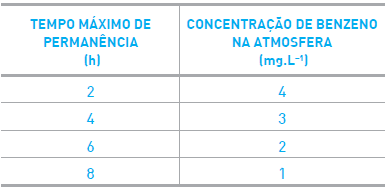
Considerando as normas de segurança, e que a densidade do benzeno líquido é igual a 0,9
g.mL-1, o tempo máximo, em horas, que os técnicos podem permanecer no interior do galpão,
corresponde a:
Segundo pesquisas recentes, há uma bactéria que parece ser capaz de substituir o fósforo por arsênio em seu DNA.
Uma semelhança entre as estruturas atômicas desses elementos químicos que possibilita essa substituição é:
Observe, a seguir, a fórmula estrutural do ácido ascórbico, também conhecido como vitamina C:
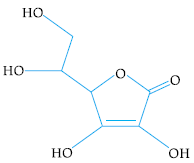
Para uma dieta saudável, recomenda-se a ingestão diária de 2,5 x 10-4 mol dessa vitamina, preferencialmente obtida de fontes naturais, como as frutas.
Considere as seguintes concentrações de vitamina C:
- polpa de morango: 704 mg.L-1;
- polpa de laranja: 528 mg.L-1.
Um suco foi preparado com 100 mL de polpa de morango, 200 mL de polpa de laranja e 700 mL de água.
A quantidade desse suco, em mililitros, que fornece a dose diária recomendada de vitamina C é:
Em um experimento, uma pequena amostra de soro sanguíneo foi colocada em um suporte poroso embebido em meio formado por solução salina mantida em pH 6,0. Através desse suporte estabeleceu-se um circuito elétrico, como mostra o esquema abaixo.

|
Proteína |
pI (valores médios) |
|
|
nome |
velocidade de migração |
|
|
gamaglobulina |
v1 |
8,0 |
|
betaglobulina |
v2 |
7,6 |
|
alfaglobulina |
v3 |
6,6 |
|
albumina |
v4 |
4,8 |
A ordem crescente das velocidades de migração das proteínas citadas é:
A bola utilizada em uma partida de futebol é uma esfera de diâmetro interno igual a 20 cm. Quando cheia, a bola apresenta, em seu interior, ar sob pressão de 1,0 atm e temperatura de 27 ºC.
Considere π = 3, R = 0,080 atm.L.mol-1 .k-1 e, para o ar, comportamento de gás ideal e massa molar igual a 30 g.mol-1.
No interior da bola cheia, a massa de ar, em gramas, corresponde a:
Um laboratório realiza a análise de células utilizando uma solução fisiológica salina com pH neutro. O laboratório dispõe de apenas quatro substâncias que poderiam ser usadas no preparo dessa solução: HCl, NaCl, NaOH e NaHCO3 .
Dentre elas, a que deve ser escolhida para uso na análise está indicada em:
