Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
Uma forma de evitar a poluição ambiental causada pelo descarte de óleo de cozinha usado é reaproveitá-lo para produzir sabões, que são sais de ácidos carboxílicos. Para tanto, faz-se reagir o óleo com solução aquosa fortemente alcalina de NaOH e/ou KOH.
Nessa reação, conhecida como reação de saponificação, forma-se também um outro produto que é o
A cor das flores de diversas plantas ocorre devido à presença de substâncias, como as antocianinas, que atuam como indicadores ácido-base. Assim, conforme o pH do solo, a cor das flores pode variar. É o caso das hortênsias, que apresentam cor azul em solos ácidos e rosa em solos alcalinos.
Caso uma pessoa queira cultivar hortênsias de cor rosa, em um jardim cujo solo seja ácido, ela deverá corrigir o pH e, para isso, poderá misturar à terra, em quantidade adequada,
Um veículo de passeio, movido a gasolina, deixou a capital paulista com o tanque cheio, dirigindo-se a uma cidade do interior situada a 480 km, na região noroeste do estado. Ao final da viagem, verificou-se que o consumo médio do veículo foi de 16 km por litro de combustível.
Admitindo-se que a composição média da gasolina seja dada pela fórmula C8 H18 e que a combustão seja completa, conclui-se que o volume de CO2 , em litros, medido nas CATP e lançado ao ar durante a viagem foi de, aproximadamente,
Dados
Volume molar de gás nas CATP = 25 L / mol
Densidade da gasolina = 8 x 102 g / L
Massas molares em g / mol:
C = 12; H = 1 e O = 16
Os elementos cloro (Z = 17) e iodo (Z = 53) pertencem ao mesmo grupo da tabela periódica. Assim, átomos neutros desses elementos apresentam igual
I. número de prótons;
II. número de elétrons na camada de valência;
III. eletronegatividade.
É correto o que se afirma em
I O cloreto de cálcio é um sólido iônico.
II O cloreto de cálcio sólido é um bom condutor de eletricidade.
III Para ser usado como “secante de armário", o sal deve ser higroscópico.
São verdadeiras:
A solubilidade desse composto a 25.0°C, em água pura e em uma solução de pH igual a 13.00, será, respectivamente, em molL-1 :
O sal formado entre o ácido bórico e o hidróxido de magnésio apresenta a seguinte composição centesimal:
PCl3(g) + Cl2(g) PCl5(g)
Sob essas condições, o efeito causado sobre a referida reação é:
Em relação à eletrólise,
O Nobel da Paz de 2013 foi entregue à Organização para a Proibição das Armas Químicas, o que reforçou a preocupação mundial quanto à erradicação desse tipo de armamento. O VX é um agente químico altamente tóxico, classificado como arma de destruição em massa. A eliminação desse agente é realizada via degradação, que pode ocorrer por três caminhos, tal como ilustrado. No entanto, o composto “5" também pode atuar como arma química, por ser muito mais tóxico que os outros produtos da degradação.
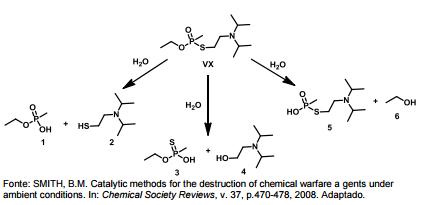
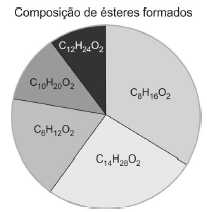
O ácido carboxílico presente em maior quantidade na amostra analisada é o:
Com relação à isomeria, numere a coluna da direita de acordo com sua correspondência com a coluna da esquerda.
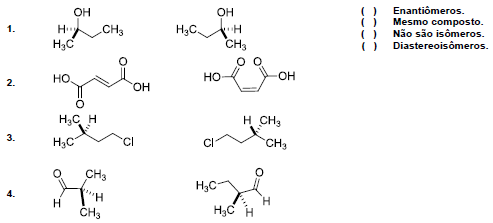
Assinale a alternativa que apresenta a numeração correta da coluna da direita, de cima para baixo.
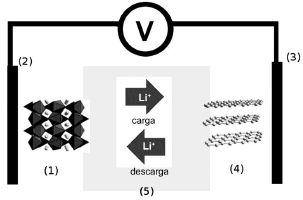
Quando a bateria está em uso (atuando como uma pilha), o anodo corresponde ao componente:
(Dados: Kf = 1,86 ºC.kg.mol-1; M(g.mol-1): Cl = 35,5; Na = 23)
A diferença na temperatura de fusão (em °C) na mistura obtida ao se dissolver 200 g de sal de cozinha em 1 kg de água, em relação à água pura, é de:
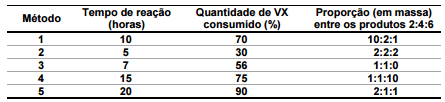
A terceira etapa é realizada por meio dos métodos de:

Os polímeros biodegradáveis podem ser empregados na confecção de sacolas plásticas utilizadas nos supermercados. Esses polímeros apresentam estruturas de cadeias alifáticas com grupos funcionais hidrolisáveis.
A fórmula estrutural que representa o monômero de um polímero biodegradável é
Um certo polímero é produzido a partir de um monômero, que é um hidrocarboneto que contém somente uma instauração. A análise elementar por combustão completa de 0,5 mol de moléculas desse hidrocarboneto resultou em 1,5 mol de moléculas de CO2 .
A massa molar, em g.mol–1 , desse monômero é