Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
O hidrogênio para células a combustível de uso automotivo poderá ser obtido futuramente a partir da reação de reforma do etanol. Atualmente, nessa reação, são gerados subprodutos indesejados: etanal (I) e etanoato de etila (II). Porém, pesquisadores da UNESP de Araraquara verificaram que, com o uso de um catalisador adequado, a produção de hidrogênio do etanol poderá ser viabilizada sem subprodutos.
(Revista Pesquisa Fapesp, 234, agosto de 2015. Adaptado)
A reação da transformação de etanol no subproduto I e a substância que reage com o etanol para formação do subproduto II são, correta e respectivamente,
O fenol é um composto químico altamente tóxico encontrado em efluentes (resíduos aquosos de processos químicos) de variadas indústrias como a farmacêutica, de tintas e de papel e celulose.
O fenol se ioniza em água de acordo com o equilíbrio

A concentração máxima permitida para fenóis em águas
não cloradas é de 0,1 mg/L. Contudo, em águas cloradas, a
concentração máxima permitida para fenóis pela resolução
n° 357 do CONAMA é de 0,003 mg/L.
Os químicos do laboratório de análises de uma indústria de tintas prepararam cinco amostras, cada uma com 1000 mL de efluente do processo, contendo fenol. A quatro delas, adicionaram – a cada uma separadamente – 0,1 mol das seguintes substâncias: KBr, NaCl, NaOH, HCl. A quinta amostra foi mantida apenas com o efluente. Após esse procedimento, fizeram análises da concentração de fenolato, C6 H5 O– , por instrumento de medida, em cada uma das cinco amostras.
Ao final dessa pesquisa, os químicos concluíram corretamente que a amostra que apresentou maior concentração de íon fenolato, dentre as cinco, foi aquela contendo
O fenol é um composto químico altamente tóxico encontrado em efluentes (resíduos aquosos de processos químicos) de variadas indústrias como a farmacêutica, de tintas e de papel e celulose.
O fenol se ioniza em água de acordo com o equilíbrio

A concentração máxima permitida para fenóis em águas
não cloradas é de 0,1 mg/L. Contudo, em águas cloradas, a
concentração máxima permitida para fenóis pela resolução
n° 357 do CONAMA é de 0,003 mg/L.
Em um experimento em laboratório de química, montou-se uma célula eletrolítica de acordo com o esquema:
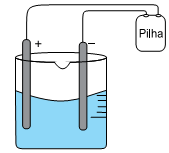
Usaram-se como eletrodo dois bastões de grafite, uma solução aquosa 1,0 mol.L–1 de CuSO4 em meio ácido a 20 °C e uma pilha.
Alguns minutos, após iniciado o experimento, observaram-se a formação de um sólido de coloração amarronzada sobre a superfície do eletrodo de polo negativo e a formação de bolhas na superfície do eletrodo de polo positivo.
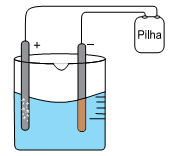
Com base nos potenciais de redução a 20 °C,
Cu2+ (aq) +2e– → Cu (s) + 0,34 V
2H+ (aq) + 2e– → H2 (g) 0,00 V
O2 (g) + 4H+ (aq) + 4e– → H2O (l) + 1,23 V
É correto afirmar que se forma cobre no
O ácido nítrico é um importante insumo para produção de fertilizantes, explosivos e tintas. Sua produção industrial é feita pelo processo Ostwald, em três etapas que podem ser representadas pelas reações:
I. 6 NH3 (g) + 15/2 O2 (g) → 6 NO (g) + 9 H2O (g) ∆H = – 1378 kJ
II. 6 NO (g) + 3 O2 (g) → 6 NO2 (g) ∆H = – 339 kJ
III. 6 NO2
(g) + 2 H2O (g) → 4 HNO3
(aq) + 2 NO (g) ∆H = – 270 kJ
O ácido nítrico é um importante insumo para produção de fertilizantes, explosivos e tintas. Sua produção industrial é feita pelo processo Ostwald, em três etapas que podem ser representadas pelas reações:
I. 6 NH3 (g) + 15/2 O2 (g) → 6 NO (g) + 9 H2O (g) ∆H = – 1378 kJ
II. 6 NO (g) + 3 O2 (g) → 6 NO2 (g) ∆H = – 339 kJ
III. 6 NO2
(g) + 2 H2O (g) → 4 HNO3
(aq) + 2 NO (g) ∆H = – 270 kJ
Os palitos de fósforo são dispositivos simples empregados para fazer fogo. A chama se produz por meio de reações que ocorrem com as substâncias da “cabeça” do palito. Quando o palito é esfregado na superfície áspera da lateral da caixa, as substâncias reagem formando Sb2 O5 , KCl e SO2 . Essa reação é muito exotérmica e rápida e promove a reação de combustão e a propagação da chama pela madeira do palito.
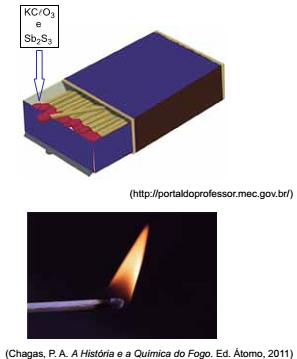
Equacionando-se e fazendo-se corretamente o balanceamento
da reação que ocorre pelo atrito da cabeça do palito de
fósforo com a lateral da caixa, a soma dos menores valores
inteiros dos coeficientes estequiométricos é
A medicina tem desenvolvido diversos tratamentos para pacientes com câncer de cérebro. Em um deles, o paciente ingere o composto borofenilalanina. Essa molécula que contém o isótopo boro-10 tem afinidade pelas células cerebrais. Após a ingestão, o paciente é submetido a um feixe de nêutrons. Cada isótopo de boro-10 captura um nêutron e forma um isótopo instável que se fissiona em duas espécies menores e emite ainda radiação gama. Dessa maneira, a célula tumoral é atingida pela energia das emissões do processo de fissão e é destruída.
(www.nipe.unicamp.br/enumas/admin/resources/uploads/robertovicente_hasoluçao.pdf.Adaptado)
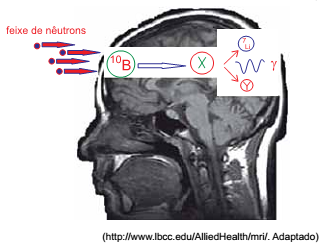
O isótopo instável, representado por X, e a espécie emitida
na fissão, representada por Y, são, respectivamente,
O nitrito de sódio, NaNO2 , é um conservante de alimentos processados a partir de carnes e peixes. Os dados de solubilidade deste sal em água são apresentados na tabela.

Em um frigorífico, preparou-se uma solução saturada de
NaNO2
em um tanque contendo 0,5 m3
de água a 50°C. Em
seguida, a solução foi resfriada para 20°C e mantida nessa
temperatura. A massa de NaNO2
, em kg, cristalizada após o
resfriamento da solução, é
Considere: Densidade da água = 1 g/mL
Na figura, apresenta-se um biodigestor utilizado em áreas rurais. Ele é totalmente vedado, criando um ambiente anaeróbio onde os microrganismos degradam o material orgânico (dejetos e restos de ração), transformando-o em biogás. O gasômetro é o compartimento superior do biodigestor e serve para a armazenagem de gases. Ele é inflável e feito de uma manta de material plástico impermeável (PVC). No gasômetro, a pressão e a temperatura são constantemente iguais às da atmosfera.
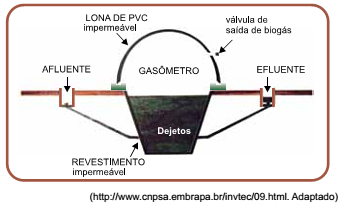
Considere uma quantidade fixa de gás no gasômetro descrito
no texto. A variação percentual do volume do gás contido
nesse compartimento ao longo de um dia, em que a temperatura
varia de mínima de 17 °C, durante a madrugada, para a
máxima de 38 °C, no decorrer do dia, é próxima de
Um novo tipo de material especial, seleneto de bismuto, capaz de conduzir eletricidade em sua superfície, não em seu interior, quando em contato com um semicondutor, arseneto de gálio, resulta em um material que conduz eletricidade em várias direções e com níveis de energia diferentes. Esses compostos seguem a fórmula XyYx e suas ligações podem ser consideradas iônicas. Os íons negativos seguem a regra do octeto, enquanto que os íons positivos apresentam a mesma carga que o íon alumínio.
(Revista Pesquisa Fapesp, 234, agosto de 2015. Adaptado)
Os índices y e x nas fórmulas do material especial e do semicondutor são, respectivamente:
Água de coco Ingredientes Água de coco, água de coco concentrada reconstituída, sacarose (menos de 1% para padronização do produto) e conservador INS223
Óleo de coco Ingredientes Óleo vegetal de coco-da-bahia (Cocos nucifera L.) extraído em primeira prensagem mecânica.
Para melhorar as qualidades nutricionais desses produtos, o fabricante pretende adicionar a cada um deles vitaminas solúveis, tendo como opção aquelas representadas na figura.
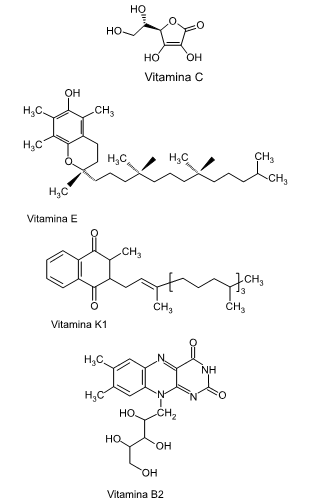
Considerando as vitaminas apresentadas, são mais solúveis na água de coco as __ (I)__ , e mais solúveis no óleo de coco as __(II)__ .
Assinale a alternativa que preenche corretamente as lacunas.
A bioluminescência é o fenômeno de emissão de luz visível por certos organismos vivos, resultante de uma reação química entre uma substância sintetizada pelo próprio organismo(luciferina) e oxigênio molecular, na presença de uma enzima (luciferase). Como resultado dessa reaçãobioquímica é gerado um produto em um estado eletronicamenteexcitado (oxiluciferina*). Este produto, por suavez, desativa-se por meio da emissão de luz visível, formandoo produto no estado normal ou fundamental (oxiluciferina).Ao final, a concentração de luciferase permanece constante.

O esquema ilustra o mecanismo geral da reação de bio-luminescência de vagalumes, no qual são formados dois produtos diferentes em estados eletronicamente excitados,responsáveis pela emissão de luz na cor verde ou na cor vermelha.

A bioluminescência é o fenômeno de emissão de luz visível por certos organismos vivos, resultante de uma reação química entre uma substância sintetizada pelo próprio organismo(luciferina) e oxigênio molecular, na presença de uma enzima (luciferase). Como resultado dessa reaçãobioquímica é gerado um produto em um estado eletronicamenteexcitado (oxiluciferina*). Este produto, por suavez, desativa-se por meio da emissão de luz visível, formandoo produto no estado normal ou fundamental (oxiluciferina).Ao final, a concentração de luciferase permanece constante.

O esquema ilustra o mecanismo geral da reação de bio-luminescência de vagalumes, no qual são formados dois produtos diferentes em estados eletronicamente excitados,responsáveis pela emissão de luz na cor verde ou na cor vermelha.

Com base nas informações apresentadas no texto e considerando a velocidade da luz igual a 300.000 km· s–1, é correto afirmar que uma das funções orgânicas e a fórmula molecular da forma aniônica da oxiluciferina do vagalume responsável pela emissão de luz com frequência igual a 4,8 × 1014 Hz são, respectivamente,
A bioluminescência é o fenômeno de emissão de luz visível por certos organismos vivos, resultante de uma reação química entre uma substância sintetizada pelo próprio organismo(luciferina) e oxigênio molecular, na presença de uma enzima (luciferase). Como resultado dessa reaçãobioquímica é gerado um produto em um estado eletronicamenteexcitado (oxiluciferina*). Este produto, por suavez, desativa-se por meio da emissão de luz visível, formandoo produto no estado normal ou fundamental (oxiluciferina).Ao final, a concentração de luciferase permanece constante.

O esquema ilustra o mecanismo geral da reação de bio-luminescência de vagalumes, no qual são formados dois produtos diferentes em estados eletronicamente excitados,responsáveis pela emissão de luz na cor verde ou na cor vermelha.

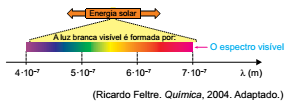
A luz branca é composta por ondas eletromagnéticas de todas as frequências do espectro visível. O espectro de radiação emitido por um elemento, quando submetido a um arco elétrico ou a altas temperaturas, é descontínuo e apresenta uma de suas linhas com maior intensidade, o que fornece “uma impressão digital” desse elemento. Quando essas linhas estão situadas na região da radiação visível, é possível identificar diferentes elementos químicos por meio dos chamados testes de chama. A tabela apresenta as cores características emitidas por alguns elementos no teste de chama:
Elemento Cor
sódio laranja
potássio violeta
cálcio vermelho-tijolo
cobre azul-esverdeada
A luz branca é composta por ondas eletromagnéticas de todas as frequências do espectro visível. O espectro de radiação emitido por um elemento, quando submetido a um arco elétrico ou a altas temperaturas, é descontínuo e apresenta uma de suas linhas com maior intensidade, o que fornece “uma impressão digital” desse elemento. Quando essas linhas estão situadas na região da radiação visível, é possível identificar diferentes elementos químicos por meio dos chamados testes de chama. A tabela apresenta as cores características emitidas por alguns elementos no teste de chama:
Elemento Cor
sódio laranja
potássio violeta
cálcio vermelho-tijolo
cobre azul-esverdeada
Leia o texto e examine a tabela para responder à questão.
O ano de 2015 foi eleito como o Ano Internacional da Luz, devido à importância da luz para o Universo e para a humanidade. A iluminação artificial, que garantiu a iluminação noturna, impactou diretamente a qualidade de vida do homem e o desenvolvimento da civilização. A geração de luz em uma lâmpada incandescente se deve ao aquecimento de seu filamento de tungstênio provocado pela passagem de corrente elétrica, envolvendo temperaturas ao redor de 3000 °C.
Algumas informações e propriedades do isótopo estável do tungstênio estão apresentadas na tabela.
Símbolo W
Número atômico 74
Número de massa 184
Ponto de fusão 3422 °C
Eletronegatividade (Pauling) 2,36
Densidade 19,3 g· cm–3
Leia o texto e examine a tabela para responder à questão.
O ano de 2015 foi eleito como o Ano Internacional da Luz, devido à importância da luz para o Universo e para a humanidade. A iluminação artificial, que garantiu a iluminação noturna, impactou diretamente a qualidade de vida do homem e o desenvolvimento da civilização. A geração de luz em uma lâmpada incandescente se deve ao aquecimento de seu filamento de tungstênio provocado pela passagem de corrente elétrica, envolvendo temperaturas ao redor de 3000 °C.
Algumas informações e propriedades do isótopo estável do tungstênio estão apresentadas na tabela.
Símbolo W
Número atômico 74
Número de massa 184
Ponto de fusão 3422 °C
Eletronegatividade (Pauling) 2,36
Densidade 19,3 g· cm–3
Pouco depois de a bomba atômica ser lançada sobre o Japão, cientistas inventaram outra arma, ainda mais poderosa: a bomba de hidrogênio. Em 1957, a bomba H explodia no atol de Bikini, no Oceano Pacífico.Tinha um poder de destruição cinco vezes maior do que todas as bombas convencionais detonadas durante a Segunda Guerra Mundial.
Prevendo a corrida armamentista, Albert Einstein declarou em 1945: “O poder incontrolado do átomo mudou tudo, exceto nossa forma de pensar e, por isso, caminhamos para uma catástrofe sem paralelo".

Disponível em:<http://www.sitedecuriosidades.com/curiosidade/as-bombas-atomicas-lancadas-sobre-o-japao.html><http://www.nippo.com.br/4.hiroshima/>.<http://pt.wikipedia.org/wiki/Bombardeamentos de Hiroshima e Nagasaki>. Acesso em: 2 set. 15.
Em relação à temática e às informações apresentadas no texto, assinale a alternativa correta.