Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
TEXTO 4
Aprígio – Saia, Dália! (Dália abandona o quarto, correndo, em desespero. Sogro e genro, face a face) Vim aqui para.
Arandir (para o sogro quase chorando) – Está satisfeito?
Aprígio – Vim aqui.
Arandir (na sua cólera) – Está satisfeito? O senhor é um dos responsáveis. Eu acho que é o senhor. O senhor que está por trás...
Aprígio – Quem sabe?
Arandir – Por trás desse repórter. O senhor teve a coragem de. Ou pensa que eu não sei? Selminha me contou. Contou tudo! O senhor fez insinuações. Insinuações! A meu respeito!
Aprígio – Você quer me.
Arandir (sem ouvi-lo) – O senhor fez tudo! Tudo pra me separar de Selminha!
Aprígio – Posso falar?
Arandir (erguendo a voz) – O senhor não queria o nosso casamento!
Aprígio (violento) – Escuta! Vim aqui saber! Escuta! Você conhecia esse rapaz?
Arandir (desesperado) – Nunca vi.
Aprígio – Era um desconhecido?
Arandir – Juro! Por tudo que há de mais! Que nunca, nunca!
Aprígio – Mentira!
Arandir (desesperado) – Vi pela primeira vez!
Aprígio – Cínico! (muda de tom, com uma Ferocidade) Escuta! Você conhecia o rapaz. Conhecia! Eram amantes! E você matou. Empurrou o rapaz!
Arandir (violento) – Deus sabe!
Aprígio – Eu não acredito em você. Ninguém acredita. Os jornais, as rádios! Não há uma pessoa, uma única, em toda a cidade. Ninguém!
Arandir (com a voz estrangulada) – Ninguém acredita, mas eu! Eu acredito, acredito em mim!
Aprígio – Você, olha!
Arandir – Selminha há de acreditar!
Aprígio (fora de si) – Cala a boca! (muda de tom) Eu te perdoaria tudo! Eu perdoaria o casamento. Escuta! Ainda agora, eu estava na porta ouvindo. Ouvi tudo. Você tentando seduzir a minha filha menor!
Arandir – Nunca!
Aprígio – Mas eu perdoaria, ainda. Eu perdoaria que você fosse espiar o banho da cunhada. Você quis ver a cunhada nua.
Arandir – Mentira!
Aprígio – Eu perdoaria tudo. (mais violento) Só não perdoo o beijo no asfalto. Só não perdoo o beijo que você deu na boca de um homem!
Arandir (para si mesmo) – Selminha!
Aprígio (muda de tom, suplicante) – Pela última vez, diz! Eu preciso saber! Quero a verdade! A verdade! Vocês eram amantes? (sem esperar a resposta, furioso) Mas não responda. Eu não acredito. Nunca, nunca, eu acreditarei. (numa espécie de uivo) Ninguém acredita!
Arandir – Vou buscar minha mulher. (Aprígio recua, puxando o revólver.)
Aprígio (apontando) – Não se mexa! Fique onde está!
Arandir (atônito) – O senhor vai.
Aprígio – Você era o único homem que não podia casar com a minha filha! O único!
Arandir (atônito e quase sem voz) – O senhor me odeia porque. Deseja a própria filha. É paixão. Carne. Tem ciúmes de Selminha.
Aprígio (num berro) – De você! (estrangulando a voz) Não de minha filha. Ciúmes de você. Tenho! Sempre. Desde o teu namoro, que eu não digo o teu nome. Jurei a mim mesmo que só diria teu nome a teu cadáver. Quero que você morra sabendo. O meu ódio é amor. Por que beijaste um homem na boca? Mas eu direi o teu nome. Direi teu nome a teu cadáver. (Aprígio atira, a primeira vez. Arandir cai de joelhos. Na queda, puxa uma folha de jornal, que estava aberta na cama. Torcendo-se. abre o jornal, como uma espécie de escudo ou bandeira. Aprígio atira, novamente, varando o papel impresso. Num espasmo de dor, Arandir rasga a folha. E tomba, enrolando-se no jornal. Assim morre.) Aprígio – Arandir! (mais forte) Arandir! (um último canto) Arandir!
(RODRIGUES, Nelson. O beijo no asfalto. Rio
de Janeiro: Nova Fronteira, 1995. p. 101-104.)
O Texto 4, fragmento final da peça O beijo no asfalto, de Nelson Rodrigues, mostra um personagem que se defende de acusações e outro que acredita estar ouvindo mentiras. A mentira parece ser inerente à condição humana. Aparelhos como o polígrafo e o chamado “soro da verdade” foram criados no intuito de detectar se uma pessoa está ou não mentindo. O princípio ativo do soro da verdade é o pentotal sódico, ou sódio tiopental, cuja fórmula molecular é C11H17N2 NaSO2 . Essa substância parece quebrar a inibição dos pacientes. Trata-se de um barbitúrico, portanto derivado do ácido barbitúrico, ou uma malonilureia, que penetra quase que imediatamente no Sistema Nervoso Central (SNC). Sabe-se que a penetração no SNC depende da lipossolubilidade da molécula. Segundo a bula do medicamento, a dose máxima recomendada para maior segurança do paciente é de 1 grama do fármaco, aplicada intermitentemente, de acordo com a necessidade e a resposta do paciente.
Com base nas informações sobre o tiopental sódico, assinale a única alternativa correta:
TEXTO 3
O acendedor de lampiões
Lá vem o acendedor de lampiões da rua!
Este mesmo que vem infatigavelmente,
Parodiar o sol e associar-se à lua
Quando a sombra da noite enegrece o poente!
Um, dois, três lampiões, acende e continua
Outros mais a acender imperturbavelmente,
À medida que a noite aos poucos se acentua
E a palidez da lua apenas se pressente.
Triste ironia atroz que o senso humano irrita: —
Ele que doura a noite e ilumina a cidade,
Talvez não tenha luz na choupana em que habita.
Tanta gente também nos outros insinua
Crenças, religiões, amor, felicidade,
Como este acendedor de lampiões da rua!
(LIMA, Jorge de. Melhores poemas. 3. ed. São Paulo: Global, 2006. p. 25)
O Texto 3 faz referência à iluminação, elemento fundamental na vida das pessoas. Dos lampiões a querosene ao LED, tem-se uma ideia de como a evolução da iluminação contribuiu para a transformação das cidades e dos hábitos das pessoas. Essa evolução vai da utilização do óleo ao querosene, deste ao gás, chegando finalmente à energia elétrica. Foi apenas no século XX que a eletricidade passou a ser popularmente usada na iluminação das ruas. Vários tipos de lâmpadas foram utilizadas em iluminação pública: incandescente, halógena, fluorescente linear, lâmpada mista, lâmpada a vapor de mercúrio, lâmpada a vapor de sódio de alta pressão. A tecnologia é desenvolvida, aplicada e melhorada. Atualmente, além da eficiência e economia, o light emitter diode ou LED é a tecnologia que permite melhor relação com o meio ambiente, porque não utiliza mercúrio, que é tóxico.
(Adaptado de CODI - Comitê de Distribuição - Substituição de lâmpadas incandescentes no sistema de iluminação pública - Relatório SCPE.33.01 de 13 out. 1988. Comitê de Distribuição (CODI), Abradee, Rio de Janeiro, 1988.)
O LED é um componente eletrônico semicondutor que transforma energia elétrica em luz. Essa transformação é diferente daquela encontrada nas lâmpadas convencionais, que utilizam filamentos metálicos, radiação ultravioleta e descarga de gases. No arsenieto de gálio
ou no fosfeto de gálio, por exemplo, ocorre a eletroluminescência,
que é a emissão de luz com aplicação de uma
fonte elétrica.
I-No estado fundamental, o átomo de arsênio apresenta um orbital completo na camada de valência.
II-Fósforo e arsênio apresentam cinco camadas de energia em sua distribuição eletrônica, no estado fundamental, pois estão localizados no mesmo período da tabela periódica.
III-Apenas os elétrons da camada de valência do gá- lio em seu estado fundamental apresentam valores idênticos para todos os números quânticos – principal, secundário, magnético e spin.
IV-No LED, a maior parte da energia absorvida é dissipada na forma de calor.
É(são) correto(s) apenas o(s) item(ns):
TEXTO 2
VI
Para entenderes bem o que é a morte e a vida, basta contar-te como morreu minha avó.
— Como foi?
— Senta-te.
Rubião obedeceu, dando ao rosto o maior interesse possível, enquanto Quincas Borba continuava a andar.
— Foi no Rio de Janeiro, começou ele, defronte da Capela Imperial, que era então Real, em dia de grande festa; minha avó saiu, atravessou o adro, para ir ter à cadeirinha, que a esperava no Largo do Paço. Gente como formiga. O povo queria ver entrar as grandes senhoras nas suas ricas traquitanas. No momento em que minha avó saía do adro para ir à cadeirinha, um pouco distante, aconteceu espantar-se uma das bestas de uma sege; a besta disparou, a outra imitou-a, confusão, tumulto, minha avó caiu, e tanto as mulas como a sege passaram-lhe por cima. Foi levada em braços para uma botica da Rua Direita, veio um sangrador, mas era tarde; tinha a cabeça rachada, uma perna e o ombro partidos, era toda sangue; expirou minutos depois.
— Foi realmente uma desgraça, disse Rubião.
— Não.
— Não?
— Ouve o resto. Aqui está como se tinha passado o caso. O dono da sege estava no adro, e tinha fome, muita fome, porque era tarde, e almoçara cedo e pouco. Dali pôde fazer sinal ao cocheiro; este fustigou as mulas para ir buscar o patrão. A sege no meio do caminho achou um obstáculo e derribou-o; esse obstáculo era minha avó. O primeiro ato dessa série de atos foi um movimento de conservação: Humanitas tinha fome. Se em vez de minha avó, fosse um rato ou um cão, é certo que minha avó não morreria, mas o fato era o mesmo; Humanitas precisa comer. Se em vez de um rato ou de um cão, fosse um poeta, Byron ou Gonçalves Dias diferia o caso no sentido de dar matéria a muitos necrológios; mas o fundo subsistia. O universo ainda não parou por lhe faltarem alguns poemas mortos em flor na cabeça de um varão ilustre ou obscuro; mas Humanitas (e isto importa, antes de tudo) Humanitas precisa comer.
Rubião escutava, com a alma nos olhos, sinceramente desejoso de entender; mas não dava pela necessidade a que o amigo atribuía a morte da avó. Seguramente o dono da sege, por muito tarde que chegasse à casa, não morria de fome, ao passo que a boa senhora morreu de verdade, e para sempre. Explicou-lhe, como pôde, essas dúvidas, e acabou perguntando-lhe:
— E que Humanitas é esse?
— Humanitas é o princípio. Mas não, não digo nada, tu não és capaz de entender isto, meu caro Rubião; falemos de outra coisa.
— Diga sempre.
Quincas Borba, que não deixara de andar, parou alguns instantes.
— Queres ser meu discípulo?
— Quero.
— Bem, irás entendendo aos poucos a minha filosofia; no dia em que a houveres penetrado inteiramente, ah! nesse dia terás o maior prazer da vida, porque não há vinho que embriague como a verdade. Crê-me, o Humanitismo é o remate das coisas; e eu, que o formulei, sou o maior homem do mundo. Olha, vês como o meu bom Quincas Borba está olhando para mim? Não é ele, é Humanitas...
— Mas que Humanitas é esse?
— Humanitas é o principio. Há nas coisas todas certa substância recôndita e idêntica, um princípio único, universal, eterno, comum, indivisível e indestrutível, — ou, para usar a linguagem do grande Camões:
Uma verdade que nas coisas anda,
Que mora no visíbil e invisíbil.
Pois essa sustância ou verdade, esse princípio indestrutível é que é Humanitas. Assim lhe chamo, porque resume o universo, e o universo é o homem. Vais entendendo?
— Pouco; mas, ainda assim, como é que a morte de sua avó...
— Não há morte. O encontro de duas expansões, ou a expansão de duas formas, pode determinar a supressão de uma delas; mas, rigorosamente, não há morte, há vida, porque a supressão de uma é a condição da sobrevivência da outra, e a destruição não atinge o princípio universal e comum. Daí o carácter conservador e benéfico da guerra. Supõe tu um campo de batatas e duas tribos famintas. As batatas apenas chegam para alimentar uma das tribos, que assim adquire forças para transpor a montanha e ir à outra vertente, onde há batatas em abundância; mas, se as duas tribos dividirem em paz as batatas do campo, não chegam a nutrir-se suficientemente e morrem de inanição. A paz, nesse caso, é a destruição; a guerra é a conservação. Uma das tribos extermina a outra e recolhe os despojos. Daí a alegria da vitória, os hinos, aclamações, recompensas públicas e todos os demais efeitos das ações bélicas. Se a guerra não fosse isso, tais demonstrações não chegariam a dar-se, pelo motivo real de que o homem só comemora e ama o que lhe é aprazível ou vantajoso, e pelo motivo racional de que nenhuma pessoa canoniza uma ação que virtualmente a destrói. Ao vencido, ódio ou compaixão; ao vencedor, as batatas.
— Mas a opinião do exterminado?
— Não há exterminado. Desaparece o fenômeno; a substância é a mesma. Nunca viste ferver água? Hás de lembrar-te que as bolhas fazem-se e desfazem-se de contínuo, e tudo fica na mesma água. Os indivíduos são essas bolhas transitórias.
— Bem; a opinião da bolha...
— Bolha não tem opinião. Aparentemente, há nada mais contristador que uma dessas terríveis pestes que devastam um ponto do globo? E, todavia, esse suposto mal é um benefício, não só porque elimina os organismos fracos, incapazes de resistência, como porque dá lugar à observação, à descoberta da droga curativa. A higiene é filha de podridões seculares; devemo-la a milhões de corrompidos e infectos. Nada se perde, tudo é ganho. Repito, as bolhas ficam na água. Vês este livro? É Dom Quixote. Se eu destruir o meu exemplar, não elimino a obra, que continua eterna nos exemplares subsistentes e nas edições posteriores. Eterna e bela, belamente eterna, como este mundo divino e supradivino.
(ASSIS, Machado de. Quincas Borba. 18. ed. São
Paulo: Ática, 2011. p. 26-28.)
Considere o fragmento do Texto 2: “— Não há exterminado. Desaparece o fenômeno; a substância é a mesma. Nunca viste ferver água? Hás de lembrar-te que as bolhas fazem-se e desfazem-se de contínuo, e tudo fica na mesma água. Os indivíduos são essas bolhas transitórias.”
Ao se colocar uma panela com água mineral para aquecer em um fogão em Goiânia, observa-se que, mesmo que a temperatura esteja abaixo do ponto de evaporação, há a formação de bolhas. Somente com a temperatura próxima de 98°C é que há a evolução muito violenta de bolhas.
A respeito dessa constatação, analise as afirmativas a seguir:
I-A pressão de vapor diminui com a altitude.
II-Crioscopia é a passagem de água do meio menos concentrado para o meio mais concentrado.
III-Ebulioscopia é o estudo do abaixamento da temperatura de ebulição da solução devido à presença de um soluto.
IV-A formação de bolhas na etapa inicial do aquecimento também tem a ver com os gases dissolvidos na água.
Em relação às proposições analisadas, assinale a
única alternativa cujos itens estão todos corretos:
TEXTO 1
Queimada
À fúria da rubra língua
do fogo
na queimada
envolve e lambe
o campinzal
estiolado em focos
enos
sinal.
É um correr desesperado
de animais silvestres
o que vai, ali, pelo mundo
incendiado e fundo,
talvez,
como o canto da araponga
nos vãos da brisa!
Tambores na tempestade
[...]
E os tambores
e os tambores
e os tambores
soando na tempestade,
ao efêmero de sua eterna idade.
[...]
Onde?
Eu vos contemplo
à inércia do que me leva
ao movimento
de naufragar-me
eternamente
na secura de suas águas
mais à frente!
Ó tambores
ruflai
sacudi suas dores!
Eu
que não me sei
não me venho
por ser
busco apenas ser somenos
no viver,
nada mais que isso!
(VIEIRA, Delermando. Os tambores da tempestade. Goiânia: Poligráfica, 2010. p. 164, 544, 552.)
O Texto 1 faz menção a água, bem cuja disponibilidade e qualidade têm causado sérias preocupações. Sabe-se que em muitos casos, a água da chuva pode superar em qualidade as águas superficiais e subterrâneas. Por não entrar em contato com o solo nem estar diretamente sujeita ao lançamento de poluentes de origem antropogênica, a água da chuva pode constituir uma fonte alternativa, com qualidade razoável para diversos usos. A qualidade do ar tem grande influência sobre a qualidade da água da chuva. Dependendo da localização, suas características podem ser afetadas por fatores naturais ou pela ação antrópica. Em regiões próximas a oceanos, há maior probabilidade de se encontrar sódio, potássio, magnésio e cloro na água da chuva. A concentração de cloretos na água da chuva varia de 0,1 a 2,0 mgL-1, podendo chegar a valores maiores, dependendo da proximidade com os oceanos.
Considerando-se uma precipitação de 100 mm, ou seja, que em 1m2 , houve a precipitação de 100 litros de água, e que a água desse 1 m2 possa ser armazenada em um recipiente, qual seria a quantidade molar aproximada de íons cloreto presente nessa água?
Considere a média aritmética da concentração de íons cloreto para realizar esse cálculo.
Assinale a alternativa que apresenta a resposta correta:
INSTRUÇÃO: Responder à questão com base nas informações a seguir.
A erva-mate (Ilex paraguaiensis) contém muitas substâncias orgânicas, as quais podem ter ação benéfica no organismo. As estruturas moleculares de algumas substâncias presentes nessa planta são mostradas a seguir:
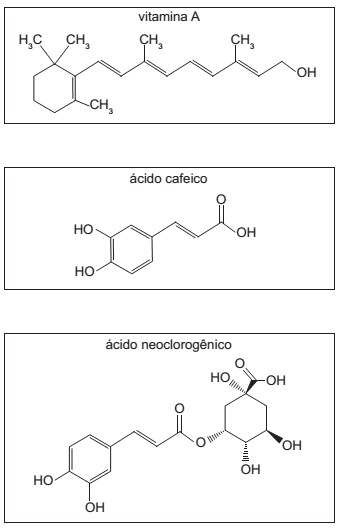
Considerando essas estruturas, é correto afirmar que
O funcionamento da pilha comumente utilizada em controles remotos de TV, também conhecida como pilha seca ou de Leclanché, é expresso pela equação química a seguir:
Zn(s) + 2 MnO2(s) + 2 NH4 +(aq) → Zn2+(aq) + Mn2 O3(s) + 2 NH3(g) + H2O(l)
Um dos motivos de essa pilha não ser recarregável é
porque
INSTRUÇÃO: Para responder à questão, analise as informações a seguir, contidas em um rótulo de alimento.
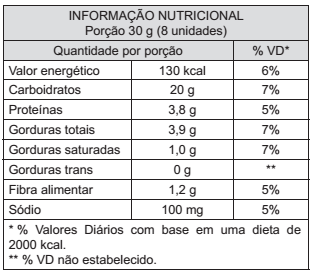
De acordo com as informações apresentadas, é correto
afirmar:
INSTRUÇÃO: Para responder à questão, analise o
texto e a tabela a seguir.
Os indicadores ácido-base são úteis para se obter informações sobre o pH de soluções. Alguns, como o extrato de repolho roxo, podem ser preparados facilmente por qualquer pessoa na cozinha. Outros, como o tornassol, a fenolftaleína e o alaranjado de metila, são mais usados em laboratórios. Eles apresentam uma cor em pH ácido, outra cor em pH básico, e tonalidades intermediárias em uma faixa limitada de pH (faixa de mudança de cor), conforme pode ser observado na tabela.

De acordo com as informações acima, é correto afirmar:
A pólvora é considerada a primeira mistura explosiva, usada na China, na Arábia e na Índia. Há textos chineses antigos que a denominam “substância química do fogo”, mesmo sendo uma mistura de nitrato de potássio, carvão e enxofre. A combustão da pólvora pode ser representada pela seguinte equação:
4KNO3 + 7C + S → 3CO2 + 3 CO + 2 N2 + K2CO3 + K2S
O que caracteriza a explosão é o súbito aumento de
volume, com grande liberação de energia. Nas CNTP,
520 g de pólvora produzem, por explosão,
INSTRUÇÃO: Para responder à questão, analise
as informações a seguir.
Em uma aula de Ciências, no Ensino Fundamental, o professor adicionou uma colher de cloreto de sódio a um copo cheio de água à temperatura ambiente e agitou o sistema. Ao perguntar às crianças o que havia ocorrido, algumas responderam que o sal não estava mais no copo.
Levando em conta a situação apresentada, a correta
explicação para o fenômeno é:
INSTRUÇÃO: Para responder à questão, analise
as informações a seguir.
O fogo sempre foi objeto de fascínio e instrumento de extrema utilidade para o ser humano. Mesmo hoje, com o uso cada vez mais disseminado da energia elétrica, não deixamos de utilizar o fogo no cotidiano: ainda queimamos carvão na churrasqueira, lenha na lareira, gás liquefeito de petróleo no fogão e parafina nas velas.
Sobre esse assunto, são apresentadas as seguintes afirmativas:
I. A combustão é uma reação redox em que o comburente age como oxidante.
II. Na combustão do gás de cozinha, há produção de água, mas na do carbono não há.
III. A velocidade de combustão do carvão em pedaços é igual à do carvão em pó.
IV. As reações de combustão são exotérmicas e liberam gás carbônico.
Em relação à combustão, são corretas somente as
afirmativas
INSTRUÇÃO: Para responder à questão, analise o texto a seguir.
Construir casas e edifícios exige uma escolha criteriosa
de materiais de construção, levando em conta aspectos
de segurança, durabilidade e custo adequado. Por
exemplo, certos elementos, como vigas, colunas e paredes,
precisam ter boas propriedades mecânicas; as
partes expostas devem resistir à erosão causada pela
água e pelo ar; o risco de incêndio deve ser minimizado
pelo uso de materiais não inflamáveis.
Consideradas essas exigências, duas substâncias que
poderiam estar presentes na composição desses materiais
são:
O ânion bromato reage com o ânion brometo em meio ácido gerando a substância simples bromo segundo a equação:
BrO3-(aq) + 5 Br-(aq) + 6 H+ (aq) → 3 Br2(aq) + 3 H2O(l)
A cinética dessa reação foi estudada a partir do acompanhamento dessa reação a partir de diferentes concentrações iniciais das espécies
BrO3- (aq), Br- (aq) e H+(aq).
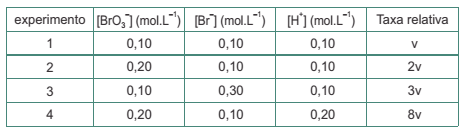
Ao analisar esse processo foram feitas as seguintes observações:
I. Trata-se de uma reação de oxidorredução.
II. O ânion brometo (Br- ) é o agente oxidante do processo.
III. A lei cinética dessa reação é v = k[BrO3 ][Br ][H+ ]2 .
Pode-se afirmar que estão corretas
Foram estudados, independentemente, o comportamento de uma amostra de 100 mg do radioisótopo bismuto-212 e o de uma amostra de 100 mg do radioisótopo bismuto-214. Essas espécies sofrem desintegração radioativa distinta,sendo o bismuto-212 um emissor β, enquanto que o bismuto-214 é um emissor α.
As variações das massas desses radioisótopos foram acompanhadas ao longo dos experimentos. O gráfico a seguir ilustra as observações experimentais obtidas durante as primeiras duas horas de acompanhamento.
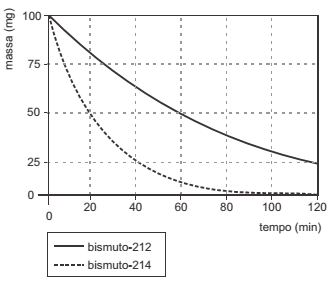
Sobre esse experimento é INCORRETO afirmar que
O eugenol e o anetol são substâncias aromáticas presentes em óleos essenciais, com aplicações nas indústrias de cosméticos e farmacêutica. O eugenol está presente principalmente nos óleos de cravo, canela e sassafrás, já o anetol é encontrado nos óleos essenciais de anis e anis estrelado.
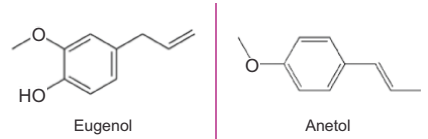
Sobre esses compostos foram feitas as seguintes afirmações.
I. Ambos apresentam isomeria geométrica.
II. O eugenol apresenta funções fenol e éter, enquanto que o anetol apresenta função éter.
III. A fórmula molecular do eugenol é C10H12O2 , enquanto que o anetol apresenta fórmula molecular C10H12O.
IV. O anetol apresenta temperatura de ebulição maior do que o eugenol.
Estão corretas APENAS as afirmações:
O β-caroteno é um corante antioxidante presente em diversos vegetais amarelos ou laranja, como a cenoura, por exemplo. Em nosso organismo, o β-caroteno é um importante precursor do retinal e do retinol (vitamina A), substâncias envolvidas no metabolismo da visão.
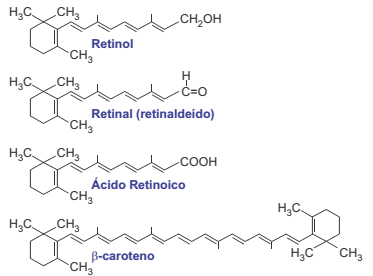
Sobre as reações envolvidas no metabolismo do retinol foram feitas as seguintes afirmações:
I. β-caroteno, retinal e retinol são classificados, respectivamente, como hidrocarboneto, aldeído e álcool.
II. O retinol sofre oxidação ao ser transformado em retinal.
III. Retinal é um isômero de função do retinol.
IV. O retinal é reduzido ao se transformar em ácido retinoico.
Estão corretas APENAS as afirmações:
Dado: 1 pm equivale a 10-12m
O raio covalente de um átomo corresponde à distância entre o núcleo atômico e a camada de valência. O comprimento de ligação é, aproximadamente, a soma dos raios covalentes dos átomos envolvidos

Na fórmula estrutural do ácido acético, encontramos ligações C-H, O-H, C-O, C=O e C-C.
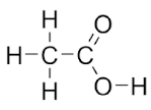
Considerando a distribuição eletrônica e o número
atômico de cada átomo, a alternativa que apresenta
valores coerentes para os comprimentos de ligação
presentes na molécula de ácido acético é
Após determinado processo industrial, obtém-se uma mistura contendo sulfato de sódio (Na2 SO4 ) e carbonato de sódio (Na2CO3 ). Uma amostra contendo 10,0 g dessa mistura foi completamente neutralizada com 100 mL de uma solução 1,00 mol.L–1 de HCl.
O sulfato de sódio não reage com ácido clorídrico e o carbonato de sódio reage segundo a reação representada a seguir.
Na2CO3 (s) + 2 HCl(aq) → 2 NaCl(aq) + CO2(g) + H2O(l)
O teor de carbonato de sódio na mistura é de