Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
I. Metilamina (CH3NH2) possui caráter básico, pois o par de elétrons livres do átomo de nitrogênio pode receber próton dando origem a uma ligação.
II. Metilamina (CH3NH2) possui caráter básico, pois um dos átomos de hidrogênio ligados ao átomo de nitrogênio pode ser doado facilmente.
III. Fenol (C6H5OH) possui um caráter ácido fraco, mas ainda assim ele pode doar íon H+ quando reage, por exemplo, com uma base forte.
É correto APENAS o que se afirma em
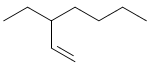
Segundo as regras da IUPAC, a nomenclatura do composto
representado acima é
A seguir está representada a estrutura do ácido fumárico.
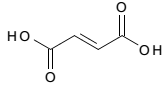
A respeito desse ácido, é correto afirmar que ele possui
Considere: M(Cu) = 63,5 g mol-1
M(S) = 32 g mol-1
Considere: R = 0,082 atm L mol-1 K-1
M(O2) = 32 g mol-1
Num processo de fissão nuclear, um nêutron colidiu com o núcleo de um isótopo do urânio levando à formação de dois núcleos menores e liberação de nêutrons que produziram reações em cadeia com liberação de grande quantidade de energia. Uma das possíveis reações nucleares nesse processo é representada por:
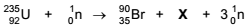
O produto X, formado na fissão nuclear indicada acima, é
um isótopo do elemento químico:
I. KCl(aq) + AgNO3(aq) → AgCl(s) + KNO3(aq)
II. FeCl3(aq) + SnCl2(aq) → FeCl2(aq) + SnCl4(aq)
III. Ba(OH)2(aq) + H2SO4(aq) → BaSO4(s) + H2O(l)
Nessas equações, os símbolos (aq), (s) e (l) representam, respectivamente, “espécies químicas dissolvidas em água", “espécies químicas no estado sólido" e “espécies químicas no estado líquido".
É correto afirmar que, na reação indicada, são íons espectadores
As reações de cloração (halogenação) dos alcanos ocorrem na presença de gás cloro (Cl2 ), sob condições ideais, e geralmente dão origem a diversos produtos contendo átomos de cloro. Por exemplo, no caso da cloração do metilbutano (C5 H12), é possível obter quatro produtos diferentes. Esse tipo de reação é classificada como
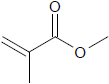
Essa substância possui fórmula molecular
A seguir está representada a estrutura da dihidrocapsaicina, uma substância comumente encontrada em pimentas e pimentões.
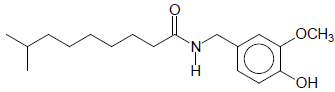
Na dihidrocapsaicina, está presente, entre outras, a função orgânica
O metanol é um álcool utilizado como combustível em alguns tipos de competição automotiva, por exemplo, na Fórmula Indy. A queima completa (ver reação termoquímica abaixo) de 1 L de metanol (densidade 0,80 g mL-1 ) produz energia na forma de calor (em kJ) e CO2 (em gramas) nas seguintes quantidades respectivamente:
2 CH3 OH(l) + 3 O2(g) → 4 H2 O(l) + 2 CO2(g) ; ∆H = 1453 kJ
Considere: M(CH3
OH) = 32 g mol-1
M(CO2
) = 44 g mol-1